Clear Sky Science · pl
Kryptonimowa redundancja między PAR1b a PAR1a, dwoma członkami rodziny kinaz PAR1, w przeżywalności myszy z delecją PAR1b
Jak komórki znajdują plany awaryjne na uszkodzone DNA
Nasze komórki nieustannie stykają się z uszkodzeniami DNA, a gdy mechanizmy naprawcze zawodzą, skutkiem może być rak lub śmierć rozwojowa. Badanie to przygląda się zaskakującemu mechanizmowi ratunkowemu u myszy: kiedy brakuje kluczowego białka, które pomaga słynnemu genowi związanym z rakiem, BRCA1, wykonać swoje zadanie, bliski krewny cicho wkracza do akcji. Praca pokazuje, jak wczesne embriony mogą przeprogramować swoje systemy kontroli genów, żeby przetrwać, dając nowe spojrzenie na to, dlaczego niektóre defekty genetyczne są śmiertelne, podczas gdy inne są niespodziewanie tolerowane.
Rodzina organizatorów komórkowych z ukrytą rolą
Naukowcy skupili się na rodzinie enzymów nazywanych kinazami PAR1, które pomagają komórkom utrzymać wewnętrzną organizację. Jeden z członków rodziny, PAR1b, wcześniej wykazano, że kieruje BRCA1 do jądra komórkowego, gdzie BRCA1 nadzoruje dokładną naprawę DNA i chroni wrażliwe miejsca replikacji. Usunięcie BRCA1 u myszy jest śmiertelne we wczesnym stadium rozwoju embrionalnego, co podkreśla jego znaczenie. A jednak, co zagadkowe, myszy całkowicie pozbawione PAR1b przeżywają do dorosłości, mimo że PAR1b działa upstream względem BRCA1. Ta rozbieżność zasugerowała, że inna kinaza PAR1 może w pewnych warunkach dyskretnie zastępować PAR1b.
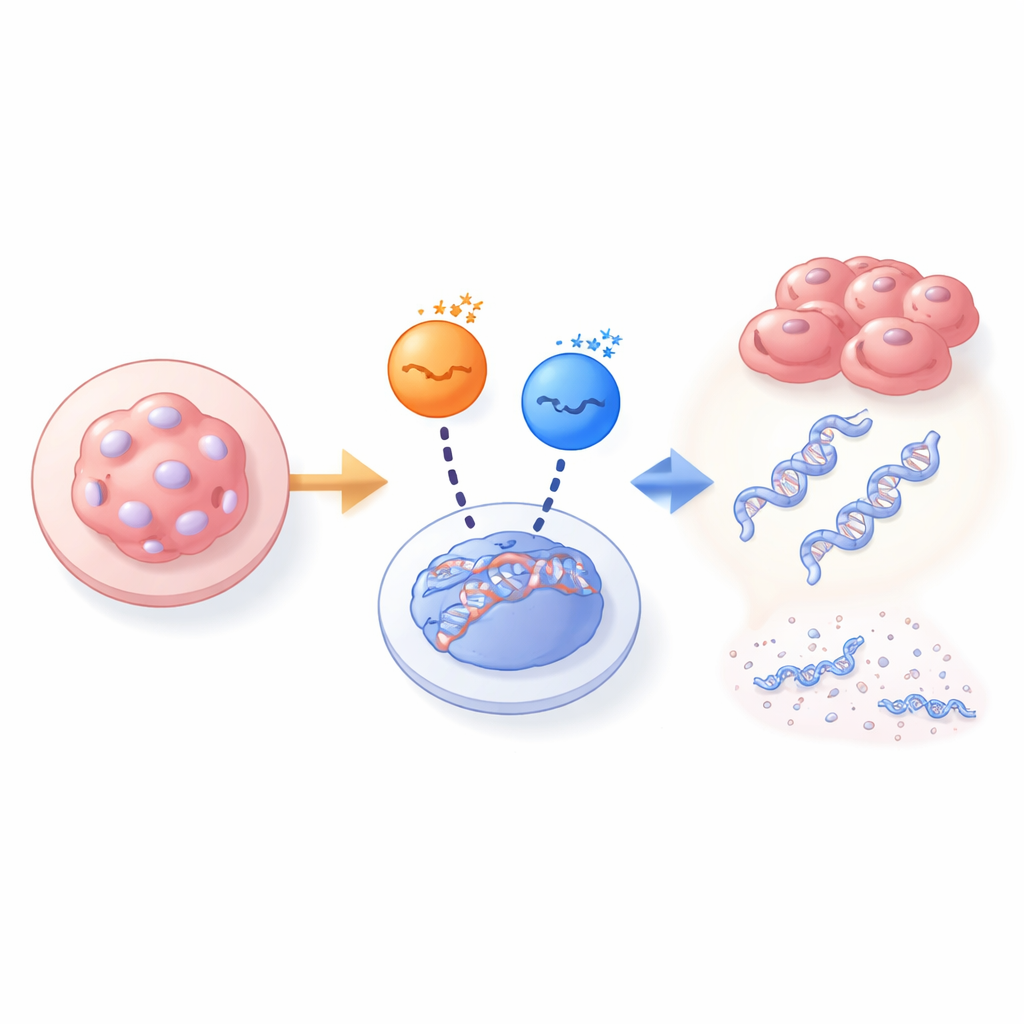
Kiedy jedna kinaza zawodzi, inna przejmuje obowiązki
Aby zbadać tę tajemnicę, zespół porównał fibroblasty embrionalne myszy pochodzące z normalnych embrionów i z embrionów całkowicie pozbawionych PAR1b. W normalnych komórkach wyłączenie PAR1b wyraźnie zmniejszało poziom BRCA1 w jądrze i prowadziło do narastania markerów złamań DNA, co z kolei blokowało wzrost komórek. Redukcja innych kinaz PAR1 (PAR1a, PAR1c, PAR1d) miała niewielki efekt. Jednak w komórkach pochodzących z embrionów pozbawionych PAR1b BRCA1 wciąż był obecny w jądrze, a DNA pozostawało względnie nienaruszone, mimo braku PAR1b. W tych komórkach null dla PAR1b usunięcie PAR1a stało się śmiertelne, podczas gdy usunięcie PAR1c lub PAR1d nie miało takiego efektu. Ta zmiana zależności pokazała, że PAR1a przejęła rolę PAR1b w kierowaniu BRCA1, ale tylko w embrionach, które od samego początku brakowały PAR1b.
Wczesne przeprogramowanie epigenetyczne jako strategia przetrwania
Naukowcy podejrzewali, że ten ukryty system zapasowy wiąże się z epigenetyką — sposobem pakowania DNA i chemicznych znaków, które włączają lub wyłączają geny bez zmiany kodu genetycznego. Przy użyciu badania całego genomu mierzącego dostępność chromatyny znaleźli tysiące regionów, w których dostępność DNA różniła się między komórkami normalnymi a null dla PAR1b. Wiele zmian dotyczyło genów kontrolujących sposób zwijania i modyfikowania chromosomów, co sugeruje szerokie przeprogramowanie sieci kontroli genów. Jednym z wyróżniających się efektów był wpływ na gen 53BP1, białko, które normalnie kieruje komórki ku szybszemu i mniej dokładnemu sposobowi naprawy DNA, przeciwnemu wobec dokładniejszej metody BRCA1. W komórkach null dla PAR1b ciało genu 53BP1 było bardziej skondensowane, a poziomy jego RNA i białka znacznie niższe.
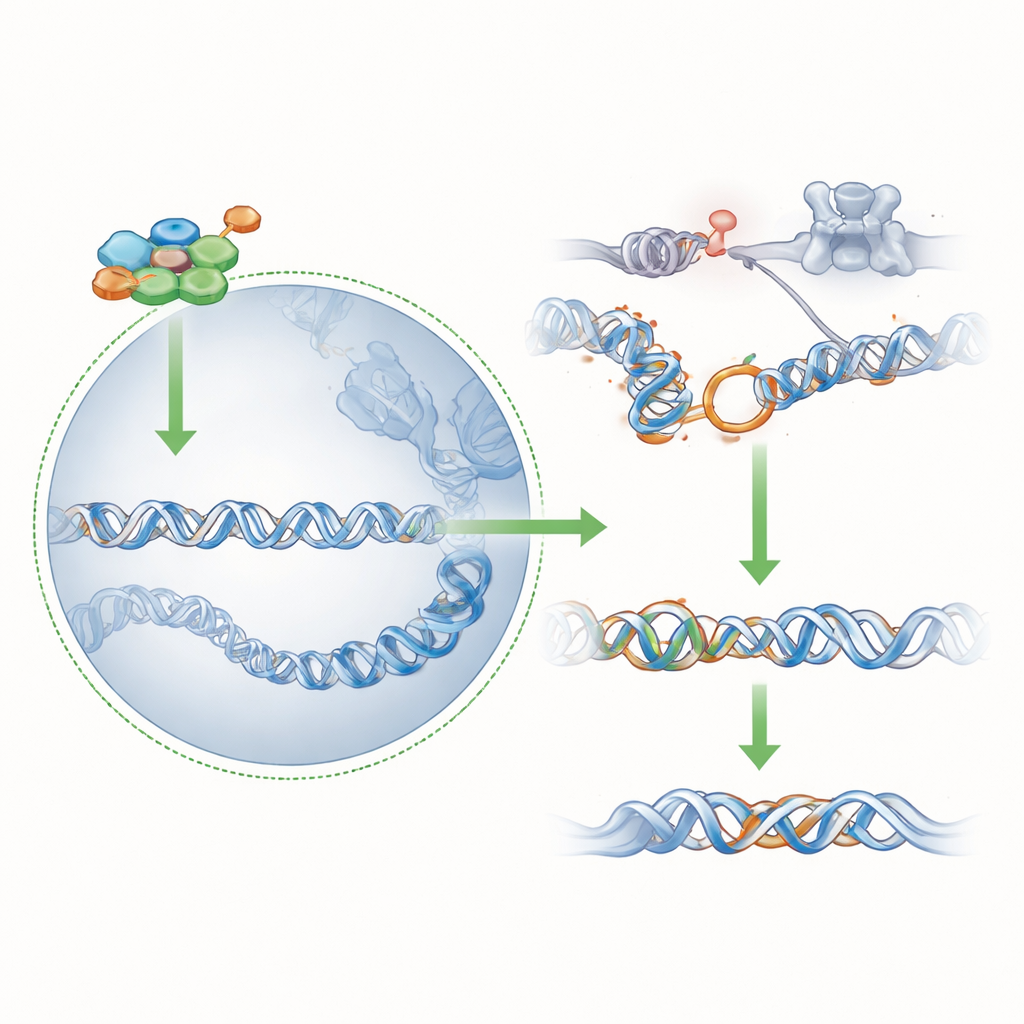
Przechylenie równowagi między ścieżkami naprawy
Poprzez obniżenie poziomu 53BP1, embrion efektywnie zmniejsza swoją zależność od pełnej siły BRCA1: nawet umiarkowana ilość BRCA1 w jądrze, dostarczana przez PAR1a zamiast PAR1b, może teraz zapewnić wystarczająco dokładną naprawę, by utrzymać komórki przy życiu. Eksperymenty z użyciem bakteryjnego białka, które wyłącza wszystkie kinazy PAR1, potwierdziły, że jądrowa obecność BRCA1 w komórkach null dla PAR1b nadal zależy od aktywności rodziny PAR1, konkretnie PAR1a. Razem wyniki kreślą obraz, w którym wczesna utrata PAR1b wywołuje szybkie przeformowanie chromatyny i sieci naprawy DNA, uciszając przeciwnika BRCA1 (53BP1) i odsłaniając zdolność PAR1a do zastąpienia PAR1b.
Co to oznacza dla chorób i terapii
Praca wprowadza pojęcie „kryptonimowej redundancji”: funkcji zapasowej, która istnieje, ale zwykle pozostaje uśpiona i staje się widoczna tylko wtedy, gdy kluczowy element zostanie utracony bardzo wcześnie w rozwoju. U myszy pozwala to embrionom przetrwać utratę PAR1b, w przeciwieństwie do utraty samego BRCA1. Wyniki sugerują również, że niektórzy ludzie z uszkadzającymi wariantami PAR1b mogą przeżyć, ponieważ uruchamiają się podobne mechanizmy zapasowe, choć nie bez możliwych konsekwencji dla funkcji mózgu, metabolizmu czy ryzyka nowotworu. W dłuższej perspektywie zrozumienie, jak wczesne dostosowania epigenetyczne uciszają 53BP1 i przesuwają kontrolę BRCA1 z PAR1b na PAR1a, mogłoby zainspirować strategie celowego odtwarzania tych zmian — albo by chronić komórki utraciły PAR1b, albo by precyzyjnie modulować szlaki naprawy DNA w terapii nowotworów.
Cytowanie: Murata-Kamiya, N., Del Valle Lazarte, A.A., Kikuchi, I. et al. Cryptic redundancy between PAR1b and PAR1a, two members of the PAR1 kinase family, in the survival of PAR1b-knockout mice. Sci Rep 16, 5971 (2026). https://doi.org/10.1038/s41598-026-39737-4
Słowa kluczowe: BRCA1, naprawa DNA, redundancja kinaz, regulacja epigenetyczna, rozwój embrionalny