Clear Sky Science · pl
Mutacja Sema5A związana z zaburzeniem ze spektrum autyzmu p.Arg676Cys uruchamia sygnalizację Arf6/FE65 i powoduje nieprawidłową morfogenezę komórek
Jak drobna zmiana może zaburzyć okablowanie mózgu
Zaburzenie ze spektrum autyzmu wpływa na to, jak ludzie komunikują się, wchodzą w interakcje i reagują na otaczający świat, jednak biologiczne etapy prowadzące od zmiany w DNA do zmienionej funkcji mózgu często pozostają tajemnicą. To badanie zagłębia się w jedną z takich zmian genetycznych w białku „kierującym” wzrostem w mózgu o nazwie Sema5A i pokazuje, z wyjątkową dokładnością, jak pojedyncza wymieniona jednostka budulcowa w tym białku może skłonić młode komórki nerwowe do nadmiernego wydłużania i splątania wypustek. Zrozumienie tego mikroskopijnego błędu w okablowaniu może w przyszłości pomóc naukowcom opracować terapie, które skierują komórki mózgowe z powrotem ku zdrowszemu kształtowi.
Komórki mózgowe, które rosną za daleko
Podczas rozwoju mózgu młode komórki nerwowe wysyłają długie, cienkie wypustki, które poszukują właściwych partnerów, tworząc obwody leżące u podstaw myślenia i zachowania. Ten wzrost musi być ściśle kontrolowany: zbyt mało rozgałęzień i komórki nie nawiążą połączeń; zbyt dużo i obwody mogą stać się hałaśliwe lub błędnie sparowane. Wcześniejsze prace pokazały, że wersja Sema5A związana z autyzmem, w której jedna aminokwasowa reszta na pozycji 676 zostaje zmieniona z argininy na cysteinę, powoduje, że komórki nerwowe w hodowli tworzą wyjątkowo długie wypustki. Nowe badanie miało odkryć, które wewnętrzne przełączniki i białka pomocnicze ten mutant Sema5A wykorzystuje, by napędzać taki niekontrolowany wzrost.
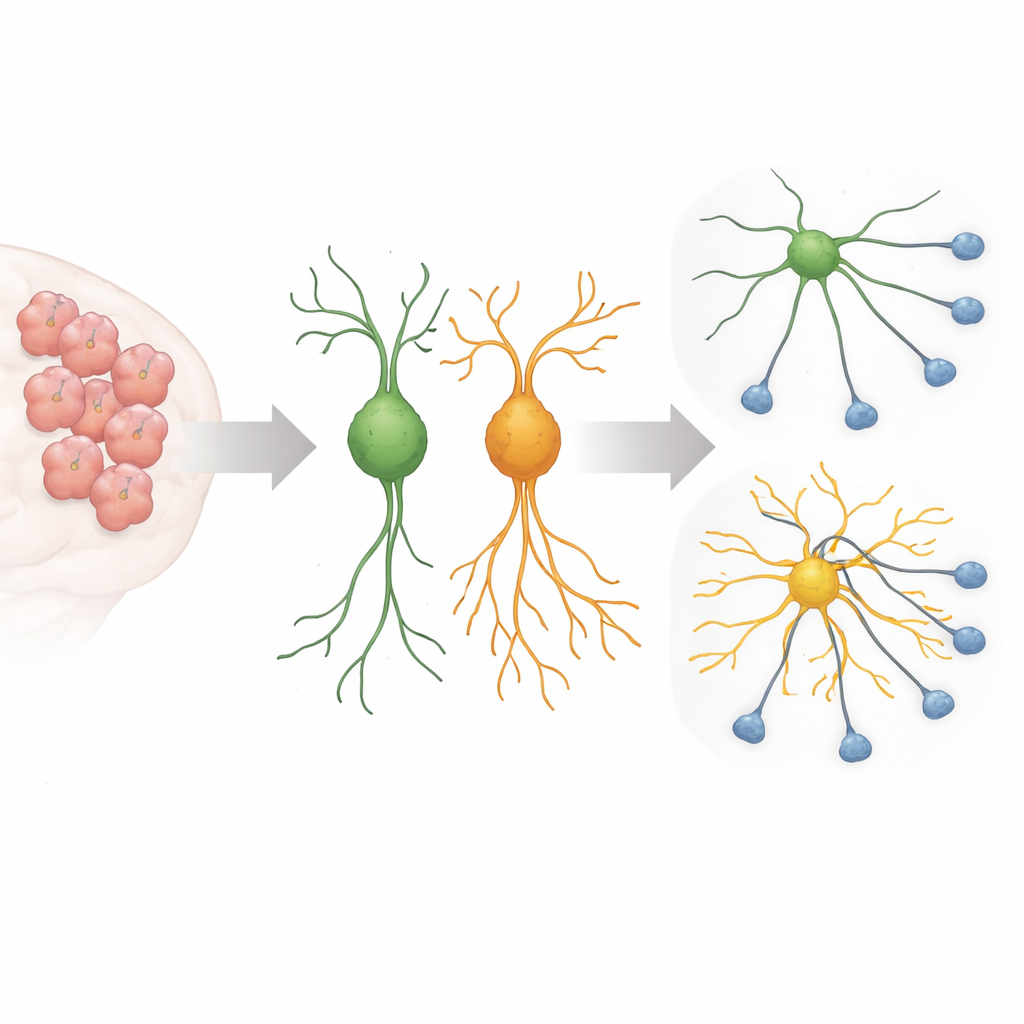
Mylący sygnał wewnątrz komórki
Naukowcy skupili się na małym przełączniku molekularnym zwanym Arf6 oraz na białku rusztowaniowym FE65, obu znanych z udziału w kształtowaniu błon komórkowych i wewnętrznego szkieletu, który podtrzymuje wypustki komórek. Wykorzystując system CRISPR–Cas13 do selektywnego zmniejszenia poziomów tych białek w komórkach podobnych do nerwowych pochodzących od myszy oraz w pierwotnych komórkach mózgowych myszy, odkryli, że obniżenie Arf6 lub FE65 wyraźnie ogranicza nadmierny wzrost wywołany przez mutant Sema5A. Długie, pajęcze wypustki skurczyły się do bardziej typowych długości, a markery dojrzewania neuronów zmalały, co sugeruje, że efekt tej mutacji w dużym stopniu zależy od tego konkretnego szlaku sygnałowego.
Połączenie z „silnikiem” kształtu komórki
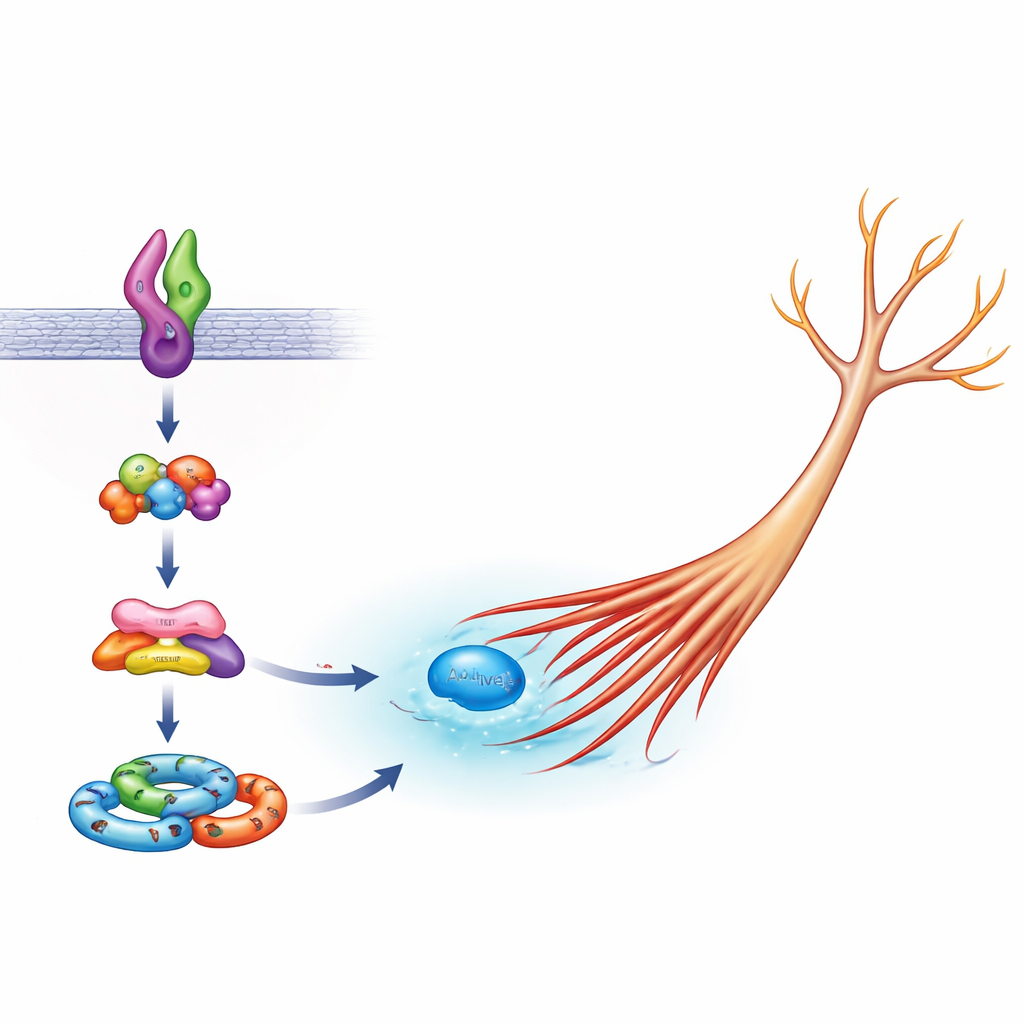
W komórkach nerwowych rodzina cząsteczek działa jako „silnik” kształtu, kontrolując aktynę — główny filament strukturalny w wypustkach komórkowych. Kluczowy członek tej rodziny, Rac1, zwykle uaktywnia się, by wspomóc wydłużanie neurytów, lecz nadmierna aktywność może napędzać niekontrolowany wzrost. Zespół wykazał, że w komórkach z normalnym Sema5A Arf6 jest potrzebny do zwykłej aktywacji Rac1 podczas zdrowego wydłużania, podczas gdy FE65 nie jest niezbędny. Jednak w obecności mutant Sema5A zarówno Arf6, jak i FE65 stają się krytyczne: obniżenie któregokolwiek z nich albo zalanie komórki samym regionem FE65 wiążącym jego partnera ELMO2 zmniejszało nadmierną aktywność Rac1 w kierunku normy. Sugeruje to, że szkodliwa wersja Sema5A korzysta specyficznie z kompleksu Arf6–FE65–ELMO2–DOCK5, by nadmiernie stymulować Rac1 i skłaniać neurity do zbyt dalekiego wzrostu.
Zatapione centrum partnerów sygnałowych
Aby zobaczyć, jak te elementy ze sobą współdziałają, naukowcy przyjrzeli się też „sygnalosomom” opartym na ELMO2 — skupiskom białek, które montują się, aby przekazywać sygnały wzrostowe. Gdy Arf6 lub FE65 zostały zredukowane, komórki wyrażające mutant Sema5A tworzyły mniej tych kompleksów ELMO2 w ciałach komórkowych i na końcach rosnących wypustek, co zgadza się z ideą, że Arf6 i FE65 pomagają budować maszynerię zamieniającą mutację Sema5A w fizyczną zmianę kształtu komórki. Praca wpisuje się w szerszy obraz, w którym małe przełączniki molekularne, takie jak Arf6 i Rac1, wspierane przez rusztowania pokroju FE65, działają jako centralne węzły łączące wiele genów związanych z autyzmem z ostateczną architekturą obwodów mózgowych.
Dlaczego ten mikroskopijny łańcuch ma znaczenie
Dla osoby niezaznajomionej z tematem alfabetyczna zbitka nazw białek może wydawać się odległa od codziennego doświadczenia autyzmu. Tymczasem to badanie oferuje konkretne ogniwo: śledzi, jak precyzyjna zmiana genetyczna w Sema5A może nadmiernie uaktywnić określony łańcuch białek pomocniczych, powodując, że komórki nerwowe wydłużają swoje wypustki za bardzo i potencjalnie łączą mózg w nietypowy sposób. Wskazując Arf6, FE65 i kompleks sygnałowy ELMO2 jako kluczowe ogniwa tego łańcucha, praca podkreśla potencjalne cele dla przyszłych leków. W zasadzie leki, które łagodnie stonują ten nadaktywowany szlak, mogłyby kiedyś pomóc skorygować leżące u podstaw zmiany kształtu komórek związane z formami autyzmu powiązanymi z Sema5A, dodając ważny element do większej układanki zaburzeń neurorozwojowych.
Cytowanie: Takahashi, M., Yako, H., Miyamoto, Y. et al. Autism spectrum disorder-associated Sema5A p.Arg676Cys drives Arf6/FE65 signaling and aberrant cell morphogenesis. Sci Rep 16, 9423 (2026). https://doi.org/10.1038/s41598-026-39722-x
Słowa kluczowe: zaburzenie ze spektrum autyzmu, mutacja Sema5A, morfogeneza neuronów, sygnalizacja Rac1, szlak Arf6 FE65