Clear Sky Science · pl
Celowanie w określone typy neuronów w mózgu naczelnych niebędących ludźmi za pomocą rekombinowanego immunotoksyny specyficznej dla mysiego CD25
Dlaczego to badanie mózgu ma znaczenie
Zrozumienie, jak konkretne grupy komórek mózgowych kontrolują ruch, emocje i zachowanie, jest kluczowe dla leczenia zaburzeń takich jak choroba Parkinsona czy autyzm. Mózg to jednak gęsty las splecionych komórek i większość narzędzi usuwa wiele „drzew” naraz. To badanie przedstawia sposób na usunięcie tylko wybranego typu neuronu w mózgu małpy, przy minimalnych uszkodzeniach towarzyszących, otwierając drzwi do znacznie bardziej precyzyjnych eksperymentów nad tym, jak konkretne obwody kształtują zachowanie i chorobę.
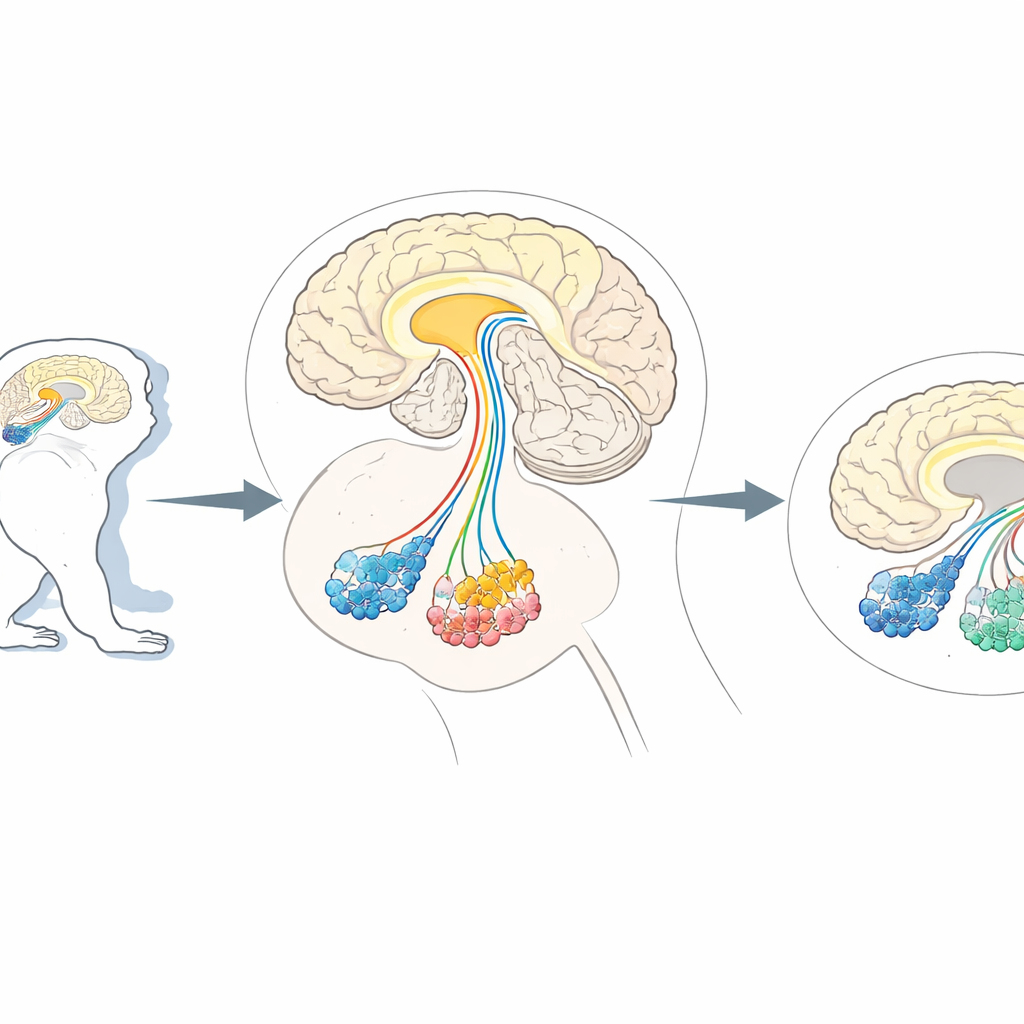
Potrzeba precyzyjnego „przycinania” komórek mózgowych
Naukowcy często zwracają się ku naczelnych niebędących ludźmi, takim jak marmozety i makaki, ponieważ ich mózgi są zorganizowane podobnie do naszych. Te zwierzęta stanowią nieocenione modele schorzeń dotyczących funkcji wyższych partii mózgu, od problemów ruchowych parkinsonowskich po zmiany w zachowaniach społecznych przypominające autyzm. Istniejące metody potrafią wyciszać lub pobudzać określone szlaki, ale rzeczywiste usunięcie jednego typu neuronu w tych złożonych mózgach bez uszkodzenia innych pozostawało trudne. Wcześniejsze prace na myszach wykorzystywały sztuczkę: wybrane neurony były zaprogramowane do ekspresji ludzkiego markera powierzchni komórkowej zwanego CD25, rozpoznawalnego przez zaprojektowaną toksynę zabijającą tylko oznaczone komórki. Jednak ten sam marker występuje naturalnie w komórkach układu odpornościowego naczelnych, a możliwie także w niektórych komórkach mózgu, co zwiększa ryzyko, że toksyna zaatakuje niewłaściwe cele u małp.
Projektowanie bezpieczniejszego molekularnego skalpela
Autorzy postanowili zbudować nowy molekularny skalpel dostosowany do użycia u naczelnych. Zamiast celować w ludzką wersję CD25, skupili się na wersji mysiej, która jest znacznie mniej podobna do naturalnego CD25 występującego u małp. Najpierw immunizowali królika białkiem mysiego CD25 i użyli metody opartej na chipie, aby wyłowić pojedyncze komórki królicze produkujące przeciwciała silnie wiążące mysie CD25, ale nie ludzką formę. Spośród nich zidentyfikowali wyróżniające się przeciwciało nazwane RMAb-52 o bardzo wysokim powinowactwie. Następnie połączyli kluczowe fragmenty tego przeciwciała z toksycznym fragmentem bakterii Pseudomonas, tworząc pojedyncze zrekombinowane białko „immunotoksynę” o nazwie anti-mCD25-PE38.
Testowanie narzędzia
W eksperymentach w probówce nowa immunotoksyna wiązała się z mysim CD25 znacznie mocniej niż z ludzkim CD25, potwierdzając jej selektywność. Po zastosowaniu do hodowanych komórek zaprojektowanych tak, by wyrażały mysie CD25, toksyna znacząco obniżyła ich przeżywalność przy bardzo niskich dawkach, podczas gdy komórki z ludzkim CD25 pozostały nienaruszone. Następnie zespół przeszedł do badań na żywych marmozetach. Przy użyciu specjalnego wektora wirusowego przemieszczającego się wstecznie wzdłuż włókien nerwowych dostarczyli gen mysiego CD25 do neuronów produkujących dopaminę, które wysyłają sygnały z głębokiego obszaru mózgu zwanego istotą czarną do prążkowia — szlaku kluczowego dla kontroli ruchu. Po upływie czasu potrzebnego na ekspresję markera w tych neuronach wstrzyknięto bezpośrednio do docelowego obszaru śródmózgowia białko anti-mCD25-PE38.
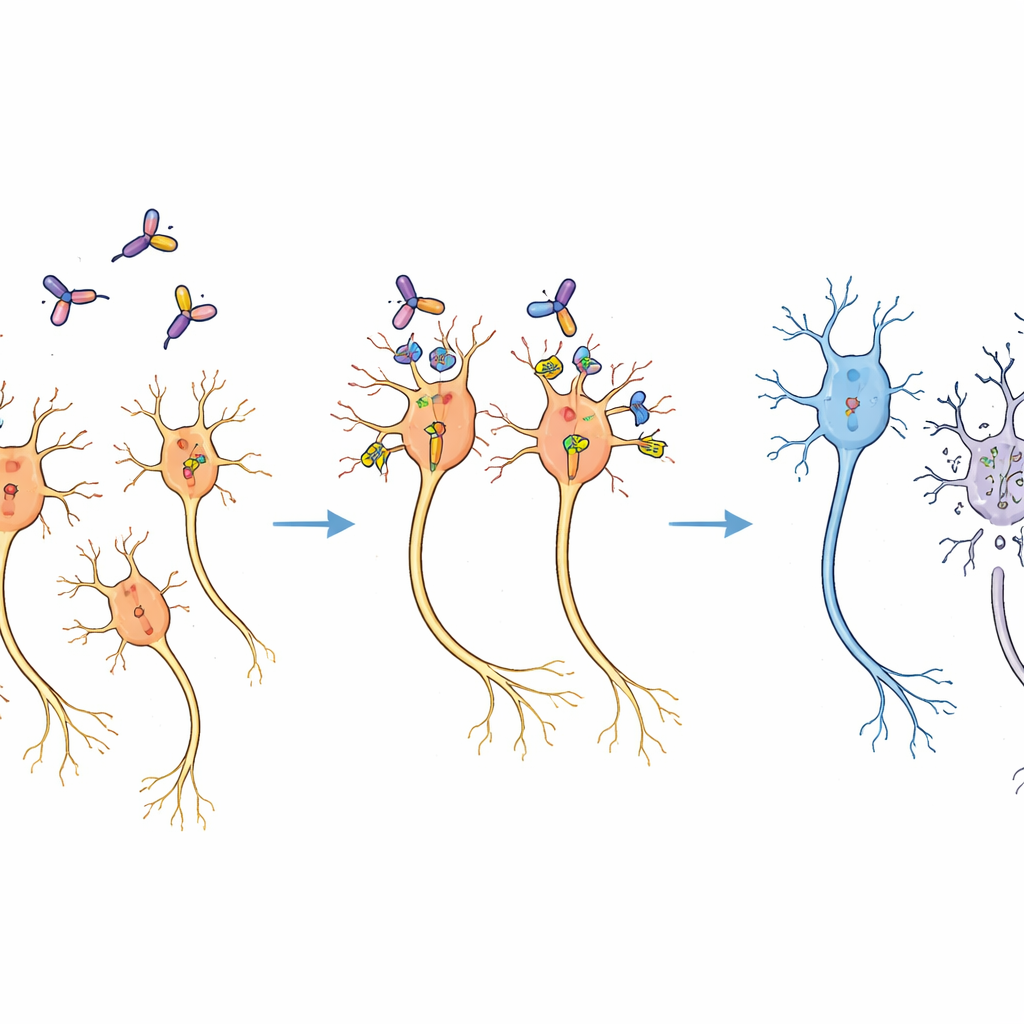
Selektywna utrata bez rozległych uszkodzeń
Dwa tygodnie po leczeniu sekcje mózgowe marmozet zdradziły jasny obraz. Po stronie, która otrzymała immunotoksynę, liczba neuronów dopaminergicznych zmniejszyła się do około dwóch trzecich w porównaniu z nieleczoną stroną, o czym świadczyło barwienie enzymu syntetyzującego dopaminę. Otaczająca tkanka mózgowa wyglądała jednak normalnie pod mikroskopem, a inne obszary mózgu, które również otrzymały wektor wirusowy, nie wykazały oczywistej utraty komórek. Eksperymenty pilotażowe wcześniej ustaliły zakres dawek unikających niespecyficznych uszkodzeń tkanek, a wybrana dawka mieściła się wyraźnie w tym bezpiecznym oknie. Wzorzec utraty odpowiadał oczekiwanemu rozprzestrzenieniu wirusa i toksyny, co wskazuje, że neurony zostały wyeliminowane specyficznie dlatego, że zostały zaprojektowane do ekspresji mysiego CD25, a nie z powodu nieselektywnego działania toksyny.
Co to oznacza dla przyszłych badań mózgu
Dla czytelnika niebędącego specjalistą kluczowy przekaz jest taki, że badacze zbudowali wysoce selektywny przycisk kasowania dla wybranych populacji neuronów w mózgach naczelnych. Łącząc retrogradowy system dostarczania wirusowego z immunotoksyną specyficzną dla mysiego antygenu, mogą usuwać określone szlaki — na przykład obwody dopaminergiczne zaangażowane w chorobę Parkinsona — jednocześnie oszczędzając sąsiednie komórki. Ta strategia unika niebezpiecznych reakcji krzyżowych z własnym CD25 zwierzęcia i powinna być szczególnie użyteczna, gdy naturalny receptor jest obecny lub podwyższony w przebiegu choroby. W dłuższej perspektywie podejście to pomoże naukowcom mapować, jak poszczególne trasy w okablowaniu mózgu przyczyniają się do ruchu, podejmowania decyzji i objawów psychiatrycznych, przybliżając nas do ukierunkowanych terapii, które korygują wadliwe obwody zamiast szeroko wpływać na cały mózg.
Cytowanie: Kobayashi, T., Kato, S., Kimura, S. et al. Targeting of specific neuronal types in the non-human primate brain by using a murine CD25-specific recombinant immunotoxin. Sci Rep 16, 8247 (2026). https://doi.org/10.1038/s41598-026-39662-6
Słowa kluczowe: neuronauka naczelnych niebędących ludźmi, celowanie immunotoksyną, neurony dopaminergiczne, obwody mózgowe marmozet, modele choroby Parkinsona