Clear Sky Science · pl
Białko wiążące RNA indukowane zimnem sprzyja aktywacji fibroblastów, a jego hamowanie stanowi potencjalny cel terapeutyczny w zwłóknieniu płuc
Dlaczego bliznowacenie płuc ma znaczenie
Zwłóknienie płuc to stan, w którym płuca stopniowo przemieniają się z miękkiej, elastycznej tkanki w sztywny, przypominający bliznę materiał. W miarę jak blizny się rozprzestrzeniają, oddychanie staje się utrudnione, spada poziom tlenu, a wielu pacjentów umiera w ciągu kilku lat od rozpoznania. Obecne leki mogą spowolnić uszkodzenie, ale rzadko zmieniają długoterminowe rokowanie. W tym badaniu zbadano białko reagujące na stres o nazwie CIRBP i postawiono proste pytanie o dużych implikacjach: czy to białko napędza bliznowacenie płuc, a jeśli tak, czy jego blokada może chronić płuca?
Sygnał stresu ukryty na widoku
CIRBP jest zwykle wytwarzane wewnątrz wielu typów komórek po ich wystawieniu na stres, taki jak zimno, niski poziom tlenu czy uszkodzenia toksyczne. W komórce pomaga stabilizować RNA, czyli komunikaty określające, które białka mają być syntetyzowane. CIRBP może jednak także wydostawać się lub być wydzielane poza komórkę, gdzie zachowuje się raczej jak sygnał alarmowy, wywołując stan zapalny. Wcześniejsze badania kliniczne wykazały, że osoby z idiopatycznym zwłóknieniem płuc mają więcej CIRBP w zwłókniałej tkance płucnej i we krwi, a wyższe poziomy korelowały z gorszymi wynikami. Nowe badanie postanowiło sprawdzić, czy CIRBP jest jedynie obserwatorem odzwierciedlającym stres tkanki, czy aktywnym uczestnikiem napędzającym postęp choroby.
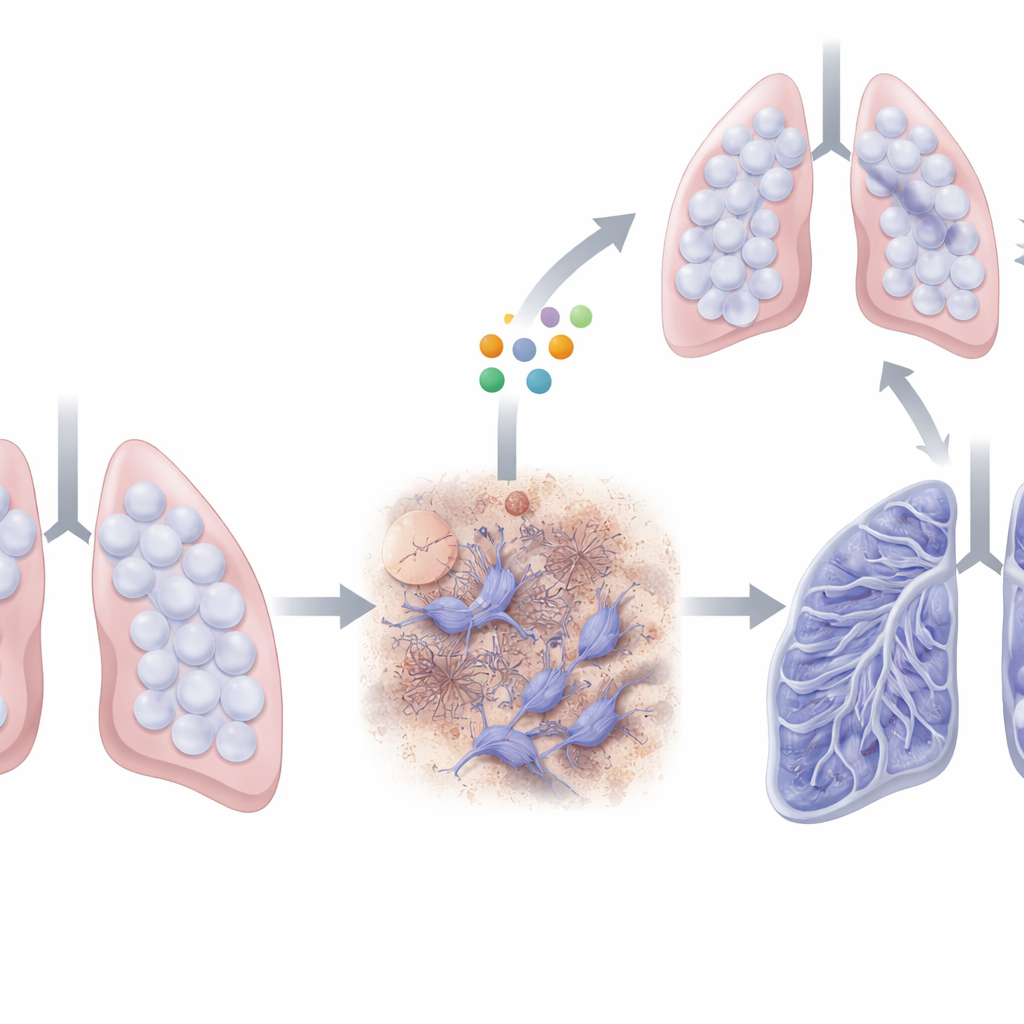
Testowanie roli CIRBP w chorych płucach
Naukowcy użyli standardowego modelu mysiego zwłóknienia płuc, w którym lek chemioterapeutyczny bleomycyna jest podawany bezpośrednio do dróg oddechowych, wywołując uszkodzenie i bliznowacenie w ciągu kilku tygodni. Porównali myszy normalne z osobnikami genetycznie zmodyfikowanymi tak, by nie wytwarzały CIRBP. Po ekspozycji na bleomycynę u normalnych myszy zaobserwowano wyraźny wzrost CIRBP, szczególnie w najbardziej zwłókniałych obszarach płuca. W przeciwieństwie do tego, myszy pozbawione CIRBP przeżywały dłużej, miały mniej widocznych blizn w preparatach tkankowych oraz niższe poziomy kolagenu i innych markerów włóknienia. Te wyniki sugerują, że CIRBP nie tylko występuje w tkance, ale aktywnie przyczynia się do gromadzenia się blizn.
W jaki sposób CIRBP pobudza fibroblasty
Aby przyjrzeć się mechanizmowi, zespół wyizolował pierwotne fibroblasty — komórki tkanki łącznej, które odkładają kolagen i odgrywają kluczową rolę w włóknieniu. Po dodaniu oczyszczonego CIRBP do hodowli komórek fibroblasty wydzielały więcej kolagenu, mnożyły się szybciej i poruszały się chętniej — zachowania sprzyjające rozrostowi tkanki bliznowatej. Co istotne, CIRBP nie zwiększał wyraźnie klasycznych markerów w pełni przekształconych „mięśniowopodobnych fibroblastów” wewnątrz komórek, co sugeruje, że głównie reguluje ich aktywność, a nie całkowicie zmienia tożsamość. Analizy ekspresji genów wykazały, że fibroblasty traktowane CIRBP zwiększały aktywność wielu genów związanych z odpornością i zapaleniem, a pomiary białkowe wskazały na jedną cząsteczkę szczególnie: cytokinę IL-6, której poziom gwałtownie wzrósł w odpowiedzi na CIRBP.
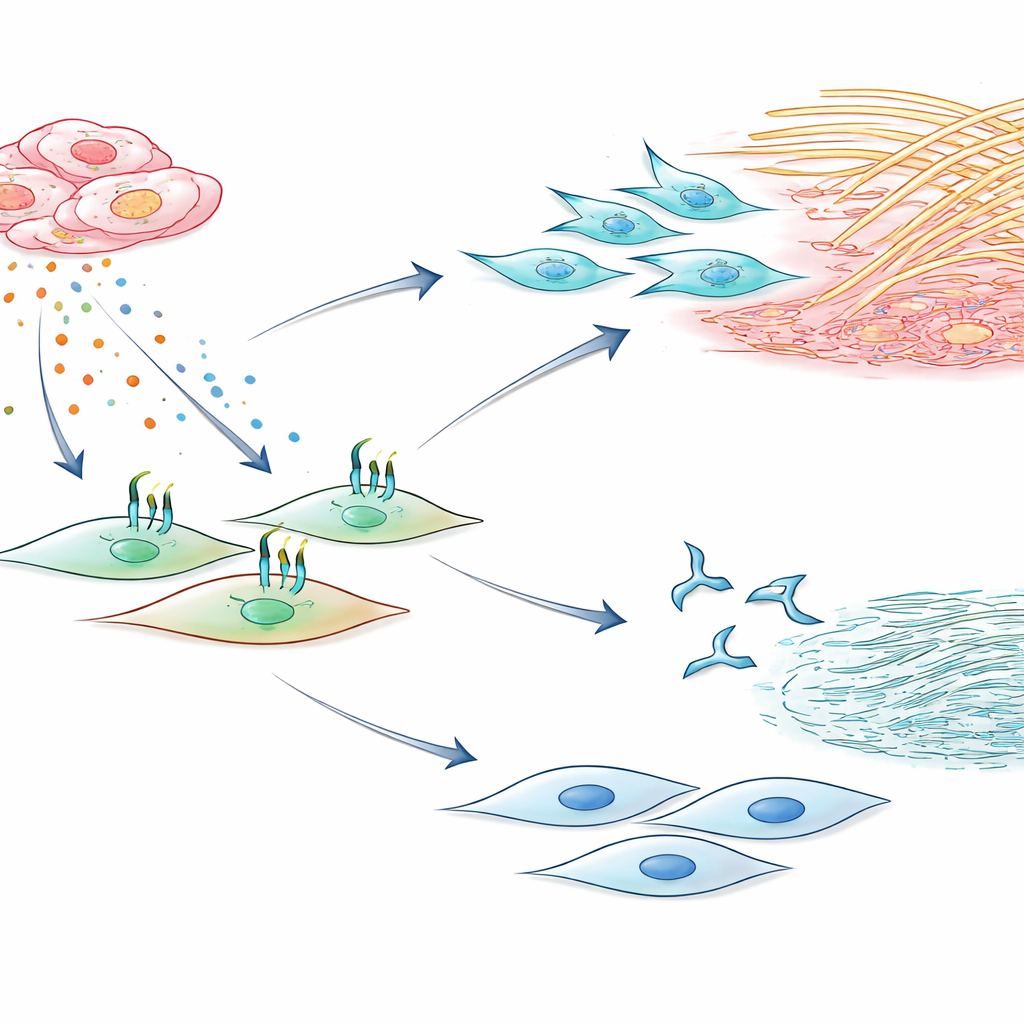
Łańcuch sygnalizacyjny, który można przerwać
Badanie odwzorowało następnie łańcuch sygnałowy łączący CIRBP z aktywacją fibroblastów. CIRBP poza komórką wydaje się angażować dwa receptory wrodzonego układu odpornościowego na fibroblastach, znane jako TLR2 i TLR4. Gdy receptory te wykrywały CIRBP, komórki wydzielały więcej IL-6, która z kolei działała z powrotem na te same fibroblasty w pętli autokrynnej, aby dalej zwiększać uwalnianie kolagenu i wzrost komórek. Zablokowanie IL-6 za pomocą przeciwciał neutralizujących ograniczyło wydzielanie kolagenu i proliferację, potwierdzając centralną rolę tej cytokiny w pętli. Podobnie leki hamujące TLR2 lub TLR4 osłabiły efekty CIRBP na IL-6, kolagen i podziały komórkowe. Najbardziej uderzającym rezultatem było działanie krótkiego peptydu nazwanego C23, pochodzącego z samego CIRBP i zaprojektowanego tak, by konkurować o wiązanie z tymi receptorami — silnie zmniejszał produkcję IL-6 i powiązane zachowania fibryczne w hodowanych fibroblastach.
Peptydowe leczenie łagodzące uszkodzenia
Wreszcie naukowcy sprawdzili, czy celowanie w CIRBP może pomóc zwierzętom z już istniejącym uszkodzeniem płuc. W modelu z bleomycyną rozpoczęli podawanie myszom wstrzyknięć C23 tydzień po początkowym urazie, w czasie gdy uszkodzenie już się rozwijało. W porównaniu z placebo myszy otrzymujące C23 przeżywały lepiej, miały łagodniejsze zmiany na histologii oraz niższe stężenie kolagenu w płucach i obniżone poziomy białek związanych z włóknieniem. Wyniki te wskazują, że blokowanie sygnalizacji CIRBP może istotnie osłabić postęp zwłóknienia płuc, nawet gdy leczenie rozpoczyna się po wystąpieniu urazu.
Co to oznacza dla przyszłych terapii płuc
Dla osób niezajmujących się specjalistycznie kluczowy przekaz jest taki: badanie identyfikuje CIRBP jako białko alarmowe indukowane stresem, które sprzyja bliznowaceniu płuc poprzez przełączenie fibroblastów w bardziej agresywny, wydzielający kolagen stan za pośrednictwem pętli sygnalizacyjnej TLR2/TLR4–IL-6. Przerwanie tego łańcucha, w szczególności za pomocą peptydu C23, złagodziło włóknienie i poprawiło przeżywalność u myszy. Choć przed zastosowaniem u pacjentów wciąż pozostaje wiele pracy, CIRBP wyróżnia się obecnie jako obiecujący cel wyższego rzędu: stłumienie jego sygnału mogłoby spowolnić lub zapobiec śmiertelnemu bliznowaceniu płuc przy jednoczesnym zachowaniu większości normalnych mechanizmów obronnych układu odpornościowego.
Cytowanie: Mochizuka, Y., Hozumi, H., Watanabe, H. et al. Cold inducible RNA binding protein promotes fibroblast activation and its inhibition represents a potential therapeutic target in pulmonary fibrosis. Sci Rep 16, 8324 (2026). https://doi.org/10.1038/s41598-026-39649-3
Słowa kluczowe: zwłóknienie płuc, fibroblasty, CIRBP, sygnalizacja IL-6, bliznowacenie płuc