Clear Sky Science · pl
czynnik indukowany niedotlenieniem 1α wykazuje podwójne role w progresji raka pęcherza poprzez regulację angiogenezy i inwazji zależną od TIMP3
Dlaczego guzy pozbawione tlenu mają znaczenie
Komórki nowotworowe często dzielą się tak szybko, że przewyższają własne zaopatrzenie w krew, pozostawiając części guza pozbawione tlenu. To środowisko o niskiej zawartości tlenu, czyli hipoksja, zmusza komórki do uruchomienia programów przetrwania, które mogą utrudniać leczenie nowotworów. W raku pęcherza — powszechnym guzie układu moczowego — naukowcy od dawna podejrzewali, że jeden z takich programów wyczuwających tlen, kontrolowany przez białko zwane HIF-1α, głównie sprzyja wzrostowi i szerzeniu się guza. W tym badaniu przyjrzano się temu bliżej i odkryto zaskakujący zwrot akcji: w pewnych warunkach obniżenie HIF-1α może faktycznie uczynić komórki raka pęcherza bardziej agresywnymi, a drugie białko, TIMP3, znajduje się w centrum tej paradoksalnej sytuacji.
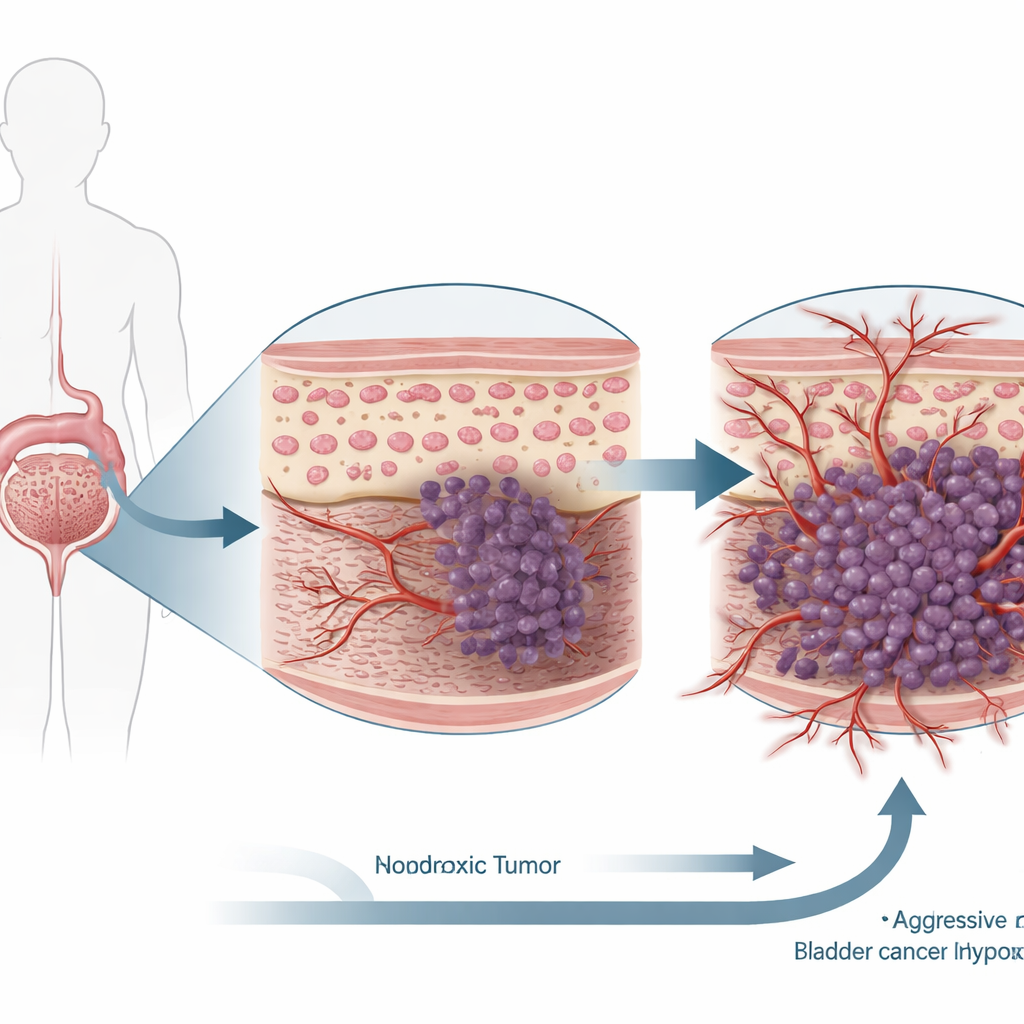
Bliższe spojrzenie na komórki raka pęcherza
Naukowcy pracowali na dwóch dobrze opisanych ludzkich liniach komórkowych raka pęcherza i poddali je działaniu albo normalnego poziomu tlenu, albo hipoksji, naśladując ubogie w tlen obszary w realnych guzach. Następnie wykorzystali narzędzia genetyczne do zmniejszenia poziomu HIF-1α w tych komórkach i zmierzyli, jak ta zmiana wpływała na podstawowe cechy nowotworu: tempo podziałów komórek, skłonność do umierania oraz zdolność do przemieszczania się, penetrowania przez barierę i pobudzania powstawania nowych naczyń. Równolegle przeanalizowali próbki guzów pęcherza od pacjentów, by porównać poziomy HIF-1α i TIMP3 w tkance nowotworowej w stosunku do pobliskiej tkanki prawidłowej pęcherza.
Zaskakujące odwrócenie ról w warunkach niskiego tlenu
Próbki od pacjentów potwierdziły, że HIF-1α jest rzeczywiście wyższy w guzach pęcherza niż w tkance prawidłowej, co jest zgodne z jego reputacją jako czynnika sprzyjającego nowotworowi. Jednak w eksperymentach komórkowych przeprowadzonych w warunkach hipoksji zmniejszenie HIF-1α wywołało efekt odwrotny do oczekiwanego. Gdy HIF-1α został wyciszony przy jednoczesnym niedoborze tlenu, komórki nowotworowe rosły szybciej w czasie, rzadziej przechodziły zaprogramowaną śmierć i stawały się lepsze w migracji oraz inwazji przez modele barier. Wydzielały także sygnały, które zachęcały komórki naczyń do tworzenia gęstszych, bardziej rozbudowanych sieci przypominających rury — cecha świadcząca o zwiększonym unaczynieniu guza. Krótko mówiąc, przy niższym poziomie HIF-1α w warunkach niedotlenienia komórki raka pęcherza zachowywały się bardziej złośliwie.
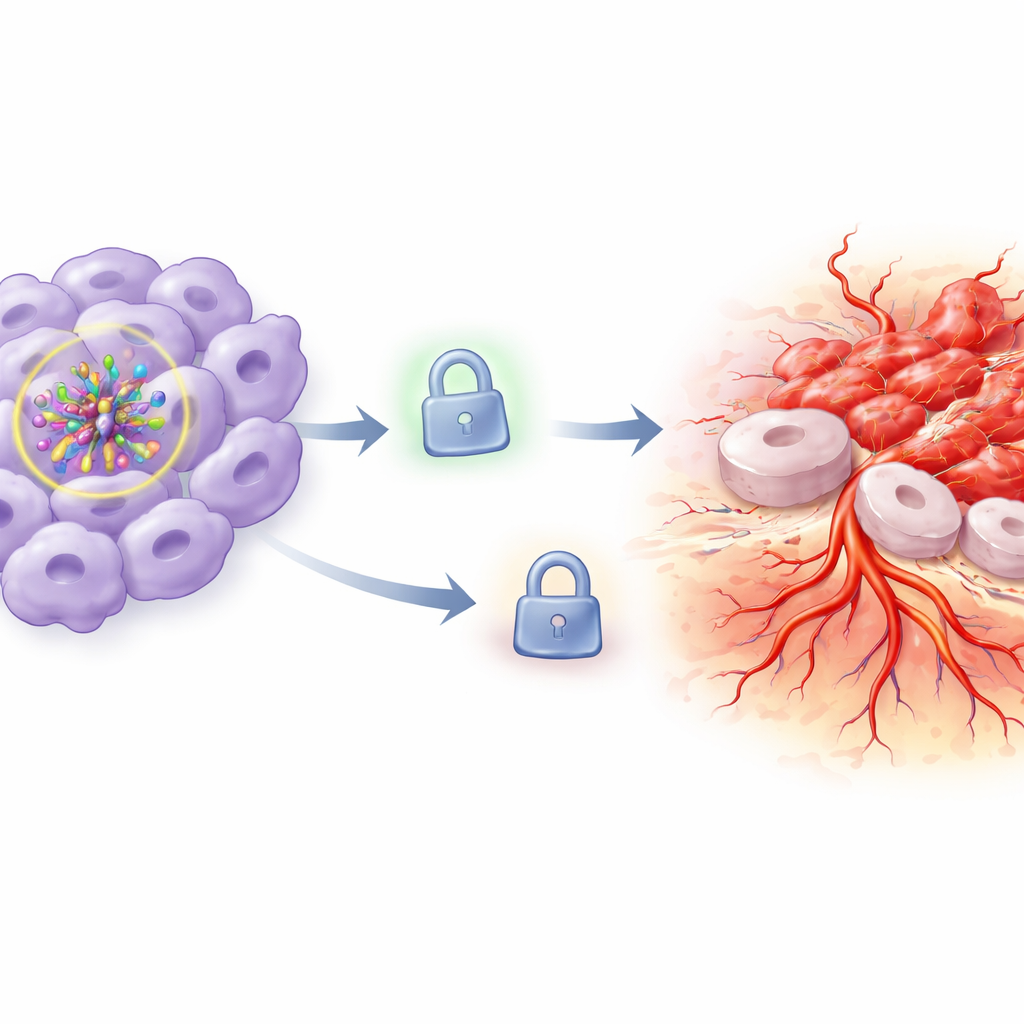
Brakujący hamulec rozprzestrzeniania guza
Aby zrozumieć, dlaczego tak się działo, zespół skupił się na TIMP3, białku, które zwykle działa jak hamulec rozkładu tkanki i powstawania nowych naczyń poprzez blokowanie enzymów rozkładających macierz zewnątrzkomórkową. W komórkach z obniżonym HIF-1α utrzymywanych w normalnym natlenieniu poziomy TIMP3 pozostały stosunkowo wysokie. Jednak gdy poziom tlenu spadł, białko TIMP3 gwałtownie zmalało. Utrata TIMP3 dobrze korelowała ze zaobserwowanym wzrostem inwazji i angiogenezy: przy osłabionym hamulcu komórki nowotworowe mogły łatwiej przebudowywać swoje otoczenie i się rozszerzać. Naukowcy następnie odwrócili sytuację, zmuszając komórki do produkcji dodatkowego TIMP3, podczas gdy HIF-1α pozostał wyciszony w warunkach hipoksji. Przywrócenie TIMP3 częściowo lub niemal całkowicie odwróciło agresywne zachowanie: komórki mniej się dzieliły, chętniej umierały, mniej się przemieszczały i inwazyjnie zachowywały, a także indukowały mniej i krótszych struktur naczyniopodobnych.
Co to oznacza dla przyszłych terapii
Wyniki sugerują, że HIF-1α ma podwójną osobowość w raku pęcherza. Z jednej strony jego całkowite poziomy są wyższe w guzach i pomaga uruchamiać znane programy sprzyjające nowotworowi. Z drugiej strony, w warunkach silnego niedotlenienia wydaje się on pomagać w utrzymaniu ochronnej obecności TIMP3. Usunięcie HIF-1α w tym kontekście może niezamierzenie obniżyć TIMP3 i uwolnić bardziej inwazyjne, promujące tworzenie naczyń zachowania. Dla terapii oznacza to, że proste blokowanie HIF-1α może się zemścić, chyba że lekarze jednocześnie znajdą sposoby na utrzymanie TIMP3 lub podobnych hamulców. Praca podkreśla znaczenie rozumienia nie tylko pojedynczych celów, lecz także szerszej sieci kontroli i równowagi, które kształtują odpowiedź guza na jego surowe, ubogie w tlen środowisko.
Cytowanie: Wang, X., Guo, J., Zhang, R. et al. Hypoxia-inducible factor 1α exerts dual roles in bladder cancer progression through TIMP3-mediated regulation of angiogenesis and invasion. Sci Rep 16, 8425 (2026). https://doi.org/10.1038/s41598-026-39635-9
Słowa kluczowe: rak pęcherza, niedotlenienie guza, HIF-1α, TIMP3, angiogeneza