Clear Sky Science · pl
Dokowanie molekularne i dynamika ujawniają nowe inhibitory CDK6 do ukierunkowanej terapii glejaka
Dlaczego to badanie nad rakiem mózgu jest istotne
Glejaka to jedna z najbardziej agresywnych postaci raka mózgu, a u wielu pacjentów obecne terapie nadal nie działają wystarczająco skutecznie ani długo. W tym badaniu autorzy proponują nowe podejście do zwalczania glejaka, skupiając się na pojedynczym nadaktywowanym przełączniku wewnątrz komórek nowotworowych — białku zwanym CDK6. Zamiast zwierząt laboratoryjnych czy próbówek, użyli zaawansowanych symulacji komputerowych, przesiawszy setki związków przypominających leki i identyfikując jeden szczególnie obiecujący kandydat, nazwany związek 21, który pewnego dnia mógłby pomóc spowolnić lub zatrzymać tę śmiertelną chorobę.
Śmiertelny guz, który unika obecnych terapii
Glejaka rośnie szybko, nacieka sąsiednie tkanki mózgu i niemal zawsze nawraca po zabiegu chirurgicznym, radioterapii i chemioterapii. Standardowe leki, takie jak temozolomid, mogą początkowo zmniejszyć guza, ale wiele komórek nowotworowych adaptuje się i staje się opornych, co prowadzi do nawrotu. Jednym z powodów jest to, że ich wewnętrzny mechanizm podziału komórek utknął w trybie „start”. Białka zwane kinazami zależnymi od cyklin (CDK) działają jak koła zębate wyznaczające czas, kiedy komórka ma kopiować DNA i się dzielić. W glejaku ścieżka CDK4/6 jest często nadaktywna, popychając komórki do mnożenia się mimo radioterapii i leków. To czyni CDK6 atrakcyjnym celem: jeśli naukowcy potrafią wyłączyć go selektywnie w komórkach nowotworowych, mogą spowolnić wzrost i zwiększyć skuteczność istniejących terapii.
Poszukiwanie lepszego inhibitora CDK6 na komputerze
Zamiast zaczynać w laboratorium, zespół przeprowadził szeroko zakrojone wirtualne poszukiwania. Rozpoczęli od znanej cząsteczki wiążącej CDK6 i poprosili program przesiewowy o znalezienie setek podobnych struktur w bazie związków leczniczych. Z 400 początkowych kandydatów 109 wybrano do szczegółowego dokowania z trójwymiarową strukturą ludzkiego CDK6. Dokowanie przypomina próbowanie wielu kluczy w zamku: oprogramowanie prognozuje, które cząsteczki najlepiej pasują do aktywnej kieszeni białka i jak silne może być ich wiązanie. Czterdzieści osiem kandydatów wypadało lepiej niż pierwotna referencyjna cząsteczka, ale jeden — związek 21 — wyróżnił się najsilniejszym przewidywanym wiązaniem i szczególnie korzystnymi kontaktami w miejscach CDK6 znanych z kontroli selektywności.
Sprawdzanie, czy „wirtualny lek” zachowuje się jak prawdziwy lek
Mocne wiązanie to tylko część historii; użyteczny lek musi także dotrzeć do mózgu, dobrze się rozpuszczać i nie szkodzić zdrowej tkance. Badacze użyli dodatkowych programów do oszacowania, jak każdy z najlepszych związków będzie się wchłaniał, krążył w organizmie i był usuwany. Związek 21 spełnił standardowe reguły „drug‑lijkeness”, wykazał dobrą przewidywaną rozpuszczalność i, co istotne w przypadku guzów mózgu, prognozowano, że przekroczy barierę krew–mózg przy zachowaniu rozsądnego profilu bezpieczeństwa. Oddzielne narzędzie toksykologiczne zasugerowało, że poza potencjalnymi problemami przy bardzo wysokich dawkach doustnych, związek 21 jest mniej prawdopodobny niż wiele innych, by powodować podrażnienia skóry czy oczu albo wywoływać ciężkie ostre uszkodzenia. Inny zestaw obliczeń zbadał rozmieszczenie elektronów w cząsteczce, dając wskazówki co do jej stabilności chemicznej i skłonności do niepożądanych reakcji; te testy również faworyzowały związek 21 nad referencyjnym lekiem.
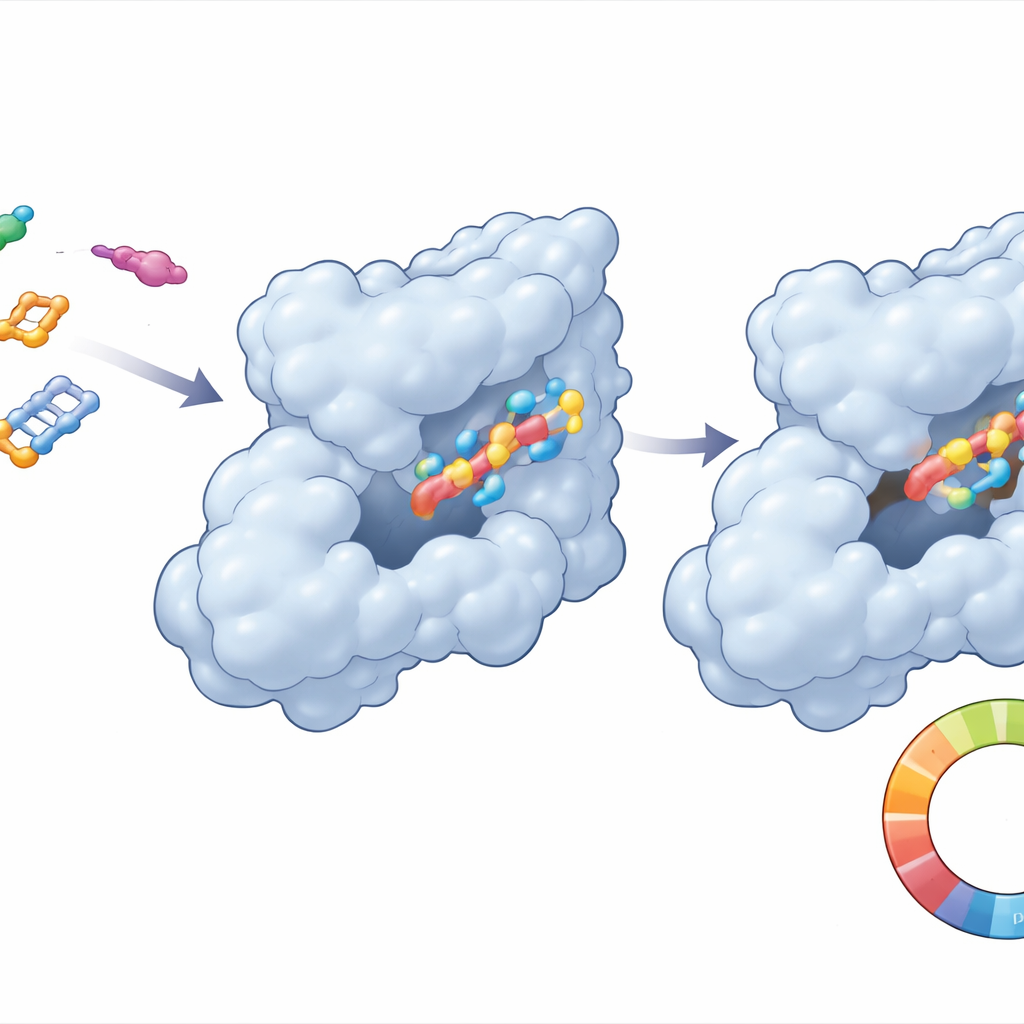
Obserwacja, jak lek i jego cel poruszają się razem
Ponieważ białka i cząsteczki leków nie są sztywne, zespół przeprowadził długie komputerowe „filmy” trwające 250 miliardowych części sekundy, aby zobaczyć, jak CDK6 i każdy związek zachowują się w wodnym, przypominającym organizm środowisku. W przypadku związku 21 kompleks szybko ustabilizował się w stałym układzie i poruszał się jedynie w niewielkim stopniu, co jest dobrym znakiem, że cząsteczka pozostanie osadzona w kieszeni CDK6. Kluczowe punkty kontaktowe między lekiem a białkiem utrzymywały się, podczas gdy ogólna struktura CDK6 pozostawała zwarta. W przeciwieństwie do tego, związek referencyjny wykazywał większe fluktuacje i słabsze, mniej spójne kontakty. Dodatkowe obliczenia energetyczne wspierały te wnioski, sugerując, że CDK6 preferuje wiązać związek 21 silniej, głównie dzięki dopasowanym hydrofobowym (oleistym) interakcjom oraz dobrze ustawionym wiązaniom wodorowym.
Co to może oznaczać dla przyszłej opieki nad pacjentami z rakiem mózgu
Podsumowując, testy komputerowe dają mocne przesłanki, że związek 21 jest wysokiej jakości punktem wyjścia do nowego leku na glejaka ukierunkowanego na CDK6. Wydaje się bardziej selektywny, stabilniejszy i lepiej przystosowany do dotarcia do mózgu niż cząsteczka referencyjna, przy jednoczesnym unikaniu wielu typowych pułapek toksykologicznych. Jednak praca pozostaje na etapie predykcyjnym: w tym badaniu nie testowano komórek ani zwierząt. Kolejne kroki to synteza związku 21, sprawdzenie, czy rzeczywiście hamuje wzrost komórek glejakowych w laboratorium, oraz ocena zachowania w modelach zwierzęcych. Jeśli te badania potwierdzą symulacje, ta cząsteczka — lub jej ulepszone wersje — mogłyby w przyszłości przyczynić się do bardziej precyzyjnych, ukierunkowanych terapii, które dadzą pacjentom z glejakiem lepsze perspektywy i dłuższe panowanie nad chorobą.
Cytowanie: Khan, M.U., Munir, M., Manzoor, H. et al. Molecular docking and dynamics reveal novel CDK6 inhibitors for targeted glioblastoma therapy. Sci Rep 16, 9000 (2026). https://doi.org/10.1038/s41598-026-39629-7
Słowa kluczowe: glejak, inhibitory CDK6, terapia ukierunkowana, wirtualne przesiewanie leków, rak mózgu