Clear Sky Science · pl
Charakterystyka genomowa i in vitro dwóch litycznych bakteriofagów infekujących wielooporny szczep Erwinia sp. AnSW2-5
Dlaczego bakterie niszczące uprawy dotyczą nas wszystkich
Na całym świecie rolnicy walczą z chorobami bakteryjnymi, które gnicie owoców, marszczeniem liści i dewastacją plonów. Wiele z tych epidemii wywoływanych jest teraz przez szczepy, które nie reagują już na powszechnie stosowane antybiotyki, zagrażając zarówno zasobom żywnościowym, jak i środkom utrzymania zależnym od rolnictwa. W tym badaniu zbadano obiecującą alternatywę: użycie wirusów atakujących bakterie, zwanych bakteriofagami, do bezpiecznego unieszkodliwienia szczególnie uciążliwego patogenu roślinnego znalezionego w glebie powiązanej z intensywnym stosowaniem antybiotyków.
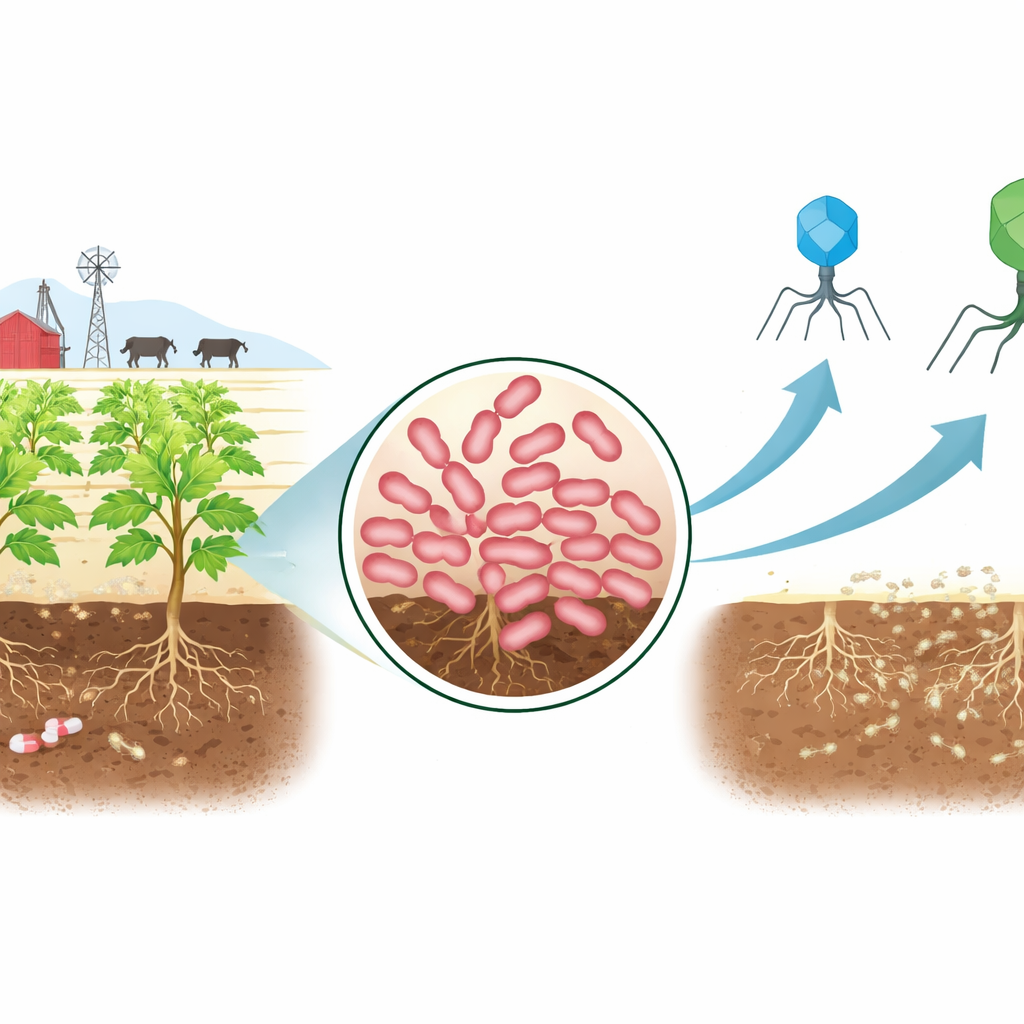
Nowy trudny intruz na gospodarstwie
Naukowcy rozpoczęli od pobrania próbek gleby z zagrody dla bydła, znanej z przyjmowania odpadów zwierzęcych i antybiotyków. Z tego wymagającego środowiska wyizolowali szczep Erwinia — grupę bakterii, która obejmuje znanych sprawców takich chorób jak parch jabłoni czy zgnilizna miękka ziemniaków. Testy wykazały, że szczep ten, nazwany AnSW2-5, był odporny na wiele głównych grup antybiotyków, w tym leków stosowanych przeciw szerokiemu spektrum infekcji. Analiza genetyczna potwierdziła przyczynę: jego DNA zawierało kilka znanych genów oporności oraz wydajne pompy molekularne usuwające antybiotyki z komórki. Jednocześnie porównania genomowe ujawniły, że szczep różni się od wcześniej opisanych gatunków Erwinia, co czyni go przydatnym modelem do badania metod kontroli nowych, trudnych do leczenia patogenów roślinnych.
Dwaj mali drapieżcy o różnych mocnych stronach
Aby znaleźć naturalnych wrogów tego wieloopornego szczepu, zespół sięgnął po wodę słodką z tego samego miejsca i wzbogacił ją w celu wyizolowania bakteriofagów zdolnych infekować AnSW2-5. Wyizolowali dwóch obiecujących kandydatów, oznaczonych jako P-A i P-K. W mikroskopie elektronowym P-A wyglądał kompaktowo z krótkim ogonem — układ związany z szybkim, bezpośrednim zakażeniem. P-K przeciwnie — miał dłuższy, kontraktylny ogon z złożoną strukturą podstawy, co sugeruje silniejszy mechanizm wwiercania się w gospodarza. Sekwencjonowanie genomów wykazało, że oba fagi są ścisle lityczne: wtargają, replikują się i powodują lizę komórki zamiast utajania się w DNA bakterii. Robią to jednak za pomocą bardzo różnych narzędzi genetycznych — zredukowany genom P-A sprzyja szybkiemu atakowi, podczas gdy większy genom P-K koduje bardziej rozbudowane elementy strukturalne i mechanizmy replikacyjne.
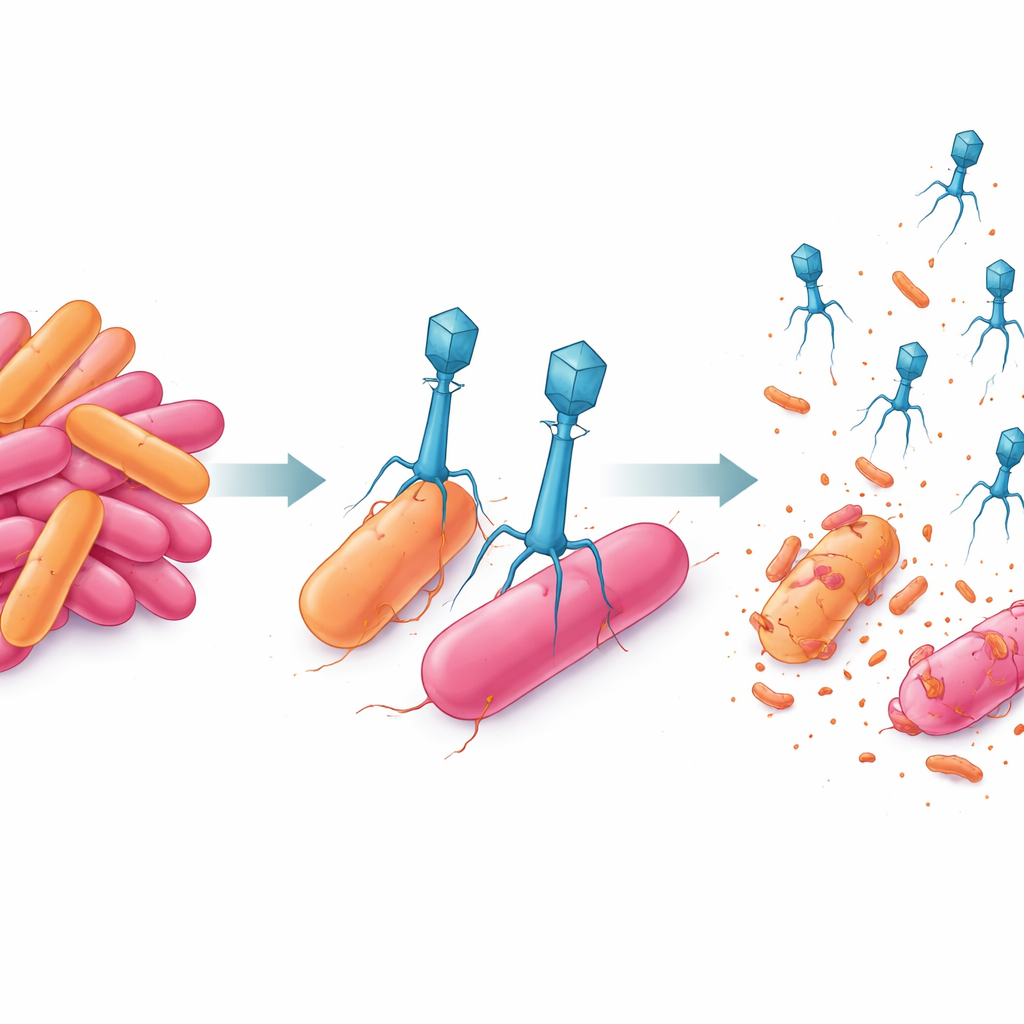
Jak wirusowy duet atakuje
Gdy naukowcy śledzili cykle życiowe każdego faga w warunkach laboratoryjnych, odkryli, że P-A uderza szybko: potrzeba mu tylko około 20 minut, zanim pojawią się nowe cząstki wirusa, a każda zainfekowana komórka uwalnia około 70 potomków. P-K potrzebuje więcej czasu — około 35 minut zanim zacznie produkować nowe fagowe cząstki — ale każda zainfekowana komórka daje w przybliżeniu 110 nowych cząstek. W testach ko-kultury, gdzie bakterie i fag rosną razem przez trzy dni, oba fagi oddzielnie spowalniały wzrost bakterii, ale nie zapobiegały mu całkowicie. Bakterie ostatecznie odradzały się, co odzwierciedla pojawienie się opornych przeżywców. Jednak gdy P-A i P-K zastosowano razem w jednym koktajlu, zmniejszyły populację bakterii o ponad 80% i utrzymały jej zahamowanie przez cały 72-godzinny eksperyment.
Powstrzymywanie narastania oporności
Jednym z najbardziej uderzających wyników było to, jak para fagów wpłynęła na pojawianie się mutantów odpornych. Pod wpływem samego P-A lub P-K niewielka frakcja bakterii — rzędu jednej na milion do jednej na dziesięć milionów — zdołała umknąć i rosnąć pomimo ataku faga. Jednak gdy użyto obu fagów jednocześnie, kolonie odpornych stały się tak rzadkie, że znalazły się poniżej progu wykrywalności eksperymentu. Sugeruje to, że dwa wirusy prawdopodobnie wiążą się z różnymi celami na powierzchni bakterii lub uszkadzają komórkę w sposób komplementarny. Aby pojedyncza bakteria przetrwała, musiałaby przezwyciężyć oba mechanizmy naraz — zdarzenie praktycznie niemożliwe. W praktycznym ujęciu czyni to koktajl znacznie bardziej odpornym na ewolucyjne sztuczki, które często skazują antybiotyki na niepowodzenie.
Co to może znaczyć dla przyszłych plonów
Podsumowując, praca pokazuje, że starannie dobrane pary bakteriofagów mogą zrobić więcej niż tylko obniżyć liczebność niebezpiecznych bakterii roślinnych — mogą także ograniczyć zdolność bakterii do rozwijania oporności. Łącząc szybko działającego faga z takim, który produkuje większą liczbę potomstwa, badacze stworzyli wirusowy duet, który utrzymywał wielooporny szczep Erwinia pod kontrolą przez dni, jednocześnie zapobiegając wykrywalnym wariantom ucieczki. Chociaż te próby przeprowadzono w laboratorium, a nie w sadach czy na polach, wskazują one na przyszłość, w której celowane mieszanki fagów staną się częścią standardowego zintegrowanego zarządzania szkodnikami, pomagając rolnikom chronić uprawy przy znacznie mniejszym poleganiu na tradycyjnych antybiotykach.
Cytowanie: Baek, K., Goh, J. & Choi, A. Genomic and in vitro characterization of two lytic bacteriophages infecting multidrug-resistant Erwinia sp. strain AnSW2-5. Sci Rep 16, 8172 (2026). https://doi.org/10.1038/s41598-026-39563-8
Słowa kluczowe: bakteriofag kontrola biologiczna, choroby bakteryjne roślin, oporność na antybiotyki w rolnictwie, terapia fagowa Erwinia, koktajle fagowe