Clear Sky Science · pl
Nowe sprzężenia benzimidazol‑alkanosulfonianowe jako inhibitory cholinesteraz z walidacją in vitro i in silico
Dlaczego te badania są ważne dla pamięci i starzenia się
Choroba Alzheimera stopniowo niszczy pamięć, samodzielność i jakość życia milionów ludzi na całym świecie, podczas gdy dostępne leki głównie łagodzą objawy, nie zatrzymując podstawowego procesu uszkodzenia. Niniejsze badanie bada nową rodzinę molekuł syntetycznych zaprojektowanych tak, by lepiej chronić kluczowy neuroprzekaźnik zaangażowany w uczenie się i pamięć, a jednocześnie przeciwdziałać szkodliwemu stresowi oksydacyjnemu. Łącząc cechy kilku skutecznych klas leków w jednej strukturze, autorzy dążą do przybliżenia istotnego kroku w kierunku skuteczniejszych terapii choroby Alzheimera.
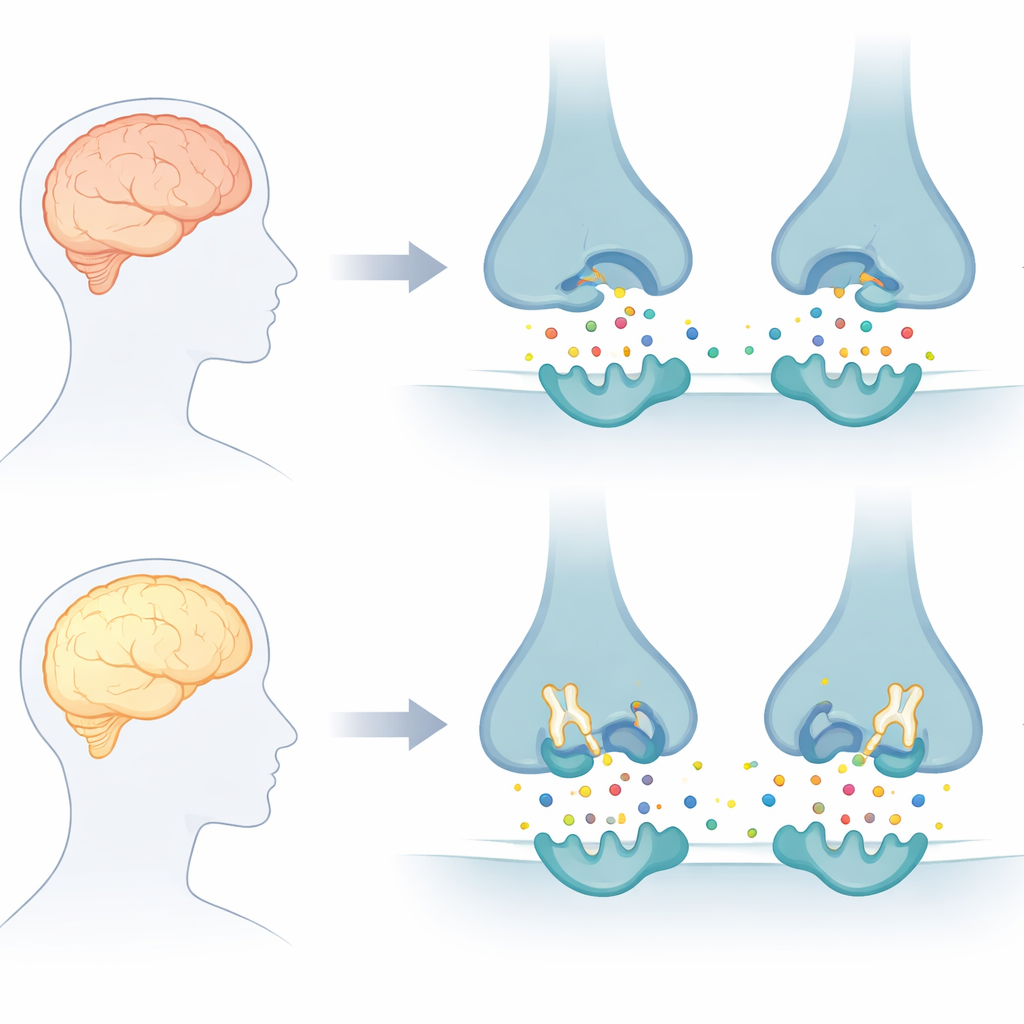
Sygnał mózgowy, który zanika za szybko
Zdrowe komórki mózgowe komunikują się za pomocą przekaźników chemicznych, z których jednym z najważniejszych jest acetylocholina. W chorobie Alzheimera acetylocholina jest rozkładana zbyt szybko przez dwie enzymy, acetylocholinoesterazę i butyrylocholinesterazę, co przyczynia się do utraty pamięci i dezorientacji. Obecne leki głównie blokują tylko jeden z tych enzymów i tylko przez pewien czas, dlatego dają krótkotrwałą ulgę objawową zamiast długotrwałej ochrony. Autorzy tego artykułu skupili się na projektowaniu „podwójnych” blokerów, które mogłyby jednocześnie ukierunkować oba enzymy i potencjalnie dać acetylocholinie większą szansę na wykonanie swojej funkcji.
Tworzenie mądrzejszego klucza molekularnego
Aby opracować te podwójne inhibitory, zespół zastosował strategię nazwaną hybrydyzacją molekularną: zespolili fragmenty pochodzące z trzech typów elementów chemicznych, które już wykazują dobrą interakcję z enzymami cholinesterazowymi. Te fragmenty obejmowały pierścień benzimidazolowy często spotykany w lekach, grupę sulfonianową zdolną silnie wiązać się z kieszeniami enzymatycznymi oraz łącznik hydrazonowy, który pomaga elastycznie połączyć części. W wyniku powstała seria powiązanych związków oznaczonych jako 4a–4r, których struktury potwierdzono standardowymi technikami chemicznymi, takimi jak spektroskopia w podczerwieni i rezonans magnetyczny jądrowy.
Badanie blokowania enzymów i mocy przeciwutleniającej
Nowe związki najpierw poddano przesiewowym testom in vitro, aby sprawdzić, jak skutecznie mogą spowalniać działanie obu cholinesteraz. Większość członków serii wykazała umiarkowane do silnych efekty hamujące, ale szczególnie pięć z nich — oznaczonych jako 4b, 4h, 4i, 4q i 4r — wyróżniło się zdolnością do inhibicji acetylocholinoesterazy. Przy pomiarach dokładniejszych wartości mocy działania kilka z tych molekuł dorównywało, a nawet przewyższało donepezil, jeden z głównych leków stosowanych obecnie w chorobie Alzheimera. Zespół zbadał też, czy najlepsze inhibitory enzymatyczne mogą neutralizować wolne rodniki, niestabilne cząsteczki uszkadzające komórki mózgowe. Związki 4q i 4r wykazały szczególnie silną aktywność przeciwutleniającą w kilku różnych testach, zbliżając się do wydajności referencyjnej witaminy C lub ją przewyższając.
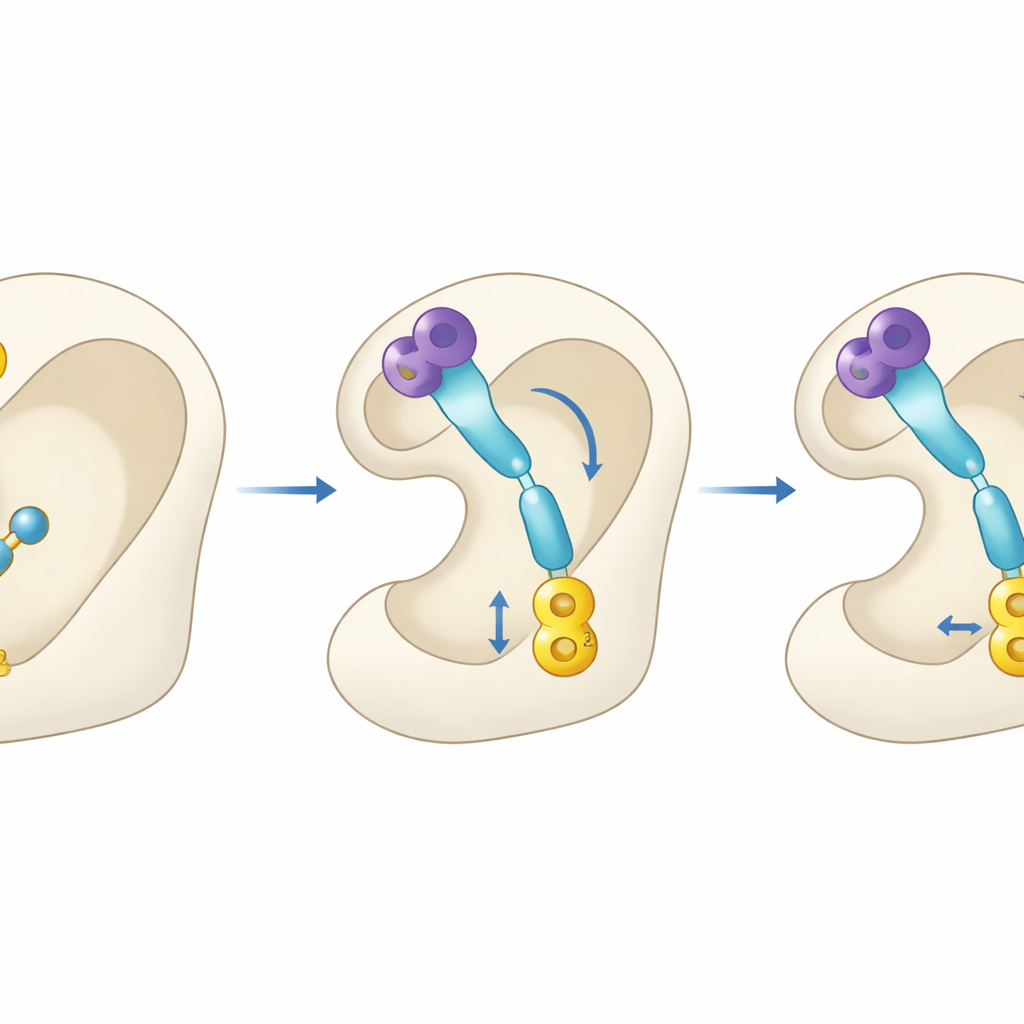
Zajrzeć do zamka enzymu
Ponieważ eksperymenty prowadzono poza organizmem, naukowcy sięgnęli po modelowanie komputerowe, by przewidzieć, jak molekuły mogą zachowywać się jako leki. Korzystając z powszechnie stosowanych narzędzi in silico, oszacowali właściwości związane z wchłanianiem, dystrybucją i metabolizmem, a następnie symulowali dopasowanie związków do trójwymiarowej struktury acetylocholinoesterazy. Badania dokowania sugerowały, że fragment benzimidazolowy każdej molekuły osadza się blisko zewnętrznego otworu enzymu, podczas gdy koniec z grupą sulfonianową sięga głęboko do centrum katalitycznego, gdzie zwykle następuje rozkład acetylocholiny. Warto zauważyć, że 4q i 4r utworzyły kilka stabilizujących interakcji w kieszeni enzymatycznej i wykazały wyższą obliczoną siłę wiązania niż sam donepezil, co odzwierciedla ich silne wyniki w testach in vitro.
Co to oznacza dla przyszłych terapii Alzheimera
Podsumowując, wyniki pokazują, że ta nowa klasa sprzężeń benzimidazol‑alkanosulfonianowych może silnie hamować acetylocholinoesterazę, wykazywać użyteczne właściwości przeciwutleniające i wiązać się z celem enzymatycznym w sposób zgodny z aktualnymi zasadami projektowania leków. Choć te molekuły są dalekie od zastosowania u pacjentów — nie przeszły jeszcze badań na zwierzętach ani u ludzi — stanowią obiecujący wzorzec dla leków następnej generacji łączących inhibicję enzymatyczną z ochroną przed stresem oksydacyjnym. Przy dalszym dopracowaniu i testach biologicznych niektóre spośród tych związków mogłyby w przyszłości przyczynić się do opracowania leków lepiej zachowujących pamięć i funkcje poznawcze w starzejącym się mózgu.
Cytowanie: Omar, M.A., Al-Ashmawy, A.A.K., Abd El Salam, H.A. et al. New benzimidazole-alkanesulfonate conjugates as cholinesterase inhibitors with in vitro and in silico validation. Sci Rep 16, 8946 (2026). https://doi.org/10.1038/s41598-026-39534-z
Słowa kluczowe: choroba Alzheimera, inhibitory acetylocholinoesterazy, pochodne benzimidazolu, związki przeciwutleniające, projektowanie leków