Clear Sky Science · pl
Modelowanie strukturalne i analizy dokowania kanonicznych i nowych zmian sensu w Escherichia coli z Sudanu związanych z opornością
Dlaczego to ma znaczenie dla zdrowia codziennego
Zakażenia odporne na antybiotyki nie są już rzadkimi medycznymi ciekawostkami; coraz częściej zagrażają rutynowym zabiegom przy zakażeniach dróg moczowych, chirurgii i intensywnej terapii. W tym badaniu szczegółowo przyjrzano się bakteriom Escherichia coli z Sudanu i postawiono konkretne pytanie: jak drobne zmiany genetyczne w białkach bakteryjnych zmieniają sposób działania powszechnych antybiotyków? Dzięki zastosowaniu komputerowego modelowania strukturalnego zamiast kosztownych eksperymentów laboratoryjnych autorzy ujawniają ukryte wzory oporności, które standardowe testy i globalne bazy danych mogą przeoczać — szczególnie w środowiskach o ograniczonych zasobach, gdzie oporność rośnie najszybciej. 
Wgląd do arsenału bakterii
Naukowcy skoncentrowali się na mutacjach typu „missense” — pojedynczych zmianach nukleotydowych, które zamieniają jeden aminokwas w białku na inny. Przeanalizowali sekwencje całych genomów 55 izolatów E. coli zebranych w Sudanie i skupili się na białkach będących bezpośrednimi celami głównych klas antybiotyków, w tym fluorochinolonów, makrolidów i rifampicyny. Do celów należą enzymy skręcające DNA (gyraza i topoizomeraza IV), rybosom odpowiedzialny za syntezę białek oraz polimeraza RNA. Spośród 71 wykrytych mutacji w tych białkach, 19 zostało wskazanych przez wiele narzędzi predykcyjnych jako prawdopodobnie szkodliwe dla funkcji białka, a co istotne — większość z nich wydawała się być nowymi wariantami, które nie zostały jeszcze skatalogowane w globalnych bazach oporności.
Nowe punkty zapalne w znanych celach
Niektóre z ważniejszych zmian skupiały się w białku rybosomalnym L22, które pomaga tworzyć tunel, przez który wychodzą nowo syntetyzowane białka. Ten region jest też miejscem wiązania makrolidów, takich jak erytromycyna. Badanie zidentyfikowało gęsty zestaw wcześniej nieopisanych mutacji L22, wiele w obrębie jednego szczepu, które leżą wzdłuż tego tunelu i w punktach kontaktu z rybosomalnym RNA. Analizy komputerowe sugerują, że kilka z tych zmian destabilizuje lokalną strukturę lub zwiększa jej elastyczność, co może przeprojektować tunel tak, że cząsteczki makrolidów przylegają mniej ciasno. Równocześnie w białkach przetwarzających DNA — ParC i ParE — oraz w polimerazie RNA pojawiły się bardziej znane „kanoniczne” mutacje oporności, potwierdzając, że szczepy z Sudanu mają pewne globalne znamiona oporności, ale również niosą własne lokalne warianty.
W jaki sposób zmiany kształtu osłabiają przyczepność antybiotyku
Zespół poszedł dalej niż tylko lista sekwencji i zapytał, jak te mutacje mogą zmieniać trójwymiarowe dopasowanie antybiotyków do ich celów. Przy użyciu symulacji dokowania molekularnego porównano wiązanie różnych leków z normalnymi i zmutowanymi białkami. Dla topoizomerazy IV ParC kluczowe mutacje w pobliżu miejsca kontaktu z lekiem znacząco osłabiły przewidywane wiązanie fluorochinolonu trovafloksacyny, co odzwierciedla luźniejsze przyleganie na styku enzym–DNA–lek. W spokrewnionym białku ParE mutacje nieznacznie zmniejszyły wiązanie novobiocyny. W przeciwieństwie do tego, nowa mutacja w gyrazie GyrA wydawała się destabilizować strukturę enzymu bez zauważalnej zmiany siły wiązania fluorochinolonu moxifloksacyny, co sugeruje, że oporność czasami może wyłaniać się przez subtelne zaburzenie funkcji enzymu, a nie tylko przez bezpośrednie wypieranie leku. 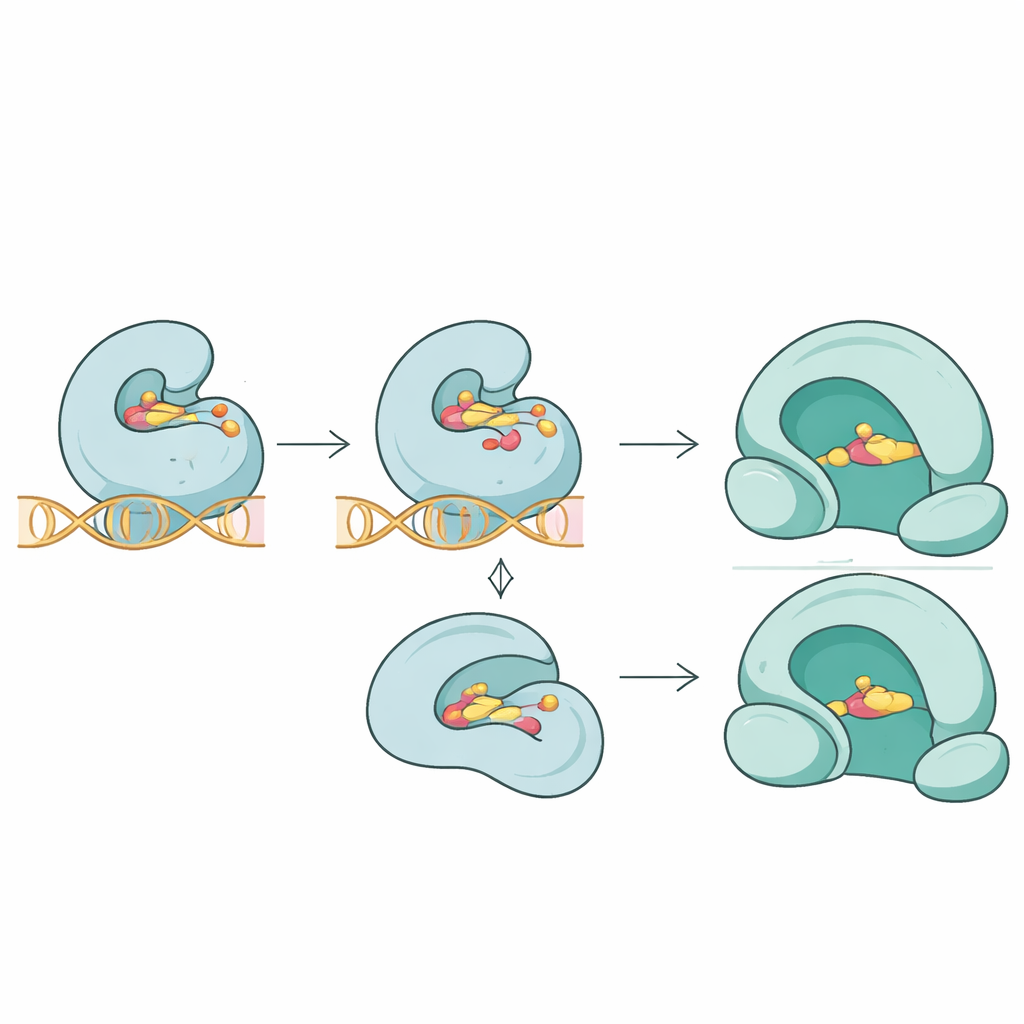
Mieszane skutki dla różnych leków
Nie wszystkie mutacje miały ten sam wpływ. Klasyczne zmiany związane z opornością na rifampicynę w białku polimerazy RNA RpoB niewiele zakłócały wiązanie nowszego, strukturalnie odrębnego inhibitora atakującego sąsiednie miejsce, co sugeruje, że przyszłe leki można projektować tak, by omijały istniejące wzorce oporności. W przypadku białka rybosomalnego L22 badania dokowania z erytromycyną pokazały mozaikę wyników: niektóre mutacje osłabiły wiązanie, inne miały mały wpływ, a jedna nawet nieznacznie poprawiła przewidywane dopasowanie. Wyniki te podkreślają, że oporność rzadko jest zero-jedynkowa; każda mutacja przesuwa stabilność białka, jego elastyczność i wiązanie leku w różnych kierunkach, a ostateczny efekt terapeutyczny zależy od tego, jak te zmiany sumują się w żywym komórkowym kontekście bakterii.
Co to znaczy dla pacjentów i nadzoru
Z perspektywy laika kluczowy przekaz jest taki, że bakterie w miejscach takich jak Sudan ewoluują oporność zarówno znanymi, jak i mniej znanymi ścieżkami. Znane ścieżki obejmują klasyczne mutacje śledzone przez programy międzynarodowe, ale to badanie pokazuje, że wiele dodatkowych, lokalnie wzbogaconych mutacji może również osłabiać antybiotyki w bardziej subtelny sposób. Mapując te zmiany na szczegółowych strukturach białek, autorzy przedstawiają krótką listę mutacji, które powinny być przetestowane w laboratorium i uwzględnione w regionalnych panelach diagnostycznych. W praktycznym wymiarze ich praca wskazuje, że inteligentne modelowanie komputerowe może pomóc krajom o ograniczonych możliwościach laboratoryjnych lepiej monitorować pojawiającą się oporność, ostatecznie wspierając bardziej wiarygodne wybory terapeutyczne i inspirując projektowanie leków, które wyprzedzą ewolucję bakterii.
Cytowanie: Sage, E.E., Ibrahim, S.A.E., Firdaus-Raih, M. et al. Structural modeling and docking analysis of canonical and novel resistance-associated missense mutations in Sudanese Escherichia coli. Sci Rep 16, 8995 (2026). https://doi.org/10.1038/s41598-026-39491-7
Słowa kluczowe: oporność na antybiotyki, Escherichia coli, mutacje sensu, bioinformatyka strukturalna, Sudan