Clear Sky Science · pl
Integracja uczenia głębokiego z modelowaniem opartym na fizyce umożliwia przewidywanie interfejsu przeciwciało-antygen z wysoką precyzją
Dlaczego to ma znaczenie dla przyszłych leków
Przeciwciała są kierowanymi pociskami naszego układu odpornościowego i podstawą wielu nowoczesnych leków. Aby projektować lepsze przeciwciała, naukowcy muszą dokładnie wiedzieć, jak przeciwciało chwyta swoją cząsteczkę docelową, czyli antygen. Eksperymentalne określanie tych struktur jest powolne i kosztowne. Badanie to pokazuje, że połączenie uczenia głębokiego z klasycznym modelowaniem w stylu fizycznym może znacząco poprawić komputerowe przewidywania miejsca styku przeciwciała i antygenu, co potencjalnie przyspieszy projektowanie i przesiewanie przeciwciał.
Znajdowanie strefy uścisku dłoni
Przeciwciała rozpoznają swoje cele za pomocą małych, elastycznych pętli na końcach, zwanych regionami wiążącymi, które łączą się, tworząc płat kontaktowy. Te pętle mogą się zginać i skręcać, a odpowiadający im obszar na antygenie często jest rozproszony i płytki, zamiast tworzyć głęboką kieszeń. Taka elastyczność i subtelność sprawiają, że problem dokowania — ustalenie, jak te dwa kształty do siebie pasują — jest wyjątkowo trudny dla komputerów. Tradycyjne programy dokujące próbują wielu względnych pozycji obu białek i oceniają je przy użyciu zasad fizycznych, takich jak przyciąganie elektrostatyczne czy przesunięcie wody, ale bez biologicznych wskazówek często wybierają błędne dopasowania.
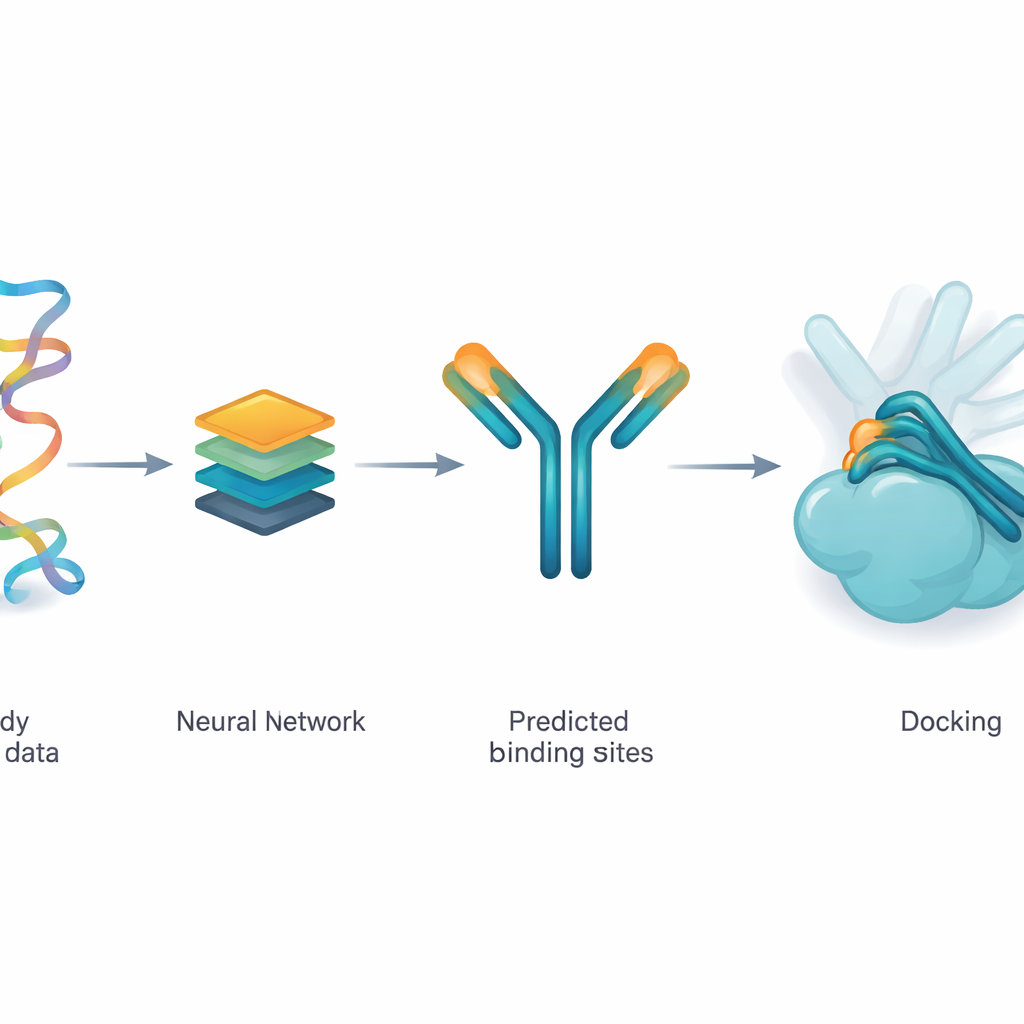
Nauka sieci sugerowania prawdopodobnych miejsc styku
Autorzy wykorzystują model uczenia głębokiego o nazwie ParaDeep do zgadywania, które aminokwasy w przeciwciałe najprawdopodobniej dotkną antygenu. ParaDeep robi to, używając tylko sekwencji przeciwciała — porządku jego elementów budulcowych — zamiast wymagać pełnej struktury 3D. Odczytuje sekwencje łańcuchów ciężkich i lekkich razem, koduje ich cechy chemiczne i położeniowe oraz używa mechanizmów uwagi, aby uwypuklić reszty wyglądające na dobre kandydaty do wiązania. Każde miejsce otrzymuje wynik prawdopodobieństwa; te powyżej progu traktowane są jako przewidywana strefa kontaktu, którą można odwzorować na strukturę przeciwciała.
Wskazywanie silnikowi fizycznemu zamiast jego zastępowania
Zamiast używać uczenia głębokiego do generowania pełnych kompleksów przeciwciało–antygen od podstaw, zespół przekazuje przewidziane przez ParaDeep reszty kontaktowe do istniejącego silnika dokującego opartego na fizyce o nazwie PyDockWEB. Ten program dokujący próbuje tysięcy możliwych sposobów, w jakie przeciwciało i antygen mogą się spotkać, i ocenia je funkcją energii. W nowym podejściu przewidziane reszty kontaktowe działają jako miękkie ograniczenia: faworyzują poszukiwanie tak, by wiele próbkowanych orientacji umieszczało te reszty blisko powierzchni antygenu. Co ważne, podstawowe ocenianie fizyczne i traktowanie białek jako brył sztywnych pozostają niezmienione, co czyni proces przejrzystym i stosunkowo lekkim obliczeniowo.
O ile lepsze stają się przewidywania?
Naukowcy przetestowali swoje hybrydowe podejście na 50 znanych kompleksach przeciwciało–antygen z wyselekcjonowanej bazy danych. Dla każdego przypadku porównali standardowe „ślepe” dokowanie z dokowaniem prowadzonym przez ograniczenia z ParaDeep. Mierzyli lokalną dokładność interfejsu (jak blisko przewidziany obszar kontaktu odpowiada rzeczywistości), ogólne podobieństwo kształtu oraz łączony wskaźnik jakości powszechnie stosowany do oceny modeli dokowania. W całym zestawie metoda prowadzona znacznie zmniejszyła błędy w miejscu wiązania, przesunęła ogólne struktury bliżej rzeczywistych kompleksów i przeniosła wiele przewidywań z kategorii wyraźnie błędnych do średniej lub wysokiej jakości. Prawie połowa modeli prowadzonych trafiła do zakresu wysokiej jakości, wobec około jednej czwartej przy dokowaniu ślepym.
Co sprawia, że niektóre dopasowania są łatwiejsze od innych
Zespół analizował też, dlaczego niektóre kompleksy zyskały więcej niż inne. Stwierdzili, że samo przewidzenie większej liczby reszt kontaktowych nie gwarantuje sukcesu; istotne było umieszczenie ograniczeń we właściwym obszarze, a nie ich liczba. Interfejsy bardziej hydrofilowe i zawierające więcej elastycznych odcinków spiralnych miały tendencję do lepszego dokowania, prawdopodobnie dlatego, że współgrały z naciskiem PyDockWEB na elektrostatykę i były łatwiejsze do wyrównania bez dużych zmian kształtu. Gdy badacze powtórzyli niektóre nieudane przypadki, używając „oraclowych” informacji o kontakcie wyciągniętych bezpośrednio ze struktur eksperymentalnych, większość tych przypadków się poprawiła, co potwierdza, że dokładne zlokalizowanie płata kontaktowego jest kluczowe — lecz dokowanie brył sztywnych nadal ma ograniczenia, gdy potrzebne są duże dostosowania kształtu.
Co to oznacza na przyszłość
Mówiąc w prostych słowach, praca ta pokazuje, że podanie programowi dokującemu opartego na fizyce inteligentnej wskazówki o tym, gdzie przeciwciało prawdopodobnie chwyci cel, może znacznie poprawić jego celowanie, bez przekształcania procesu w nieprzejrzystą czarną skrzynkę. Połączony potok ParaDeep–PyDockWEB nie zastępuje bardziej zaawansowanych metod elastycznych czy generatywnych, ale oferuje praktyczny sposób wykorzystania sygnałów uczenia głębokiego na poziomie sekwencji do kierowania znanymi, interpretowalnymi narzędziami dokującymi. W miarę jak wysiłki związane z odkrywaniem i inżynierią przeciwciał generować będą coraz większe biblioteki sekwencji, takie hybrydowe podejścia mogą pomóc badaczom szybko przesiać kandydatów strukturalnie zgodnych z pożądanym celem, przyspieszając drogę od sekwencji do praktycznego przeciwciała i dostarczając lepszych informacji do dalszego projektowania.
Cytowanie: Kodchakorn, K., Udomwong, P., Pamonsupornwichit, T. et al. Integrating deep learning with physics based modeling enables high precision antibody antigen interface prediction. Sci Rep 16, 8134 (2026). https://doi.org/10.1038/s41598-026-39466-8
Słowa kluczowe: dokowanie przeciwciał, uczenie głębokie, predykcja paratopu, interakcje białko–białko, projektowanie przeciwciał