Clear Sky Science · pl
Wpływ chemioterapii neoadiuwantowej na funkcjonalność mezenchymalnych komórek zrębu pochodzących z tkanki tłuszczowej oraz ich modulacyjne działanie na fibroblasty u pacjentów onkologicznych
Dlaczego ma to znaczenie dla osób po chorobie nowotworowej
Wiele osób po leczeniu onkologicznym boryka się później z powolnym gojeniem ran i powikłaniami po zabiegach chirurgicznych. Równocześnie lekarze coraz częściej badają możliwości wykorzystania własnych komórek naprawczych pacjenta pochodzących z tkanki tłuszczowej do wspierania regeneracji tkanek. W badaniu postawiono praktyczne i pilne pytanie: czy po chemioterapii te komórki naprawcze nadają się jeszcze do użycia, a jeśli nie, które populacje komórek są najbardziej dotknięte?
Ukryci pomocnicy w ciele
Nasza tkanka tłuszczowa to coś więcej niż magazyn energii. Zawiera bogatą populację wszechstronnych komórek naprawczych nazywanych mezenchymalnymi komórkami zrębu pochodzącymi z tkanki tłuszczowej (AD-MSC). Te komórki nie pozostają bierne; uwalniają koktajl sygnałów, które łagodzą stan zapalny, stymulują tworzenie naczyń i pobudzają pobliskie komórki do wzrostu i odbudowy uszkodzonych tkanek. Tuż nad tłuszczem, w skórze, znajdują się fibroblasty — „robotnicy”, które przemieszczają się do ran i odkładają kolagen, białkowy ruszt, który nadaje nowej tkance wytrzymałość. Wspólnie AD-MSC i fibroblasty wpływają na to, jak dobrze skóra regeneruje się po urazie lub operacji.
Badanie komórek naprawczych z tłuszczu przed i po leczeniu
Naukowcy pobrali niewielkie próbki skóry i tkanki tłuszczowej od 66 pacjentów poddawanych zabiegom chirurgicznym — część z nich otrzymała chemioterapię przed zabiegiem, część nie. Z tkanki tłuszczowej wyizolowano AD-MSC i potwierdzono, że komórki te nadal odpowiadają oczekiwanym cechom: miały typowe markery powierzchniowe i w warunkach laboratoryjnych potrafiły różnicować się w komórki o cechach kostnych, chrzęstnych i tłuszczowych. Ze skóry wyizolowano fibroblasty. Zespół porównał, jak AD-MSC i fibroblasty z pacjentów po ekspozycji na chemioterapię i bez niej różniły się w zakresie wzrostu, cyklu komórkowego, wydzielania czynników sygnałowych oraz ekspresji genów związanych z gojeniem i regeneracją.
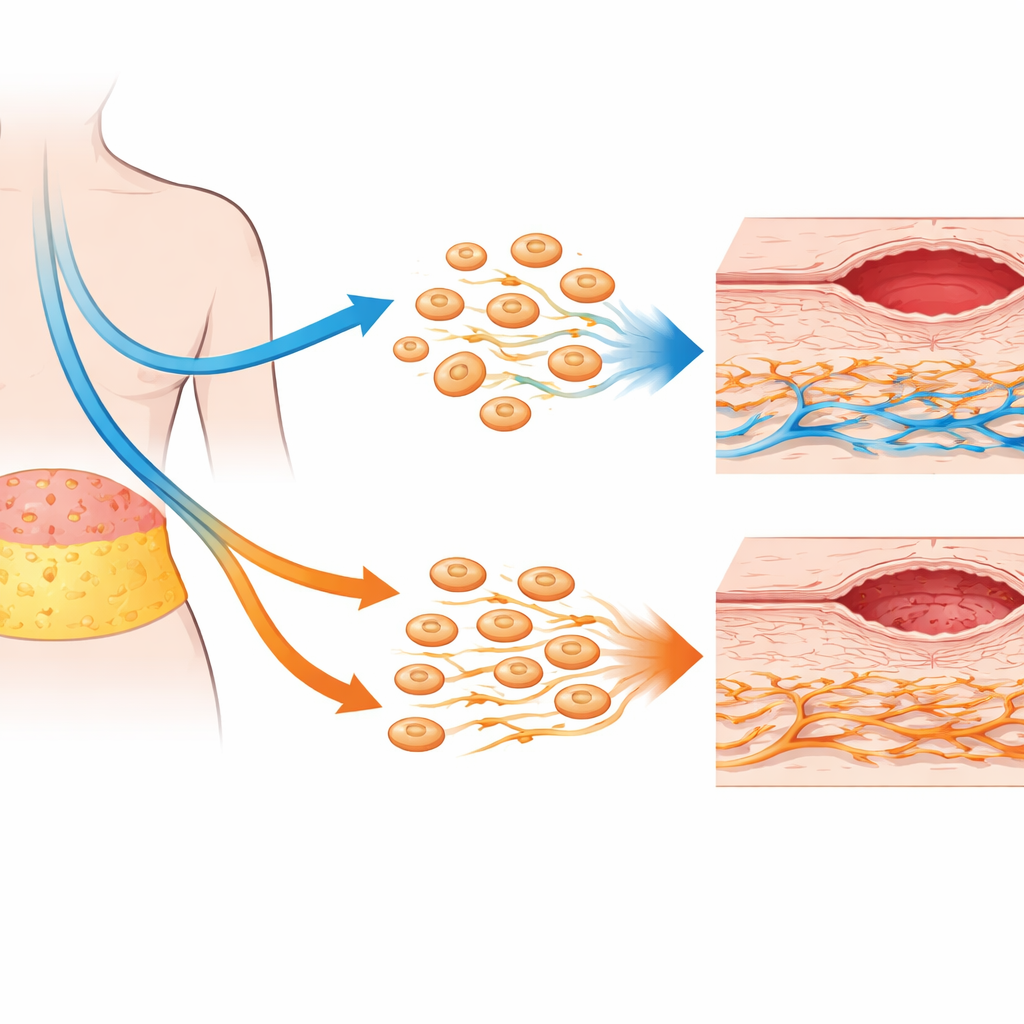
Komórki naprawcze z tłuszczu pozostają zaskakująco odporne
Wbrew obawom, że chemioterapia mogłaby osłabić potencjał AD-MSC, badanie wykazało, że te komórki pochodzące z tkanki tłuszczowej są wyjątkowo odporne. Ich podstawowe markery tożsamości, wzorzec wzrostu i profil wydzielanych białek sygnałowych pozostały w dużej mierze niezmienione po wcześniejszym leczeniu chemioterapią. Aktywność genów związanych z wzrostem, samoodnawianiem i gojeniem wykazywała jedynie niewielkie, niemające znaczenia klinicznego zmiany. Co więcej, AD-MSC od pacjentów po chemioterapii wykazywały nieco wyższą aktywność mitochondrialną, co sugeruje bardziej żywotny metabolizm, a nie uszkodzenie. W eksperymentach współhodowli — gdzie AD-MSC i fibroblasty dzieliły to samo medium, ale nie miały bezpośredniego kontaktu — AD-MSC wciąż wzmacniały niektóre zachowania fibroblastów, takie jak ukierunkowana migracja w stronę sygnałów naprawczych, zwłaszcza w próbkach od pacjentów, którzy nie otrzymali chemioterapii.
Budowniczowie skóry ponoszą konsekwencje chemioterapii
Obraz wyglądał natomiast zupełnie inaczej w przypadku fibroblastów. Komórki pobrane ze skóry pacjentów po chemioterapii wykazywały wyraźne oznaki obniżonej żywotności biologicznej. Ich zdolność do przemieszczania się w „zarysowaną” na płytce kulturę symulującą ranę była istotnie osłabiona, a produkcja kolagenu miała tendencję do obniżenia. Profil wydzielanych przez nie czynników przesunął się w kierunku bardziej zapalnym i mniej regeneracyjnym, a wiele genów związanych z sygnałami wzrostu, ich receptorami i potencjałem regeneracyjnym zostało przytłumionych. Nawet w warunkach współhodowli z własnymi AD-MSC, większość funkcji tych fibroblastów — migracja, produkcja kolagenu i korzystna aktywność genów — pozostała osłabiona w porównaniu z fibroblastami od pacjentów, którzy nie przeszli chemioterapii.
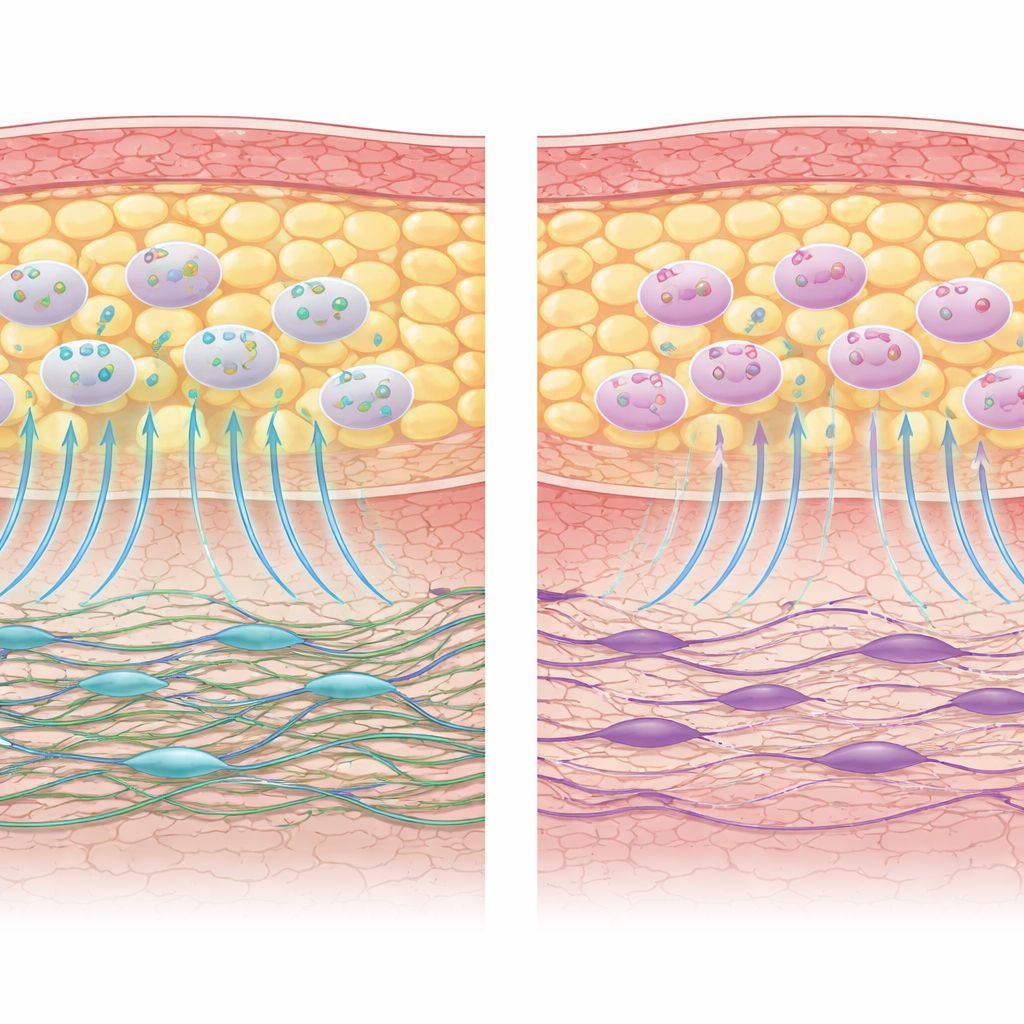
Co to oznacza dla przyszłych terapii leczących rany
Dla osoby niebędącej specjalistą przesłanie pracy jest takie: chemioterapia nie wydaje się niszczyć banku komórek naprawczych pochodzących z tłuszczu, ale osłabia pierwszoliniowych budowniczych skóry — fibroblasty — które są mniej zdolne do szybkiego zasiedlania ran i odbudowy wytrzymałej tkanki. Ponieważ AD-MSC pozostają funkcjonalnie zachowane, nadal są obiecującymi kandydatami do wykorzystania w zabiegach rekonstrukcyjnych, terapii ran i przeszczepach tłuszczu po leczeniu nowotworu. Jednak uszkodzony stan fibroblastów może ograniczać zakres korzyści, jakie te komórki typu „stem-like” mogą same dostarczyć. Autorzy sugerują, że przyszłe terapie mogą wymagać wsparcia obu ogniw partnerstwa naprawczego: ochrony lub przywrócenia zdrowia fibroblastów oraz wykorzystania odpornych AD-MSC, najlepiej w bardziej złożonych, przypominających organizm modelach, które lepiej oddadzą rzeczywiste środowisko gojenia u osób po leczeniu onkologicznym.
Cytowanie: Skoniecka, A., Słonimska, P., Tymińska, A. et al. Impact of neoadjuvant chemotherapy on the functionality of adipose-derived mesenchymal stromal cells and their modulatory effects on fibroblasts in oncology patients. Sci Rep 16, 8614 (2026). https://doi.org/10.1038/s41598-026-39457-9
Słowa kluczowe: chemioterapia, gojenie ran, komórki macierzyste z tkanki tłuszczowej, fibroblasty, medycyna regeneracyjna