Clear Sky Science · pl
Odkrywanie potencjalnych związków przeciwwirusowych i przyspieszenie odkrywania terapii przeciw wirusowi ospy małpiej
Dlaczego te badania są ważne teraz
Ospa małpia, dziś często określana jako mpox, przestała być rzadką chorobą tropikalną i stała się problemem globalnym — w ostatnich latach odnotowano ogniska na kilku kontynentach. W odróżnieniu od COVID-19 wciąż nie ma leku stworzonego specjalnie przeciw temu wirusowi. W tym badaniu wykorzystano zaawansowane narzędzia komputerowe do poszukiwania nowych małych cząsteczek, które mogłyby unieszkodliwić wirusa w jego najsłabszym punkcie: zdolności do ukrywania się przed naszym układem odpornościowym. Jeśli wynik potwierdzą badania laboratoryjne, wytypowane związki mogą stać się punktem wyjścia dla nowej klasy leków przeciwwirusowych.
Jak wirus ukrywa się przed naszymi obronami
Ospa małpia należy do tego samego szerszego rodu wirusów co ospa prawdziwa i stosuje sprytny trik, aby unikać układu odpornościowego. Nasze komórki wydzielają białko sygnalizacyjne zwane interferonem-gamma, które zwykle ostrzega komórki sąsiednie i uruchamia mechanizmy przeciwwirusowe. Wirus jednak wytwarza własne białko sekrecyjne, nazywane B8R, które unosi się poza zainfekowanymi komórkami. B8R ściśle naśladuje nasz receptor dla interferonu-gamma i przechwytuje te sygnały zanim dotrą do swojego prawdziwego celu. W praktyce działa jak gąbka, wchłaniając alarmowe komunikaty organizmu i uniemożliwiając pełną odpowiedź przeciwwirusową.
Wykorzystanie komputerów do projektowania bardziej inteligentnych terapii
Tradycyjne odkrywanie leków może trwać wiele lat i wymagać ogromnych zasobów. W tym przypadku badacze zwrócili się ku projektowaniu leków wspieranemu komputerowo, aby przyspieszyć proces. Ponieważ nie było dostępnej eksperymentalnej struktury 3D białka B8R, najpierw zastosowali narzędzia oparte na AlphaFold, aby przewidzieć jego atomowy kształt i starannie ocenili jakość tego modelu. Dysponując wiarygodną strukturą 3D, przeprowadzili wirtualne przesiewanie biblioteki chemicznej obejmującej 5000 małych cząsteczek. Zastosowano reguły opisujące właściwości typowego leku w formie tabletki (takie jak rozmiar, kształt i rozpuszczalność), aby odfiltrować słabe kandydatury, pozostawiając 2890 obiecujących związków do szczegółowego testowania przeciw modelowi białka B8R.
Znalezienie obiecującego „klucza” chemicznego
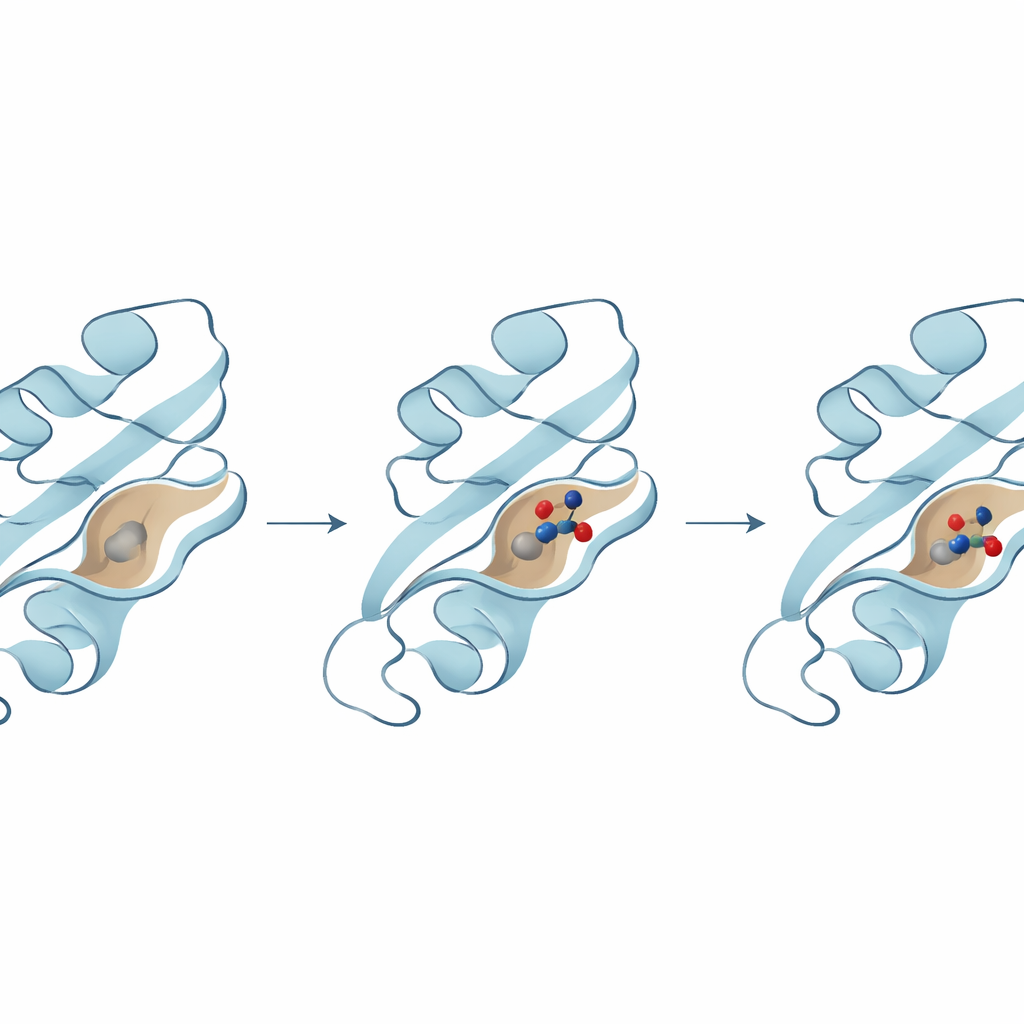
Następny krok polegał na sprawdzeniu, które molekuły mogą ciasno dopasować się do ważnej kieszeni na powierzchni B8R, tam gdzie normalnie wiąże się interferon-gamma. Zespół zastosował dokowanie molekularne — technikę, która sprawdza miliardy możliwych orientacji cząsteczki w kieszeni białka i ocenia, jak silne byłoby wiązanie. Wyłoniły się trzy główne kandydatury, z których każda miała przewidywane silne interakcje z kluczowymi aminokwasami w kieszeni. Jeden związek wykazał szczególnie najsilniejszą energię wiązania i nawiązał kilka stabilizujących kontaktów z krytycznymi resztami, co sugeruje, że może być szczególnie skuteczny w blokowaniu aktywności B8R.
Obserwowanie ruchu molekuł w czasie
Białka i molekuły leków nie są sztywne; poruszają się, wyginają i „oddychają” w wodnym otoczeniu. Aby to uchwycić, badacze uruchomili długie symulacje dynamiki molekularnej — wirtualne filmy trwające setki nanosekund — żeby zobaczyć, jak zachowuje się każda para białko–związek w czasie. Symulacje wykazały, że najlepiej sprawdzający się związek pozostał głęboko schowany w kieszeni B8R, przy czym białko lekko dostosowywało się wokół niego, zachowując stabilność strukturalną. Natomiast pozostałe dwa związki bardziej się przemieszczały, wchodziły do alternatywnych kieszeni lub wykazywały większe fluktuacje, co sugeruje słabsze lub mniej pewne wiązanie. Dodatkowe analizy elastyczności, energii i ruchów w dużej skali potwierdziły ten sam faworyt: pojedynczą cząsteczkę, która konsekwentnie tworzyła najbardziej stabilny i energetycznie korzystny kompleks.
Co to może znaczyć dla przyszłych terapii
Badanie nie twierdzi, że odkryto gotowy lek — nie przeprowadzono jeszcze eksperymentów w komórkach ani na zwierzętach. Zamiast tego dostarcza mocnego, opartego na danych punktu wyjścia: konkretnej małej cząsteczki, która wydaje się idealnie dopasowana do zablokowania białka B8R wirusa ospy małpiej i potencjalnie przywrócenia systemu alarmowego interferonu w organizmie. Skierowanie terapii przeciw strategii unikania układu odpornościowego wirusa, a nie przeciw mechanizmom replikacji, oferuje nową perspektywę w terapii przeciwwirusowej. Autorzy sugerują, że ich wiodący związek powinien teraz zostać przetestowany w laboratorium, gdzie można bezpośrednio ocenić jego zdolność do blokowania B8R i ograniczania zakażenia mpox. Jeśli te testy będą udane, może to utorować drogę do ukierunkowanego leku, który pomoże układowi odpornościowemu lepiej widzieć i zatrzymywać wirusa.
Cytowanie: Ahmad, F., Navid, A., Irfan, M. et al. Discovery of potential antiviral compounds and accelerating the therapeutic discovery against monkeypox virus. Sci Rep 16, 8306 (2026). https://doi.org/10.1038/s41598-026-39427-1
Słowa kluczowe: przeciwwirusowy przeciwko ospie małpiej, unikanie układu odpornościowego, odkrywanie leków, modelowanie komputerowe, sygnalizacja interferonowa