Clear Sky Science · pl
Utrata obciążenia mechanicznego wywołuje zapalenie błony maziowej, włóknienie i degenerację chrząstki stawowej poprzez odrębne podzbiory komórek błony maziowej
Dlaczego odpoczynek stawów może być ryzykowny
Wielu z nas słyszało, że nadmierne obciążanie stawów może je zużyć, ale badanie to pokazuje, że zbyt mała ich eksploatacja także im szkodzi. Naukowcy zastosowali model myszy, by zbadać, co dzieje się w obrębie stawu kolanowego, gdy ruch i podparcie ciężaru są drastycznie ograniczone przez tygodnie — podobnie jak po długotrwałym unieruchomieniu w gipsie, przy porażeniu czy przedłużonym leżeniu w łóżku. Śledząc mikroskopowe zmiany tkankowe i aktywność genów komórka po komórce, odkryli, jak utrata obciążenia mechanicznego zapoczątkowuje łańcuch zdarzeń w wyściółce stawu, który ostatecznie uszkadza gładką chrząstkę niezbędną do bezbolesnego ruchu.
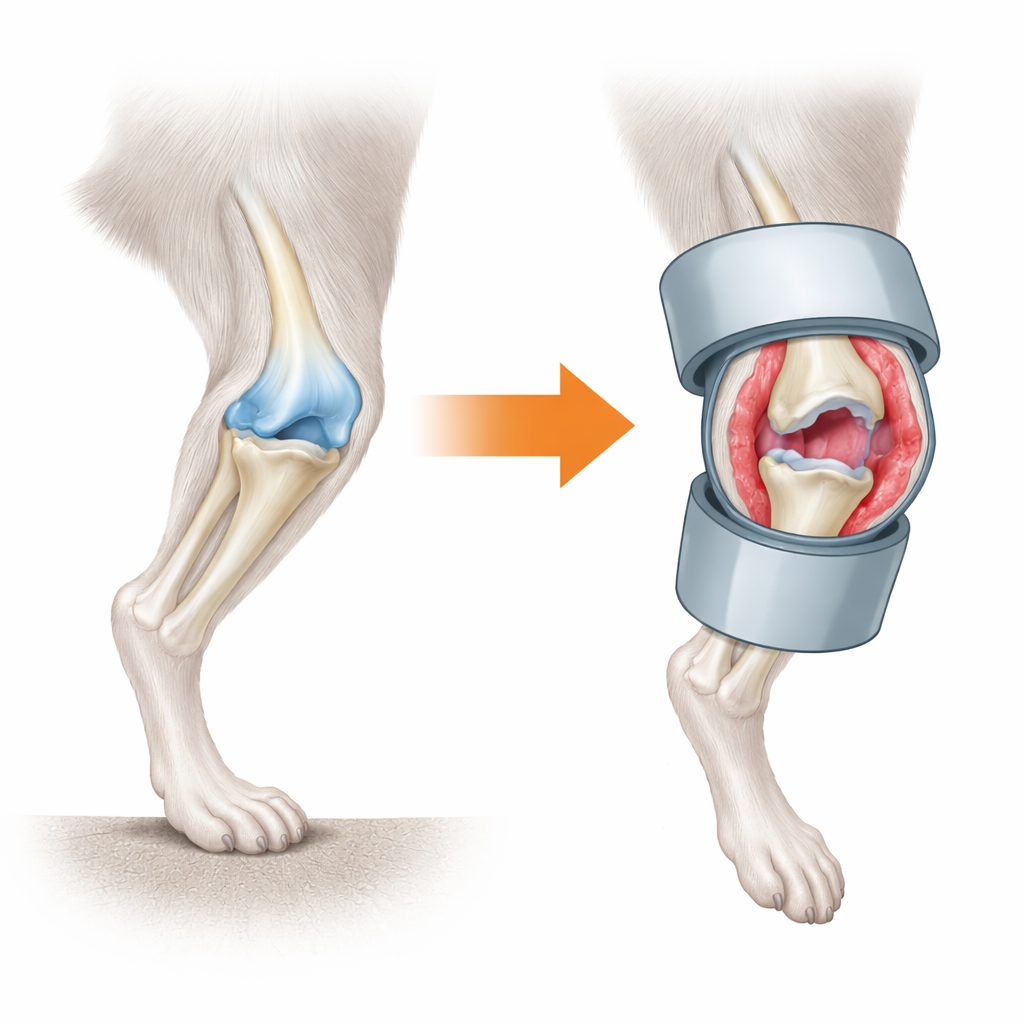
Co się dzieje, gdy kolano przestaje się ruszać
Zespół opracował model „zredukowanego obciążenia mechanicznego”, unieruchamiając kolana myszy małymi plastikowymi cylindrami i zawieszając ogony zwierząt, tak by kończyny tylne nie przenosiły ciężaru. Już po trzech dniach wewnętrzna wyściółka stawu, zwana błoną maziową, wykazywała stan zapalny: warstwy komórek pogrubiały się, pojawiały się nowe naczynia krwionośne, a komórki układu odpornościowego gromadziły się. W ciągu kolejnych dwóch tygodni wyściółka przekształciła się w włóknistą, bliznopodobną tkankę, a staw stał się sztywny. Chrząstka — śliska tkanka pokrywająca końce kości — nie rozpadała się natychmiast. Zamiast tego zaczęła wykazywać szorstkość i ubytek warstwy powierzchniowej dopiero po tym, gdy zmiany w błonie maziowej były już zaawansowane, a uszkodzenia nasilały się w ciągu sześciu tygodni.
Ruch i nacisk jako lekarstwo dla stawów
Naukowcy zapytali następnie, czy te zmiany można odwrócić. Po dwóch tygodniach unieruchomienia i odciążenia niektóre myszy odzyskały jedynie ruch stawu przy nadal braku obciążenia, inne zaś odzyskały zarówno ruch, jak i przenoszenie ciężaru. W obu grupach stan zapalny błony maziowej zmniejszył się, a wyściółka cieniała w kierunku normalnego stanu, co dowodzi, że sam ruch ma silny wpływ na zdrowie wyściółki stawu. Chrząstka natomiast regenerowała się najlepiej, gdy przywrócono zarówno ruch, jak i obciążenie. Na poziomie molekularnym geny związane z budową zdrowej chrząstki były wyraźnie stłumione podczas bezruchu, ale w dużym stopniu powracały do aktywności po ponownym umożliwieniu stawom ruchu i przenoszenia ciężaru. Sugeruje to, że chrząstka potrzebuje kombinacji ruchu ślizgowego i łagodnego nacisku, by utrzymać swoją strukturę.
W jaki sposób komórki wyściółki stawu napędzają uszkodzenie chrząstki
Zagłębiając się dalej, naukowcy zbadali, które geny uaktywniały się w błonie maziowej w miarę postępu uszkodzeń. Stwierdzili wzrost aktywności genów związanych z włóknieniem, przebudową tkanki oraz enzymami zdolnymi rozkładać chrząstkę. Wiele z tych sygnałów pochodziło od mediatorów związanych z układem odpornościowym, takich jak cytokiny zapalne i czynniki wzrostu, które mogą oddziaływać na sąsiednie komórki chrząstki. Sekwencjonowanie RNA pojedynczych komórek wykazało, że bezruch zmienił skład komórkowy w błonie maziowej. W dwóch nietypowych grupach komórkowych, które rozszerzyły się w unieruchomionych stawach, rozpoznano komórki przypominające miofibroblasty specjalizujące się w produkcji włóknistej macierzy oraz podzbiór makrofagów wykazujących wysoką ekspresję cząsteczek zapalnych i enzymów rozkładających chrząstkę. Razem te komórki tworzyły odrębne, sprzyjające uszkodzeniom mikrośrodowisko wokół stawu.
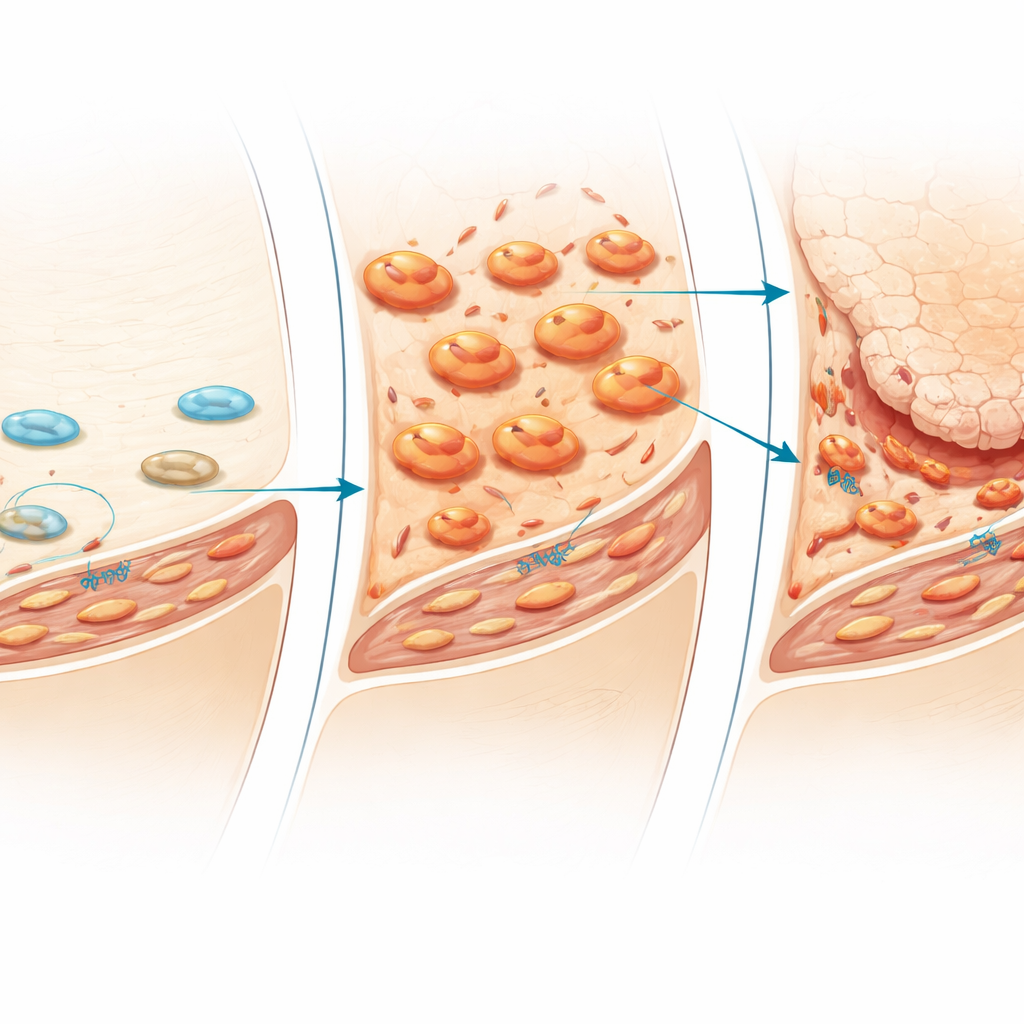
Wczesna rola komórek odpornościowych
Czas okazał się kluczowy. W przekrojach tkankowych pobranych na różnych etapach makrofagi pojawiały się najpierw w cienkiej wyściółce błony maziowej zaledwie kilka dni po usunięciu obciążenia mechanicznego, a następnie rozprzestrzeniały się głębiej w tkance. Dopiero później proliferowały fibroblasty i pojawiała się gęsta tkanka włóknista. Gdy zespół selektywnie usunął makrofagi z błony maziowej, wstrzykując liposomy eliminujące te komórki, kaskada zdarzeń zmieniła się diametralnie: zapalenie i włóknienie wyściółki stawu zostały silnie ograniczone, a degeneracja chrząstki była wyraźnie łagodniejsza. Spadły też markery podzbioru miofibroblastów. Wyniki te wskazują na makrofagi jako wczesnych organizatorów szkodliwej odpowiedzi na brak obciążenia, aktywujących fibroblasty i przygotowujących grunt pod późniejsze rozkładanie chrząstki.
Co to oznacza dla ochrony stawów
Podsumowując, badanie pokazuje, że stawy potrzebują regularnego ruchu i odpowiedniego obciążenia mechanicznego, by utrzymać równowagę między błoną maziową a chrząstką. Gdy ten mechaniczny bodziec zanika, wyspecjalizowane komórki odpornościowe i fibroblasty w błonie maziowej przechodzą w stan zapalny i włóknisty, który stopniowo eroduje chrząstkę. Co ważne, przywrócenie ruchu i obciążenia może odwrócić ten proces, zwłaszcza jeśli nastąpi zanim uszkodzenia będą zaawansowane. Dla osób stojących w obliczu długotrwałej immobilizacji — z powodu gipsu, paraliżu czy przedłużonego leżenia — wyniki te podkreślają znaczenie wczesnego, ukierunkowanego ruchu stawów i bezpiecznego obciążania, a także wskazują na możliwe przyszłe terapie farmakologiczne celujące w oś makrofag–fibroblast w celu zapobiegania trwałym uszkodzeniom stawów.
Cytowanie: Ishikura, H., Okada, H., Kin, Y. et al. Loss of mechanical stress induces synovitis, fibrosis and articular cartilage degeneration via distinct synovial cell subsets. Sci Rep 16, 8007 (2026). https://doi.org/10.1038/s41598-026-39416-4
Słowa kluczowe: unieruchomienie stawu, zapalenie błony maziowej, degeneracja chrząstki, obciążenie mechaniczne, makrofagi