Clear Sky Science · pl
Ustanowienie solidnego modelu przedklinicznego do badania wczesnych i późnych reakcji skórnych wywołanych promieniowaniem
Dlaczego to ma znaczenie dla osób z rakiem
Nowoczesna radioterapia ratuje życie, ale może nadwyrężyć skórę, powodując bolesne zaczerwienienie, złuszczanie oraz długotrwałe stwardnienie lub bliznowacenie. Lekarze wiedzą, że te reakcje są powiązane z dawką promieniowania, jednak trudno było badać je szczegółowo lub bezpiecznie testować nowe terapie. W artykule opisano starannie opracowany model na myszach, który odtwarza zarówno wczesne, jak i późne problemy skórne obserwowane u pacjentów, oferując praktyczne pole do testowania łagodniejszych schematów napromieniania i terapii ochronnych. 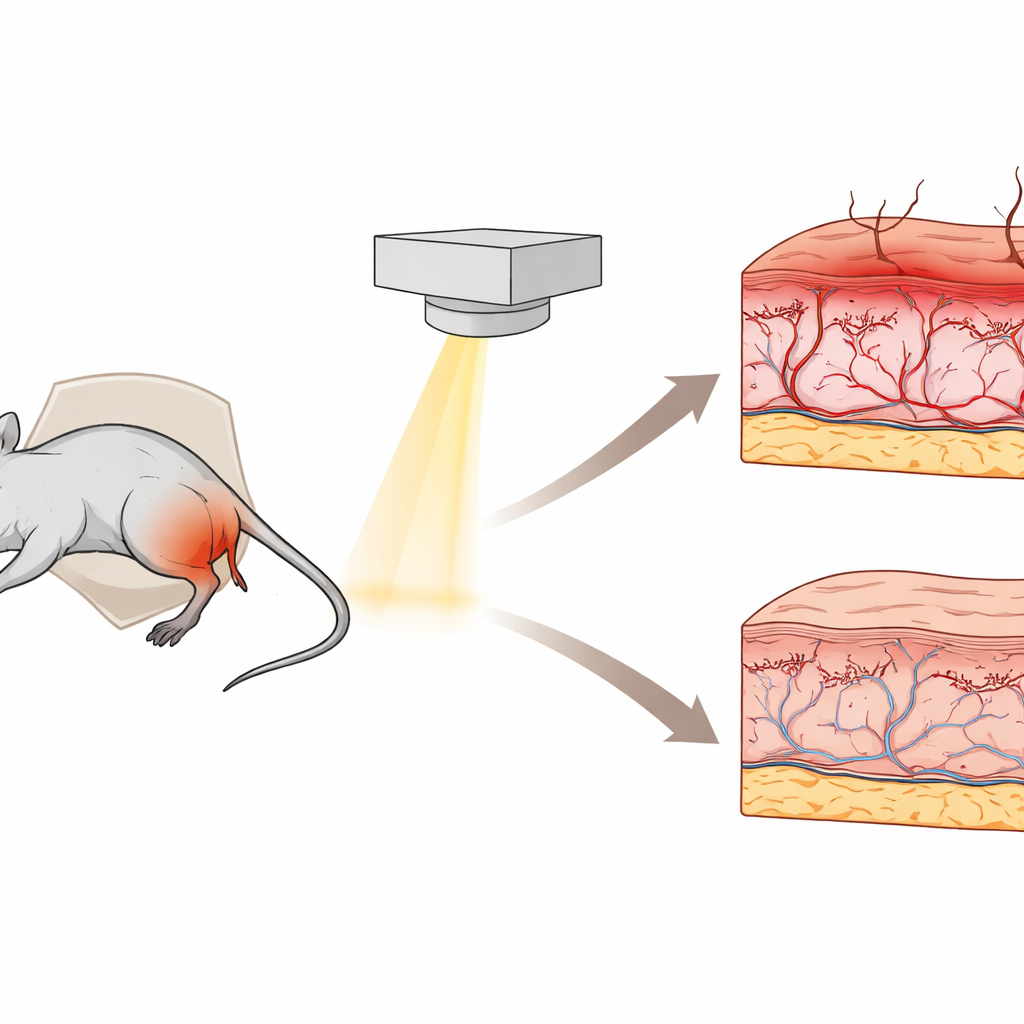
Przekształcenie powszechnego skutku ubocznego w przedmiot badań
Gdy guz jest leczony promieniowaniem, przylegająca zdrowa skóra często płaci za to cenę. Wczesne zmiany mogą pojawić się w ciągu dni do tygodni jako zaczerwienienie, obrzęk i złuszczanie, podczas gdy zmiany późne — miesiące lub lata później — mogą objawiać się utratą włosów, stwardnieniem lub bliznowaceniem skóry. Te problemy mogą opóźniać leczenie i obniżać jakość życia, a istniejące badania na zwierzętach zwykle koncentrują się tylko na uszkodzeniach krótkoterminowych lub stosują pojedyncze, bardzo wysokie dawki promieniowania, które nie przypominają standardowej opieki klinicznej. Autorzy postanowili zbudować bardziej realistyczny model, który śledzi zarówno wczesne, jak i późne uszkodzenia skóry w czasie, stosując frakcjonowane napromienianie — to samo podstawowe podejście używane w radioterapii u ludzi.
Jak zbudowano nowy model na myszach
Naukowcy pracowali z samcami myszy Swiss albino i skupili promieniowanie na małym obszarze prawej tylnej kończyny, osłaniając resztę ciała ołowiem. To ustawienie pozwoliło uszkodzić dobrze określony obszar skóry bez krzywdzenia narządów wewnętrznych, podobnie jak w przypadku celowania w guz pacjenta przy jednoczesnej ochronie otaczających tkanek. Jedna grupa myszy otrzymała łącznie 30 jednostek dawki rozłożonych na trzy sesje dzienne; druga grupa otrzymała 50 jednostek w pięciu sesjach, co lepiej odzwierciedla powtarzane ekspozycje stosowane w praktyce klinicznej. W ciągu następnego miesiąca dermatolog, nieświadomy, którą dawkę otrzymała dana mysz, oceniała widoczne zmiany skórne za pomocą standardowej skali klinicznej, a niewielkie próbki skóry pobierano w dniach 15 i 30 do analizy mikroskopowej.
Jak wyglądały wczesne reakcje skórne
Wyniki widoczne w skali wykazały wyraźną zależność od dawki. Grupa o niższej dawce zazwyczaj rozwijała umiarkowane reakcje, które osiągały szczyt około 10. dnia i goiły się do 30. dnia. Natomiast grupa o wyższej dawce rozwijała poważniejsze reakcje, osiągające szczyt nieco później i wymagające około pięciu dodatkowych dni na pełne wyzdrowienie. Pod mikroskopem napromieniona skóra wykazywała pogrubioną warstwę zewnętrzną, większą liczbę komórek zapalnych oraz wyraźny spadek liczby mieszków włosowych w porównaniu z nienarażoną skórą na drugiej nodze. Wyższa dawka powodowała silniejszy stan zapalny, uszkodzenie powierzchni i charakterystyczny wzorzec zmian powierzchniowych wskazujący na szybki, zestresowany obrót komórek skóry. Te cechy bardzo przypominają obrazy kliniczne obserwowane u pacjentów z silnymi wczesnymi reakcjami skórnymi na promieniowanie. 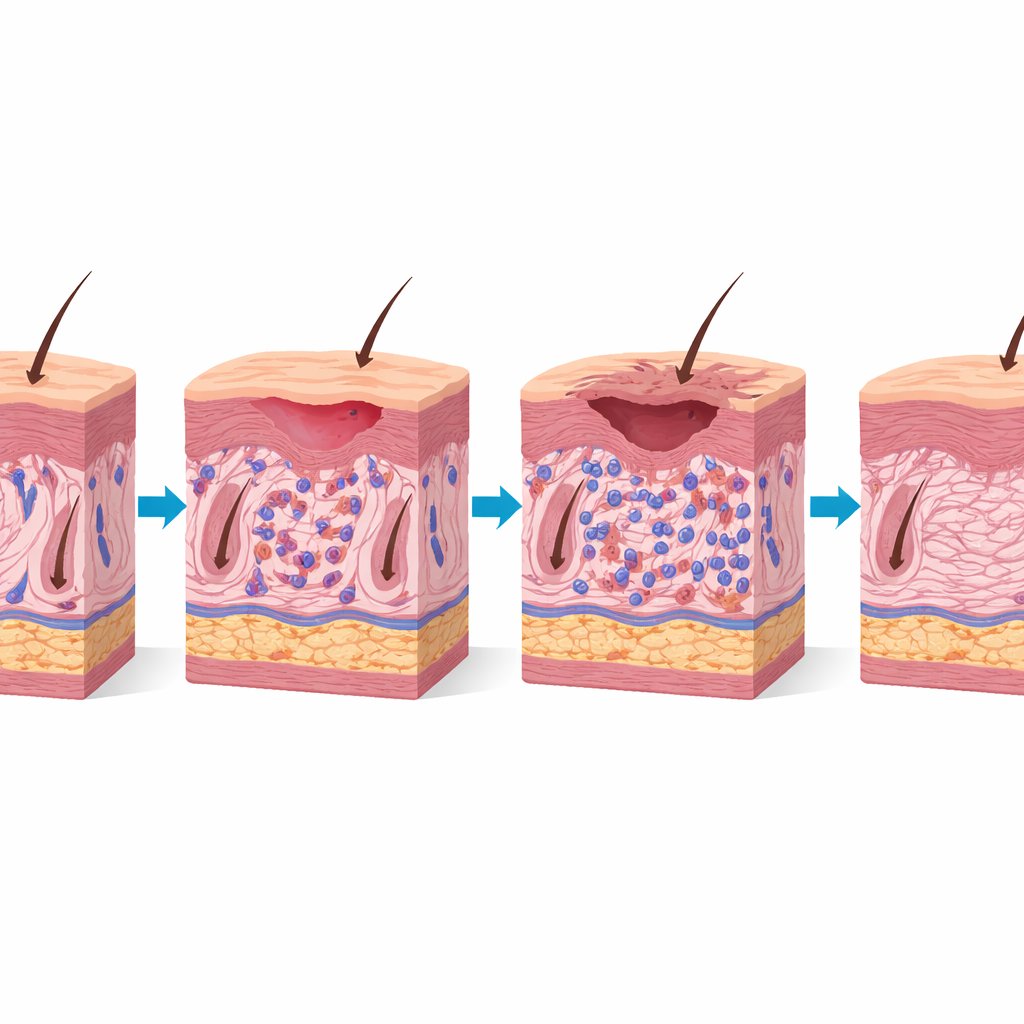
Śledzenie długoterminowego bliznowacenia i utraty włosów
Aby uchwycić efekty późne, myszy, które otrzymały wyższą dawkę, obserwowano przez cztery miesiące. Z zewnątrz leczona skóra stopniowo traciła włosy i nabrała bardziej jędrnej, nieco wklęsłej tekstury, co sugeruje początek zwłóknienia — bliznowatego pogrubienia. Barwienia tkankowe uwypuklające włókna kolagenowe potwierdziły to wrażenie: leczona skóra miała grubszy, gęściej upakowany i zdezorganizowany kolagen w głębszej warstwie, wraz z trwałą utratą mieszków włosowych. Ocena patologa wykazała wyższy stopień zapalenia, zwłóknienia i zaburzeń komórkowych w leczonej skórze niż w skórze nieleczonej, podczas gdy głębsza tkanka mięśniowa wykazywała łagodniejsze zmiany. Łącznie wyniki te wskazują, że te same zwierzęta najpierw rozwijały wczesną, odwracalną reakcję, a później bardziej trwały, bliznowaty stan, odzwierciedlając przebieg obserwowany w skórze ludzkiej.
Co ten model oznacza dla przyszłej opieki
Odtwarzając zarówno krótkotrwałe podrażnienie, jak i długotrwałe bliznowacenie w jednym, kontrolowanym modelu myszy wykorzystującym klinicznie istotne schematy napromieniania, badanie to oferuje potężne narzędzie do przyszłych badań. Naukowcy mogą teraz badać, jak komórki skóry, komórki układu odpornościowego i tkanka podporowa reagują w czasie, oraz systematycznie testować leki, opatrunki czy terapie oparte na świetle, mające na celu ochronę skóry lub przyspieszenie gojenia. Ostatecznie wnioski płynące z tego modelu mogą pomóc uczynić radioterapię nie tylko skuteczną przeciw guzom, ale także bardziej łagodną dla skóry, zmniejszając ból, unikając przerw w leczeniu i poprawiając jakość życia osób poddawanych opiece onkologicznej.
Cytowanie: Pai, P.A.N., Mumbrekar, K.D., Mahato, K.K. et al. Establishing a robust preclinical model to investigate early and late radiation-induced skin reactions. Sci Rep 16, 9064 (2026). https://doi.org/10.1038/s41598-026-39414-6
Słowa kluczowe: reakcje skórne wywołane promieniowaniem, efekty uboczne radioterapii, zwłóknienie skóry, przedkliniczny model myszy, toksyczność leczenia nowotworów