Clear Sky Science · pl
Optymalizacja monocytów THP-1-CAR wykorzystujących sygnalizację CD32a do fagocytozy i aktywacji swoistych limfocytów T
Uczenie układu odpornościowego nowych sztuczek
Nowoczesne terapie komórkowe już przeprogramowują komórki odpornościowe, by tropiły nowotwory, ale większość opiera się na limfocytach T, które mogą mieć trudności w surowym środowisku guzów litych. W tym badaniu autorzy zwracają się zamiast tego ku innemu potężnemu obrońcy — makrofagom, zawodowym „pożeraczom” organizmu — i pytają, jak je przeprojektować, by nie tylko skuteczniej pochłaniały szkodliwe komórki lub wirusy, lecz także przywoływały limfocyty T, zapewniając trwalszy, ukierunkowany atak. Praca ujawnia zasady projektowania lepszych chimerycznych receptorów antygenowych (CAR) dla makrofagów, które mogą znaleźć zastosowanie zarówno w infekcjach, jak COVID-19, jak i w trudno leczonych guzach litych.
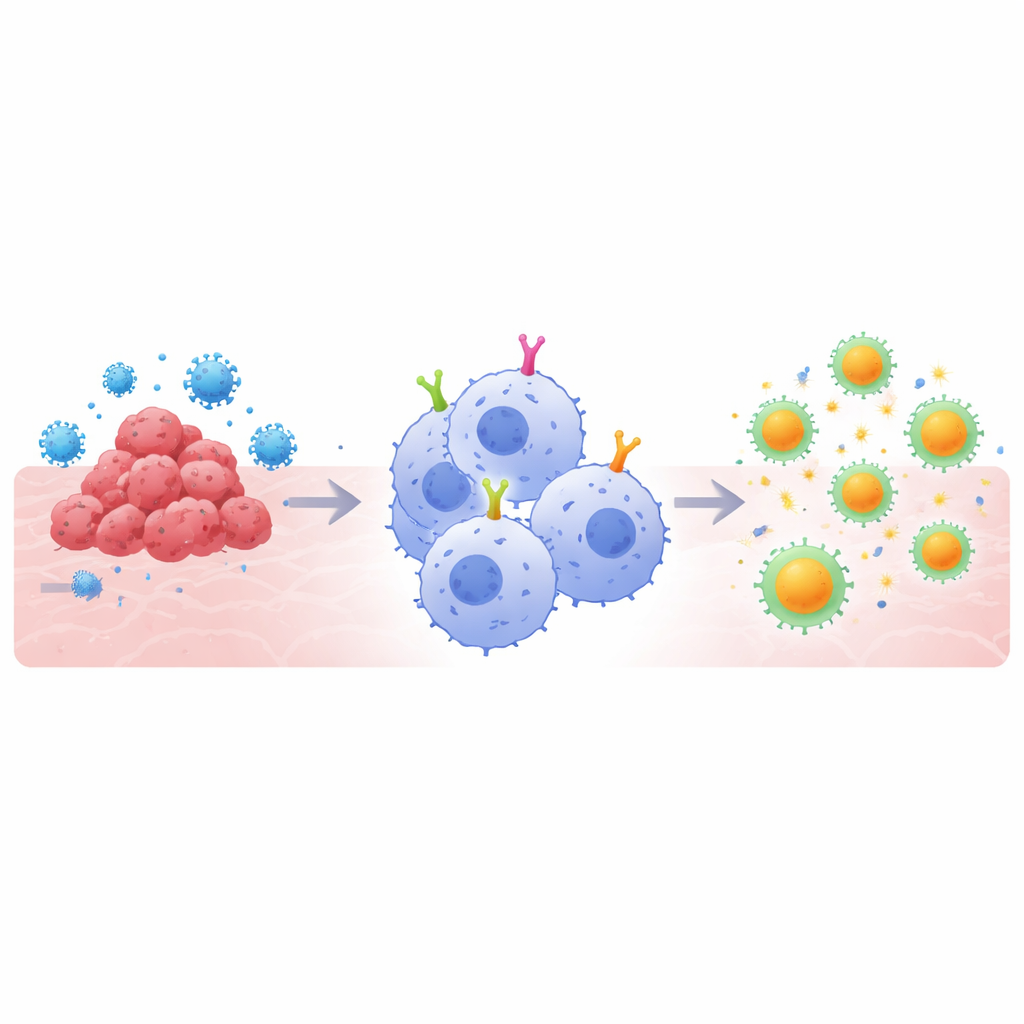
Dlaczego super‑pożeracze są ważne
Terapie oparte na CAR działają przez wyposażenie komórek odpornościowych w niestandardowe receptory powierzchniowe rozpoznające wybrany cel, taki jak białko nowotworowe czy kolcówka wirusa. Wersje z limfocytami T zrewolucjonizowały leczenie niektórych nowotworów krwi, ale napotykają przeszkody przeciw guzom litym i w niektórych infekcjach. Makrofagi oferują inne podejście: naturalnie pochłaniają zagrożenia i rozdrabniają je na fragmenty, które mogą być prezentowane limfocytom T, łącząc „wrodzoną” i „nabyta” część odporności. Jednak większość projektów CAR została pierwotnie stworzona dla limfocytów T, a nie makrofagów. Autorzy założyli, że aby w pełni wykorzystać zalety makrofagów, wewnętrzne fragmenty sygnałowe CAR — segmenty, które informują komórkę, co robić po związaniu celu — będą musiały być dostosowane specjalnie do tych „pożerających” komórek.
Poszukiwanie najlepszego okablowania wewnętrznego
Zespół systematycznie porównał kilka wewnętrznych domen sygnałowych wbudowanych w CAR wprowadzanych do ludzkiej linii monocytów (THP‑1), które można przekształcić w makrofagi. Skoncentrowali się na domenach pochodzących z receptorów, które normalnie napędzają fagocytozę i zapalenie: CD3ζ (klasyczny moduł limfocytów T), CD32a (receptor wiążący cele opsonizowane przeciwciałem), składniki CR3 CD11b i CD18 (kluczowe receptory dopełniacza) oraz TLR4 (czujnik mikrobiologicznego zagrożenia). Używając kulek i pseudowirusów pokrytych białkiem kolca SARS‑CoV‑2, mierzyli, jak dobrze każdy projekt CAR umożliwia komórkom pochłanianie celów, wytwarzanie molekuł zapalnych oraz następnie aktywację ludzkich limfocytów CD8, które wcześniej zetknęły się z wirusem. Następnie przenieśli najbardziej obiecujące projekty do CAR skierowanych przeciw mesotelinie, białku nadmiernie eksprymowanym w wielu guzach litych, aby sprawdzić, czy te same zasady sprawdzają się w kontekście nowotworowym.
Budowanie lepszych pożeraczy i wzmacniaczy sygnału
Wyłonił się wyraźny wzorzec: CAR oparte na CD32a konsekwentnie indukowały silniejszą i szybszą fagocytozę niż te wykorzystujące konwencjonalny moduł CD3ζ, pomimo że CD3ζ zawierało więcej typowych motywów aktywacyjnych. Innymi słowy, „dopasowanie” między sygnałem a machiną makrofaga miało większe znaczenie niż sama siła sygnału. Dodanie fragmentów pochodzących z CR3 (CD11b lub CD18) do CD32a nie zwiększało w większości warunków zdolności pochłaniania, ale podnosiło poziomy kluczowych cytokin zapalnych, takich jak TNF‑α i IL‑1β. Kombinacje zawierające TLR4 posunęły się jeszcze dalej w zwiększaniu sygnałów zapalnych i markera powierzchniowego CD86, związanego ze zdolnością do stymulacji limfocytów T, choć wiązało się to z kompromisami: niższym poziomem CAR na powierzchni komórki i nieco zmniejszoną fagocytozą.
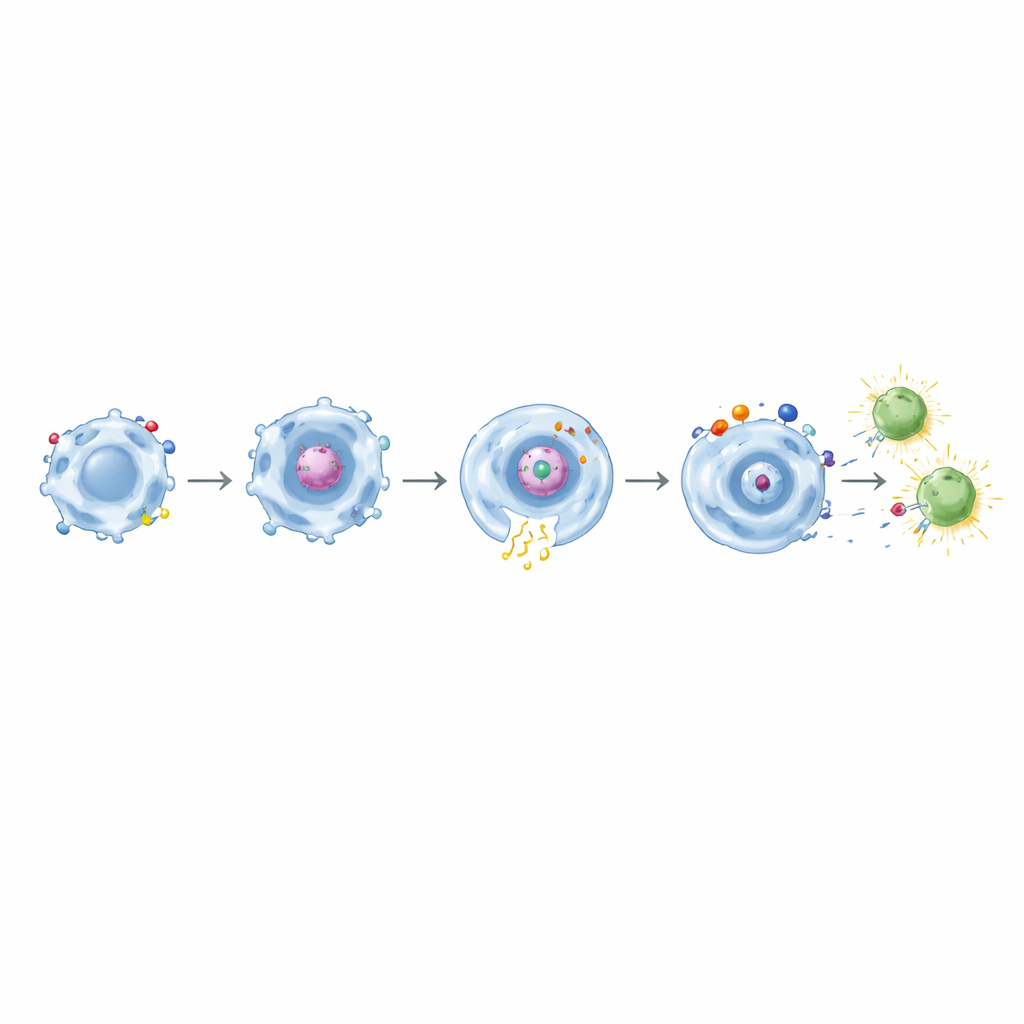
Od pożerania do uczenia limfocytów T
Co kluczowe, po tym jak makrofagi niosące CAR oparte na CD32a pochłonęły białko kolca, były w stanie aktywować komórki pamięci CD8 pochodzące od osób poprzednio zaszczepionych przeciw COVID‑19. Te limfocyty T uruchamiały wczesne markery aktywacji i produkowały molekuły efektorowe, takie jak interferon‑γ i TNF‑α. Efekt był jeszcze silniejszy przy CAR z podwójnymi domenami łączącymi CD32a z CD11b, CD18 lub TLR4. Gdy podobne projekty skierowane przeciw mesotelinie przetestowano przeciw komórkom nowotworowym inżynieryjnie modyfikowanym, ponownie wykazały precyzyjną, zależną od celu fagocytozę wraz z nasilonymi sygnałami zapalnymi. Spośród nich kombinacja CD32a+TLR4 wyróżniała się jako potężny „alarm tkankowy”, najskuteczniej zwiększając wydzielanie cytokin i ekspresję CD86 przy jednoczesnym utrzymaniu specyficznego pożerania komórek nowotworowych.
Co to może znaczyć dla przyszłych terapii
Dla laika to badanie pokazuje, że inżynieria makrofagów nie jest problemem jeden‑rozmiar‑dla‑wszystkich. Poprzez wymianę i łączenie wewnętrznych modułów sygnałowych naukowcy mogą kształtować komórki, które albo koncentrują się na efektywnym sprzątaniu chorych komórek, albo działają bardziej jak wzmacniacze odpornościowe, przekształcając supresyjne środowisko guza i rekrutując limfocyty T. CAR oparte na CD32a okazały się mocną podstawą takich projektów, przewyższając tradycyjne moduły limfocytów T w makrofagach i działając zarówno przeciw celom wirusowym, jak i nowotworowym. Choć wyniki pochodzą z modeli laboratoryjnych i będą musiały zostać potwierdzone w komórkach pierwotnych człowieka oraz w modelach zwierzęcych, dostarczają one planu działania dla następców terapii CAR‑makrofagowych, które mogą lepiej radzić sobie z guzami litymi i uporczywymi infekcjami, łącząc szybkie pochłanianie z precyzyjną aktywacją limfocytów T.
Cytowanie: Hong, J., Lee, S., Kim, Y. et al. Optimization of THP-1-CAR monocytes utilizing CD32a signaling phagocytosis for antigen-specific T cell activation. Sci Rep 16, 8175 (2026). https://doi.org/10.1038/s41598-026-39406-6
Słowa kluczowe: makrofagi CAR, sygnalizacja CD32a, fagocytoza, immunoterapia guzów litych, aktywacja limfocytów T