Clear Sky Science · pl
Pejzaż metylacji DNA u naturalnie krótkowiecznych killifish
Malutkie ryby z dużymi wskazówkami dotyczącymi starzenia
Dlaczego niektóre zwierzęta pędzą przez życie, podczas gdy inne trwają w nim przez lata? To badanie podejmuje tę zagadkę, wykorzystując roczne killifish — drobne afrykańskie ryby, które żyją zaledwie kilka miesięcy, a mimo to wykazują wiele tych samych objawów starzenia co ludzie. Mapując, jak chemiczne znaczniki na ich DNA zmieniają się w czasie, badacze pytają, czy te krótkowieczne ryby podążają za tymi samymi „epigenetycznymi” wzorcami starzenia obserwowanymi u ludzi i innych ssaków — oraz czy te wzorce mogłyby w przyszłości pomóc przewidywać zdrowie i długość życia w prostym modelu laboratoryjnym.
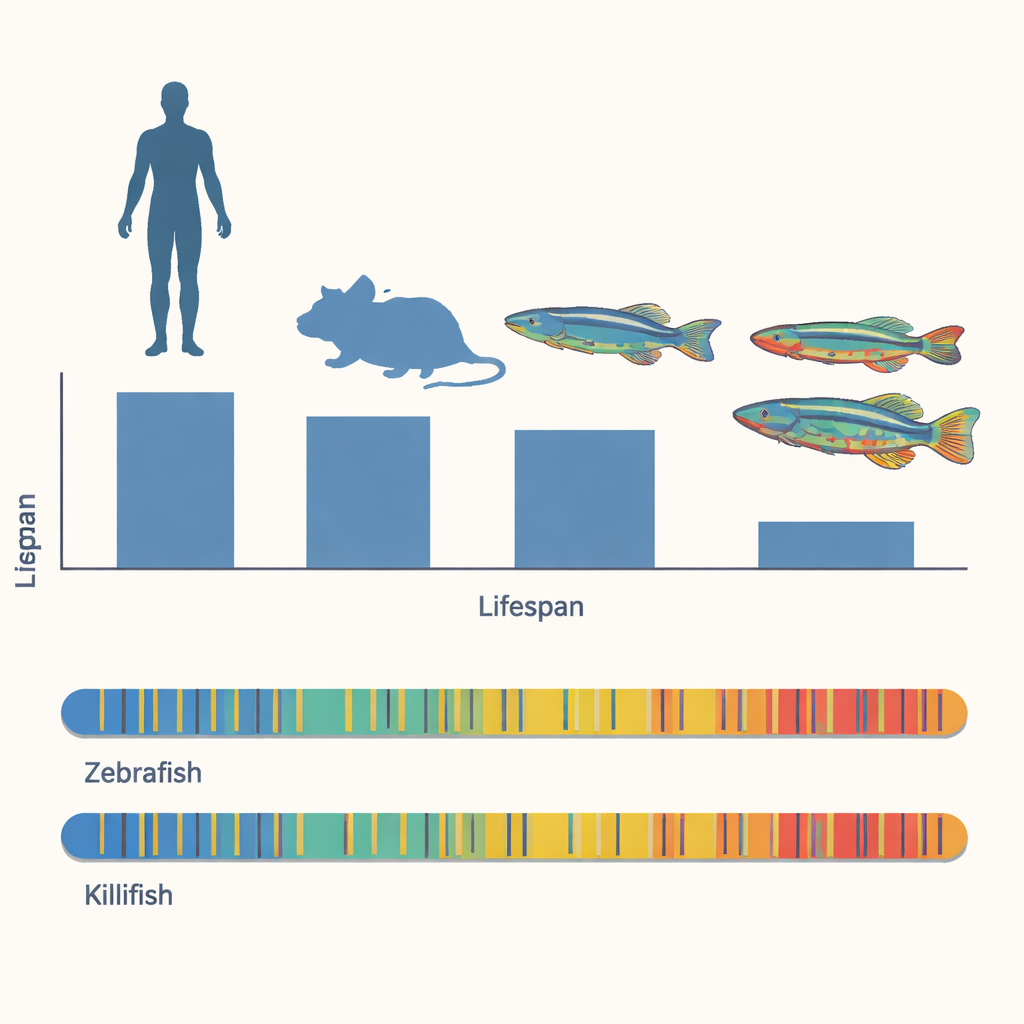
Krótkie życie w nieprzewidywalnym świecie
Ročne killifish wyewoluowały, aby przetrwać w tymczasowych kałużach, które pojawiają się w porze deszczowej i znikają krótko potem. Ich jaja czekają w suchej mule, a po powrocie wody wylęgają się i rosną w zadziwiającym tempie. Jedien gatunek, Nothobranchius furzeri, zwykle żyje tylko trzy do sześciu miesięcy; jego bliski krewny N. orthonotus może osiągnąć około dziesięciu miesięcy w podobnych warunkach. Oba gatunki rozwijają znajome oznaki starzenia — zmniejszoną płodność, wolniejsze pływanie, zmiany koloru skóry i oczu, problemy z pamięcią, osłabienie odporności, zaburzenia równowagi mikrobioty jelitowej oraz guzy. Ponieważ te zmiany rozwijają się w mniej niż rok, ryby te dają rzadką szansę na badanie biologii starzenia w przyspieszonym tempie.
Patrząc poza genetyczny plan
Badacze chcieli wiedzieć, czy szybkie starzenie killifish jest zapisane w strukturze ich genomu, czy raczej w sposobie, w jaki ten genom jest regulowany. Najpierw porównali podstawowe cechy genomu obu killifish z genomami ludzi, myszy, danio pręgowanego i nicienia C. elegans. Pomimo dramatycznie krótszych długości życia, genomy killifish są podobne pod względem wielkości i układu genów do danio. Obie ryby przeznaczają około połowy swojego DNA na sekwencje powtarzalne, w szczególności ruchome elementy genetyczne znane jako elementy transpozonowe, i wykazują porównywalny rozkład liter DNA, do których mogą przyłączać się grupy metylowe — chemiczne znaczniki będące przedmiotem badania. Te szerokie podobieństwa sugerują, że krótkie życie killifish nie może być wytłumaczone jedynie mniejszym lub bardziej zwartej budowy genomem.
Znaczniki DNA, które zmieniają się w zależności od tkanki i czasu
Aby badać regulację zamiast surowej sekwencji, zespół sporządził mapy metylacji DNA o wysokiej rozdzielczości — wzory przyłączenia grup metylowych do zasad cytozyny — w całych genomach obu gatunków. Analizowali mózg, wątrobę i serce młodych i starych N. furzeri oraz mózgi młodych, starych i bardzo starych N. orthonotus. Ogólnie pejzaż metylacji killifish przypominał ten u ssaków: większość miejsc była albo silnie oznaczona, albo prawie nieoznaczona, a obszary w pobliżu startu genów miały zazwyczaj mniej znaczników. Różnice między tkankami okazały się znacznie silniejsze niż różnice między wiekami. Mózg, wątroba i serce niosły odrębne sygnatury metylacyjne, a obszary o niskiej metylacji specyficzne dla mózgu często znajdowały się w pobliżu genów istotnych dla tożsamości komórek nerwowych, co sugeruje, że wzorce te pomagają definiować i utrzymywać funkcję każdego organu.
Subtelne odciski starzenia i ruchome DNA
Zmiany związane z wiekiem były obecne, lecz umiarkowane. W skali całego genomu poziomy metylacji pozostawały w dużej mierze stabilne wraz z wiekiem w obu gatunkach killifish. Jednak bliższa analiza ujawniła tysiące konkretnych regionów, w których metylacja zmieniała się między młodymi a starymi osobnikami. Wiele z tych zmian występowało w obrębie lub w pobliżu elementów transpozonowych — ruchomych sekwencji DNA, które stanowią dużą część genomu killifish. Różne tkanki wykazywały częściowo pokrywające się zestawy elementów wrażliwych na wiek, co sugeruje zarówno wspólne, jak i specyficzne dla organu efekty starzenia. W dłużej żyjącym N. orthonotus szczegółowe analizy mózgu ujawniły grupy miejsc metylacyjnych, których poziomy zmieniały się w sposób korelujący z wiekiem ryb, i te miejsca można było połączyć w model statystyczny, który w przybliżeniu przewidywał, czy osobnik był młody, stary czy bardzo stary.
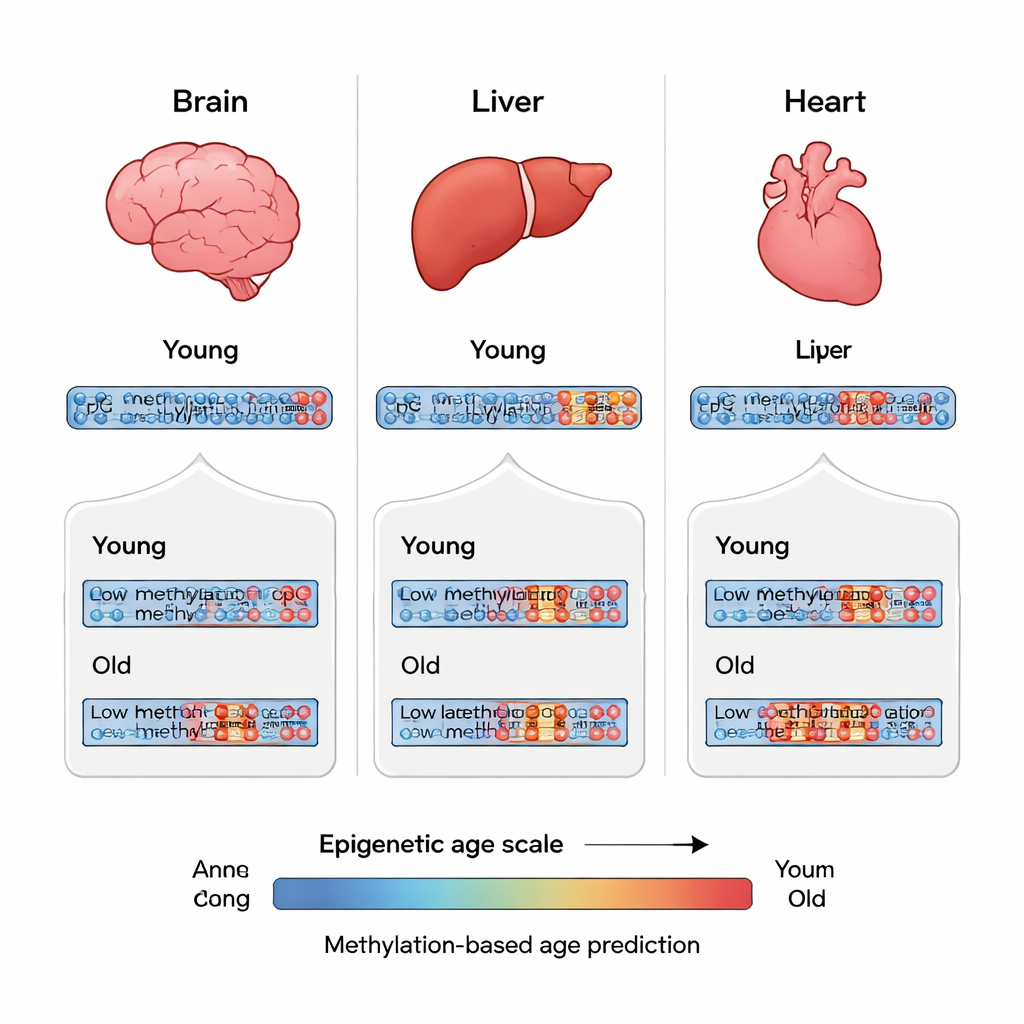
Co te malutkie ryby mówią nam o starzeniu
Badanie pokazuje, że nawet u kręgowca żyjącego zaledwie miesiące występują rozpoznawalne zmiany metylacji DNA wraz z wiekiem, podobne do tych wykorzystywanych do budowy „epigenetycznych zegarów” u ludzi i myszy. Jednak przesunięcia u killifish są stosunkowo niewielkie i rozproszone po wielu miejscach, zamiast skupiać się w kilku kluczowych szlakach. Może to odzwierciedlać skompresowaną długość życia tych ryb: jest mniej czasu na narastanie stopniowego dryfu epigenetycznego. Dostarczając pierwszych kompleksowych map metylacji dla rocznych killifish, praca ta tworzy niezbędne podstawy do przekształcenia tych zwierząt w szybki, elastyczny system do badania, jak geny, środowisko i potencjalne terapie wpływają na tempo biologicznego starzenia.
Cytowanie: Steiger, M., Singh, N., Tyers, A.M. et al. The DNA methylation landscape of naturally short-lived killifish. Sci Rep 16, 7173 (2026). https://doi.org/10.1038/s41598-026-39352-3
Słowa kluczowe: epigenetyczne starzenie się, metylacja DNA, killifish roczne, elementy transpozonowe, biologia długości życia