Clear Sky Science · pl
FAM120A - białko włączone w sieć choroby ALS
Dlaczego to ma znaczenie dla osób i rodzin
Stwardnienie zanikowe boczne (ALS) to wyniszczająca choroba, która stopniowo prowadzi do paraliżu przez obumieranie komórek nerwowych kontrolujących ruch. Nadal w pełni nie rozumiemy, dlaczego te neurony ruchowe umierają, a skuteczne terapie są wciąż rzadkie. To badanie rzuca światło na mało znane białko o nazwie FAM120A i sugeruje, że może ono pomagać komórkom nerwowym radzić sobie ze stresem oraz zapobiegać gromadzeniu się szkodliwych grudek białkowych — cechy charakterystycznej dla ALS. Odkrywając, jak to białko zachowuje się w przebiegu choroby, praca otwiera nową ścieżkę do zrozumienia, a być może w przyszłości leczenia ALS.
Odnalezienie ukrytego uczestnika w zatłoczonej sieci genów
Naukowcy zaczęli nie przy ławce laboratoryjnej, lecz przy komputerze. Zastosowali podejście „analizy konwergentnej”, łącząc wiele istniejących zestawów danych o genach powiązanych z ALS i ich interakcjach. Widok sieciowy pozwolił im zidentyfikować klastry białek działających wspólnie w kluczowych procesach komórkowych, zwłaszcza tych związanych z obróbką RNA i kontrolą jakości białek — obszarami znanymi z problemów w ALS. W jednym z takich klastrów FAM120A wyłoniło się jako wcześniej pomijane, lecz silnie powiązane białko, które wchodzi w interakcje z kilkoma ustalonymi białkami związanymi z ALS. Jego znane role w pomaganiu komórkom przetrwać stres oksydacyjny i w zarządzaniu RNA uczyniły z niego silnego kandydata do dalszych badań.
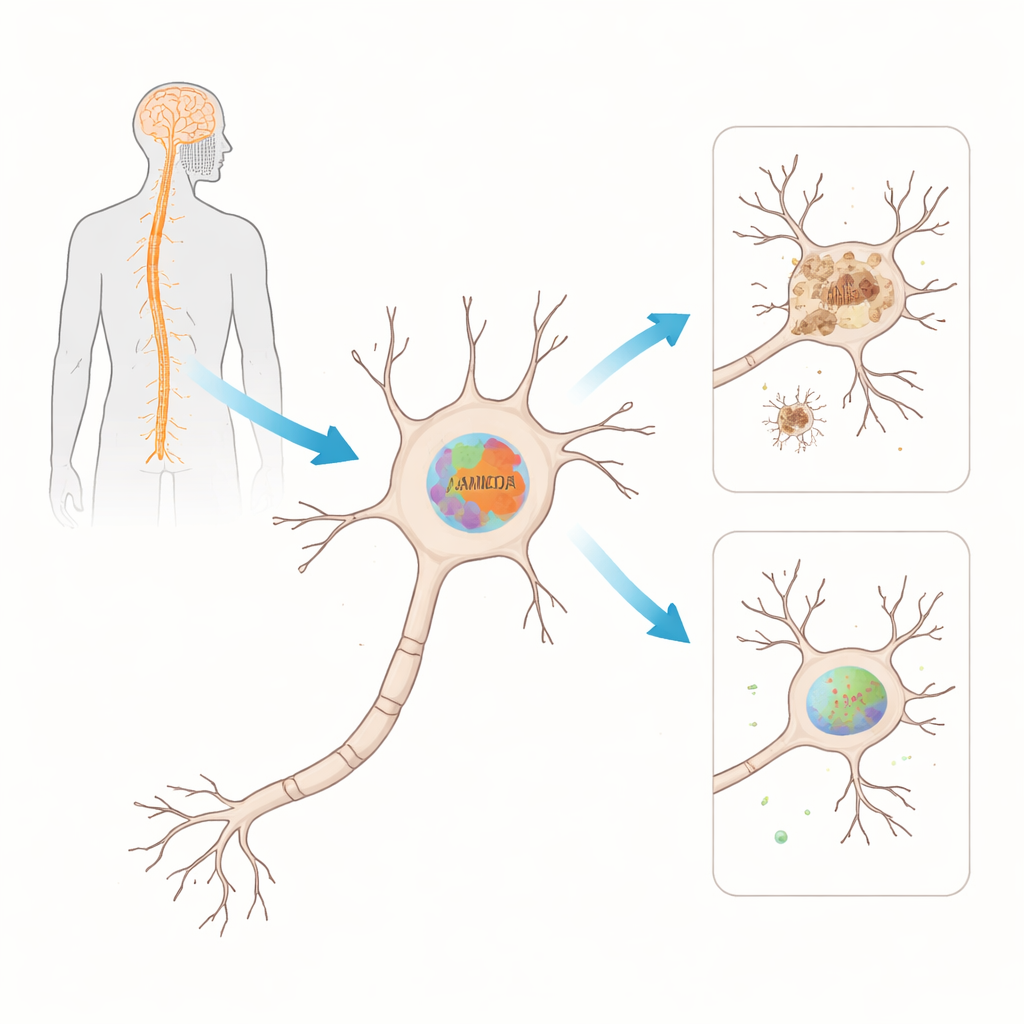
Śledzenie wrażliwego białka w trakcie postępu choroby
Aby sprawdzić, czy FAM120A rzeczywiście ma znaczenie w ALS, zespół sięgnął po szeroko stosowany model myszy niosący zmutowaną wersję genu SOD1, jedną z pierwszych zidentyfikowanych przyczyn genetycznych ALS. Mierzyli zarówno komunikaty RNA, jak i poziomy białka mysiej wersji, Fam120A, w rdzeniu kręgowym w różnych momentach — od okresu przedobjawowego po późne stadium choroby. Na wczesnym etapie poziomy RNA Fam120A spadały w rdzeniu kręgowym, zanim u zwierząt pojawiły się wyraźne objawy. Później, w miarę rozwoju paraliżu, samo białko Fam120A było wyraźnie zredukowane. Ta rozbieżność — najpierw zmiana RNA, potem białka — sugeruje, że wraz z postępem choroby zawodzą różne poziomy regulacji.
Gdzie w rdzeniu kręgowym występuje to białko
Następnie naukowcy sprawdzili, gdzie dokładnie Fam120A znajduje się w rdzeniu kręgowym. Przy użyciu mikroskopii fluorescencyjnej na przekrojach tkanki zaobserwowali, że Fam120A występuje głównie w neuronach rogu brzusznego — obszarze bogatym w neurony ruchowe, które degenerują w ALS. W późnym stadium choroby u zwierząt zauważono pewien sygnał w komórkach wspierających zwanych astrocytami, ale dominujący wzór pozostawał neuronalny. Te obserwacje łączą Fam120A bezpośrednio z tymi komórkami, które zawodzą w ALS, i wspierają tezę, że jego utrata może osłabiać ich zdolność do radzenia sobie ze stresem komórkowym, co może przyczyniać się do pogorszenia funkcji ruchowych.
Wykorzystanie nadmiaru FAM120A w komórkach przypominających nerwowe
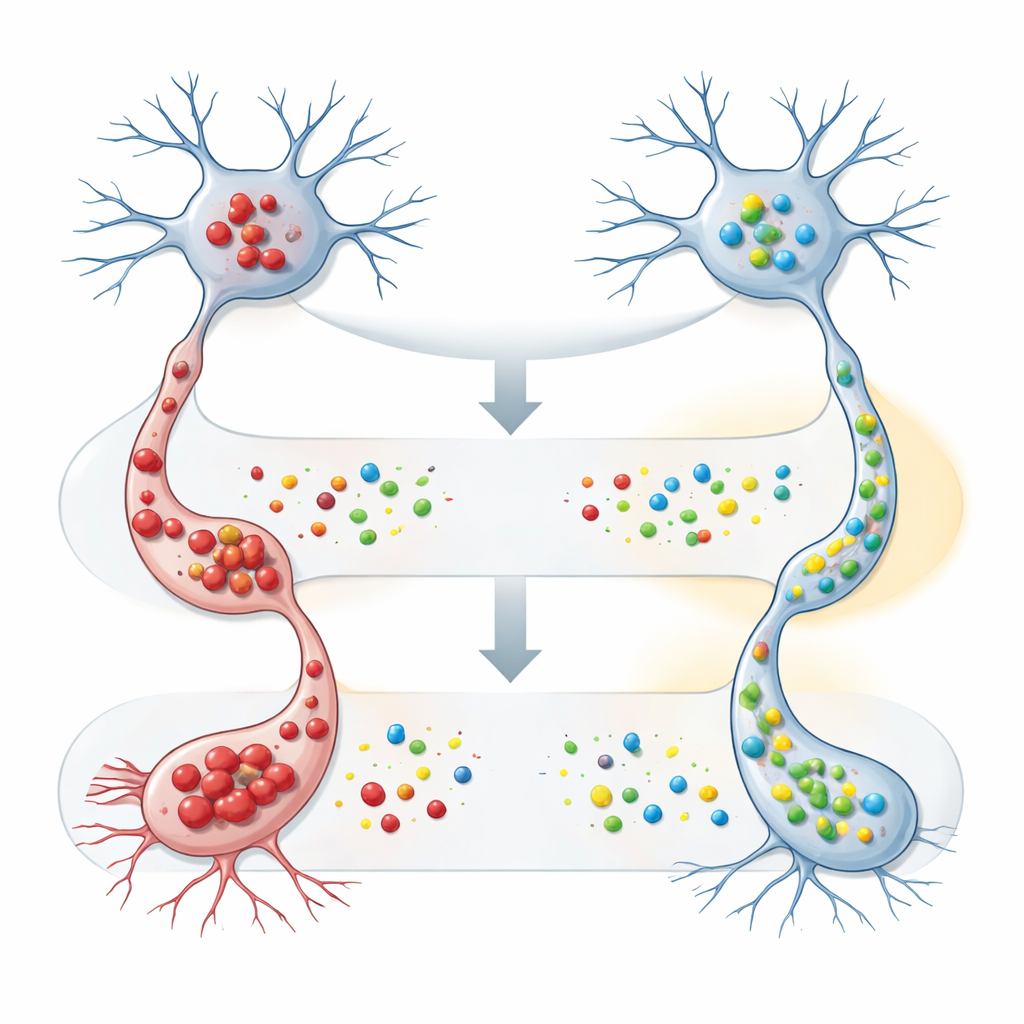
Zespół następnie przeszedł do hodowanych komórek przypominających neurony, by zbadać, co FAM120A robi w praktyce. Zmodyfikowali te komórki tak, by produkowały albo prawidłową, albo mutantową wersję SOD1, która ma skłonność do tworzenia toksycznych agregatów, a potem wymusili nadprodukcję ludzkiego FAM120A. W obecności zmutowanego SOD1 zwiększenie poziomu FAM120A znacząco zmniejszyło zarówno ilość nierozpuszczalnego SOD1 wykrywanego testami biochemicznymi, jak i liczbę widocznych agregatów pod mikroskopem. Co ważne, FAM120A miało niewielki wpływ na normalną formę SOD1, co sugeruje, że może specyficznie pomagać komórkom radzić sobie z nieprawidłowo sfałdowanymi lub mającymi tendencję do agregacji białkami — zasadniczym problemem w ALS i innych chorobach neurodegeneracyjnych.
Budowanie szerszej mapy molekularnych sprzymierzeńców i wrogów
Poza tymi eksperymentami badacze zbadali szerszą sieć interakcji FAM120A. Potwierdzili, że fizycznie łączy się ona z PURA, białkiem wiążącym RNA już powiązanym z rozwojem mózgu i neurodegeneracją, i odkryli, że poziomy PURA również spadają w rdzeniu kręgowym mysiego modelu ALS, choć później w przebiegu choroby. Zwracają uwagę na dodatkowe powiązania między FAM120A, jej genem antysensownym FAM120Aos oraz innym białkiem wiążącym RNA, ELAVL1, które reguluje geny związane z zapaleniem i reakcją na stres w mózgu. Ta rozwijająca się sieć powiązań lokuje FAM120A na skrzyżowaniu regulacji RNA, reakcji na stres i kontroli jakości białek — dokładnie tych systemów, które zawodzą w ALS.
Co to może oznaczać dla przyszłych terapii ALS
Podsumowując, wyniki sugerują, że FAM120A nie jest jedynie biernym obserwatorem, lecz istotnym elementem sieci choroby ALS. Jego wczesny spadek w wrażliwych neuronach ruchowych, fizyczne powiązania z innymi białkami regulującymi RNA oraz zdolność do zmniejszania toksycznych grudek SOD1 w komórkach wskazują na rolę ochronną w utrzymaniu równowagi białkowej. Chociaż wciąż pozostaje dużo pracy — zwłaszcza by ustalić, czy podobne zmiany zachodzą u osób z ALS i w innych modelach choroby — FAM120A wyróżnia się teraz jako obiecujący cel dalszych badań i potencjalnie terapii mających na celu zachowanie zdrowia neuronów ruchowych.
Cytowanie: Vicencio, E., Gomez, L., Beltran, S. et al. FAM120A - a protein inserted in the ALS disease network. Sci Rep 16, 8200 (2026). https://doi.org/10.1038/s41598-026-39329-2
Słowa kluczowe: stwardnienie zanikowe boczne, neurony ruchowe, agregacja białek, białka wiążące RNA, neurodegeneracja