Clear Sky Science · pl
Mikrobiologiczne i reologiczne dynamiki mieszanych biofilmów tworzonych przez bakterie i wirus eukariotyczny
Ukryte społeczności na urządzeniach szpitalnych
Wiele zakażeń szpitalnych nie zaczyna się od pojedynczego zarazka, lecz od śliskich, niewidocznych społeczności zwanych biofilmami, które pokrywają cewniki i inne urządzenia medyczne. W badaniu postawiono często pomijane pytanie o dużych konsekwencjach dla bezpieczeństwa pacjentów: co się dzieje, gdy do biofilmów wchodzą razem nie tylko bakterie, lecz także wirusy zakażające ludzi? Obserwując zachowanie typowego wirusa ssaków we wnętrzu bakteryjnych biofilmów, badacze ujawniają, w jaki sposób te lepkie mikrobiologiczne „miasta” mogą potajemnie chronić wirusy i zmieniać ich zachowanie.
Lepkie miasta mikrobów
Biofilmy przypominają mikroskopijne miasta budowane przez mikroby na wilgotnych powierzchniach — rurach, skałach, zębach czy plastikowych rurkach umieszczanych u pacjentów. Bakterie osiadają, mnożą się i wydzielają klejącą matrycę, która chroni je przed wysychaniem, chemikaliami i układem odpornościowym. W szpitalach takie biofilmy często tworzą się na cewnikach moczowych i dożylnych, gdzie mogą zapoczątkować zakażenia krwi i dróg moczowych trudne do leczenia. Biofilmy zwykle zawierają wiele gatunków, a nawet różne królestwa życia, jednak większość badań koncentrowała się wyłącznie na bakteriach, pozostawiając rolę wirusów w dużej mierze niezbadaną.
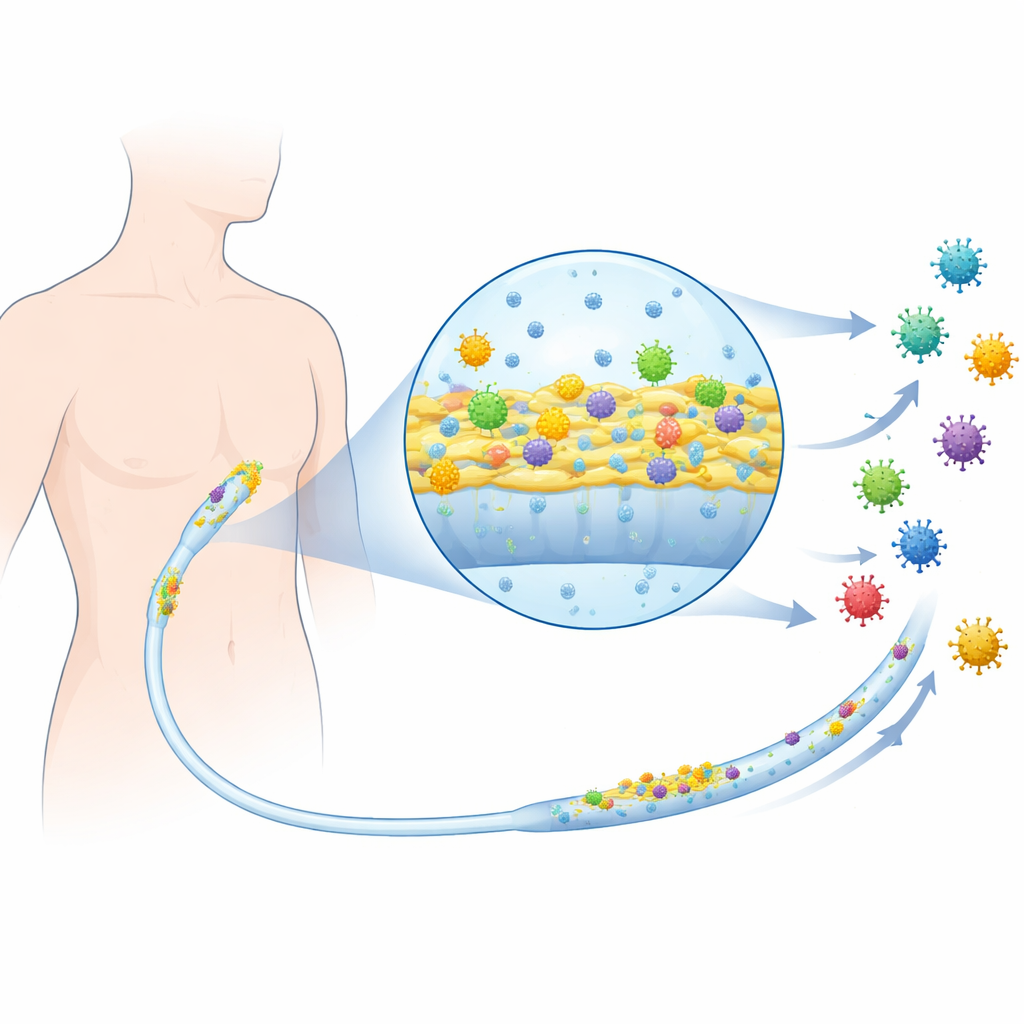
Wprowadzenie wirusa ssaków do układu
Zespół pracował z klinicznymi szczepami bakterii znanymi z kolonizowania cewników, w tym uropatogennym Escherichia coli z zakażeń dróg moczowych oraz innymi bakteriami często występującymi w zakażeniach związanych z centralnymi wkłuciami. Następnie wprowadzili reowirus ssaków, dobrze przebadany wirus nieotoczkowy infekujący komórki zwierzęce, jako model ogólniejszych wirusów zakażających ludzi. Najpierw sprawdzili, czy dodanie materiału zawierającego wirusa wpływa na normalny, wolno pływający wzrost bakterii. W wielu szczepach bakterie rosły i przeżywały równie dobrze zarówno z wirusem, jak i bez niego, co wskazuje, że wirus nie zabijał bezpośrednio bakterii ani nie działał jak antybiotyk.
Biofilmy zmieniają „dotyk”, nie rozmiar
Gdy bakterie osiadały w biofilmach, obraz stał się bardziej zniuansowany. W większości szczepów całkowita ilość biofilmu — mierzona standardowym barwieniem, które kwantyfikuje, ile materiału pokrywa powierzchnię — niewiele się zmieniała w obecności wirusa. Kilka szczepów wytwarzało jednak nieco więcej lub mniej biofilmu w zależności od tego, czy preparaty wirusowe były obecne, co sugeruje efekty specyficzne dla szczepu. Aby pójść dalej niż prosta ilość, badacze zapożyczyli narzędzia z nauki o materiałach i zmierzyli, jak „miękki” lub „sztywny” jest każdy biofilm, podobnie jak badanie tekstury żelu. Okazało się, że każdy szczep bakteryjny tworzył własne mechaniczne „odciski palców”. Co ważne, dodanie wirusa mogło albo usztywnić, albo zmiękczyć te biofilmy w zależności od szczepu: w jednym szczepie E. coli wirus uczynił matrycę bardziej sztywną, podczas gdy w szczepie Staphylococcus epidermidis wirus prowadził do słabszej, bardziej podatnej struktury.
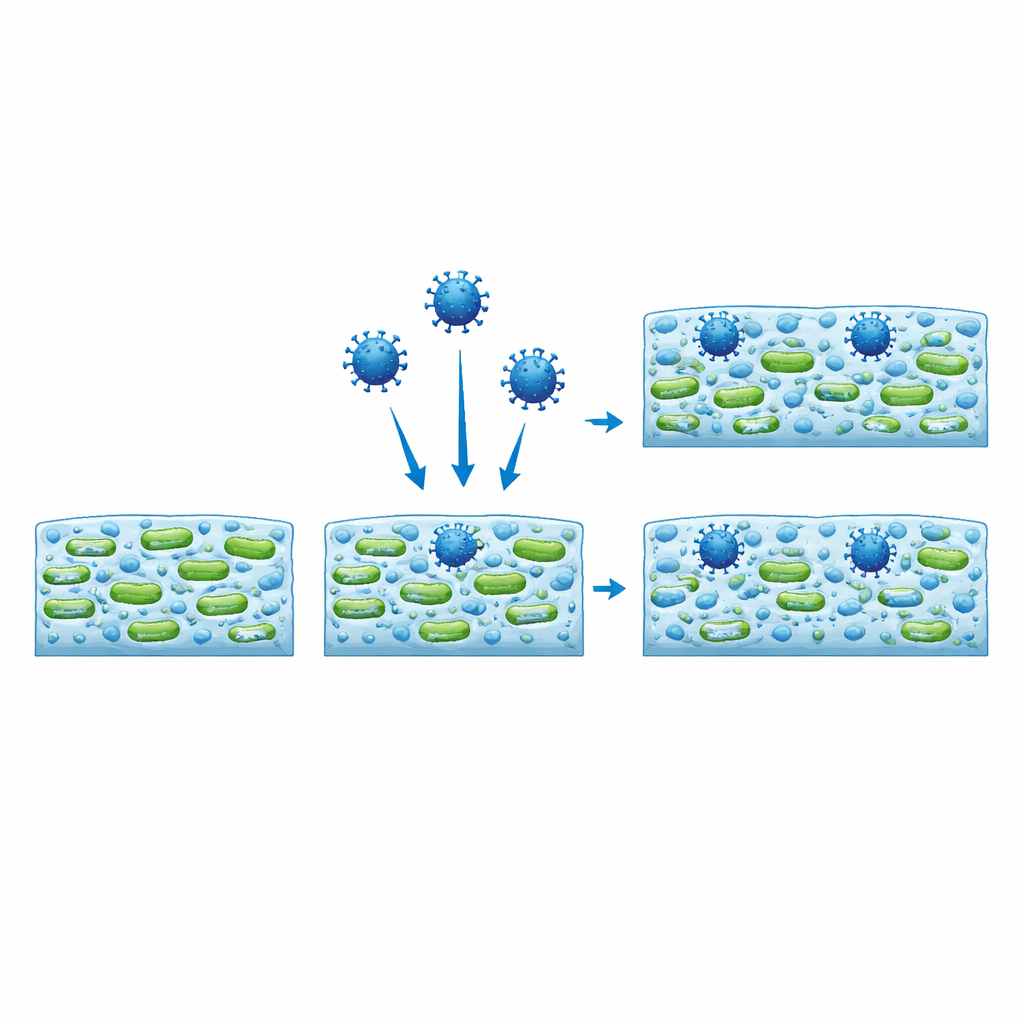
Wirusy znajdują schronienie i zachowują zjadliwość
Używając mikroskopii fluorescencyjnej, naukowcy znakowali cząstki wirusa, by świeciły, i śledzili, gdzie się znajdowały wewnątrz biofilmu. W przeciwieństwie do obojętnych, podobnych rozmiarów plastikowych kulek, które głównie pozostawały w rzadkich obszarach i były wypłukiwane, wirusy penetrowały głęboko w matrycę i miały tendencję do skupiania się tam, gdzie komórek bakteryjnych było najwięcej. W niektórych przypadkach obecność wirusa zmieniała nawet ogólny kształt biofilmu, przekształcając zwarte skupiska w bardziej sieciowe struktury lub odwrotnie, ponownie w zależności od szczepu bakterii. Aby sprawdzić, czy te uwięzione wirusy nadal są groźne, autorzy odzyskali je z biofilmów i wystawili na działanie komórek ssaków. Odkryte wirusy pozostały zakaźne, mimo że były osadzone w bakteryjnym śluzie przez dwa dni.
Dlaczego to ma znaczenie dla pacjentów i nie tylko
Dla laika kluczowy wniosek jest taki: biofilmy na urządzeniach medycznych mogą nie tylko chronić bakterie przed leczeniem — mogą także ukrywać i zachowywać wirusy infekujące komórki ludzkie lub zwierzęce. Badanie pokazuje, że wirusy mogą osadzać się w bakteryjnej matrycy, subtelnie zmieniając strukturę biofilmu, jednocześnie pozostając w pełni zdolne do zakażania nowych komórek po uwolnieniu. To sugeruje, że cewniki i inne powierzchnie pokryte biofilmami mogą stanowić ciche rezerwuaru, w których wirusy utrzymują się, chronione przed wysychaniem, środkami dezynfekującymi i atakiem układu odpornościowego. Zrozumienie tych mieszanych społeczności mikrobiologicznych może być kluczowe do projektowania lepszych materiałów, strategii czyszczenia i terapii celujących zarówno w partnerów bakteryjnych, jak i wirusowych, aby ograniczyć uporczywe zakażenia związane z urządzeniami.
Cytowanie: Gao, J., Abriat, C., Laekas-Hameder, M. et al. Microbiological and rheological dynamics of mixed biofilms formed by bacteria and eukaryotic virus. Sci Rep 16, 8315 (2026). https://doi.org/10.1038/s41598-026-39314-9
Słowa kluczowe: biofilmy, zakażenia cewnikowe, interakcje wirus–bakteria, reowirus, społeczności mikrobiologiczne