Clear Sky Science · pl
Ramowy model integracyjny wykrywania raka za pomocą równań całkowo‑różniczkowych i technik głębokiego uczenia
Dlaczego inteligentniejsze skany mają znaczenie
Wczesne wykrycie raka może uratować życie, ale odczytywanie badań obrazowych, takich jak mammogramy, jest trudne, czasochłonne i podatne na błędy ludzkie. Lekarze muszą rozróżnić słabe wzorce choroby od normalnej tkanki i szumów obrazu, często pod silną presją czasu. W artykule przedstawiono nowe podejście, które pomaga w tym zadaniu: przekształca złożone obrazy piersi w prostsze jednowymiarowe sygnały, a następnie wykorzystuje zarówno narzędzia matematyczne, jak i sztuczną inteligencję, aby ocenić prawdopodobieństwo obecności raka. Celem nie jest zastąpienie lekarzy, lecz dostarczenie im jaśniejszych i bardziej wiarygodnych wskazówek ukrytych w każdym skanie.
Przekształcanie obrazów w sygnały
Autorzy zaczynają od przemyślenia reprezentacji obrazu medycznego. Zamiast traktować mammogram jako ogromną siatkę pikseli, konwertują go na jedną liniopodobną reprezentację, która podsumowuje zmiany jasności w obrębie piersi. Najpierw obraz jest oczyszczany: przekształcany do odcieni szarości, odszumiany i wyrównywany pod względem intensywności, aby ciemne i jasne rejony były porównywalne. Krawędzie i tekstury są uwypuklane przy użyciu standardowych filtrów, a ogólny rozkład jasności analizowany jest w kategoriach częstotliwości (podobnie jak rozkład dźwięku na bas i soprany). Następnie wartości pikseli są uśredniane wiersz po wierszu lub kolumna po kolumnie, aby uzyskać gładką krzywą jednowymiarową. Szczyty tej krzywej odzwierciedlają gęstą tkankę lub podejrzane obszary; doliny - obszary mniej wypełnione. Chociaż pewne drobne detale zostają utracone, wynikowy sygnał jest kompaktowy i zachowuje szerokie struktury istotne dla diagnozy. 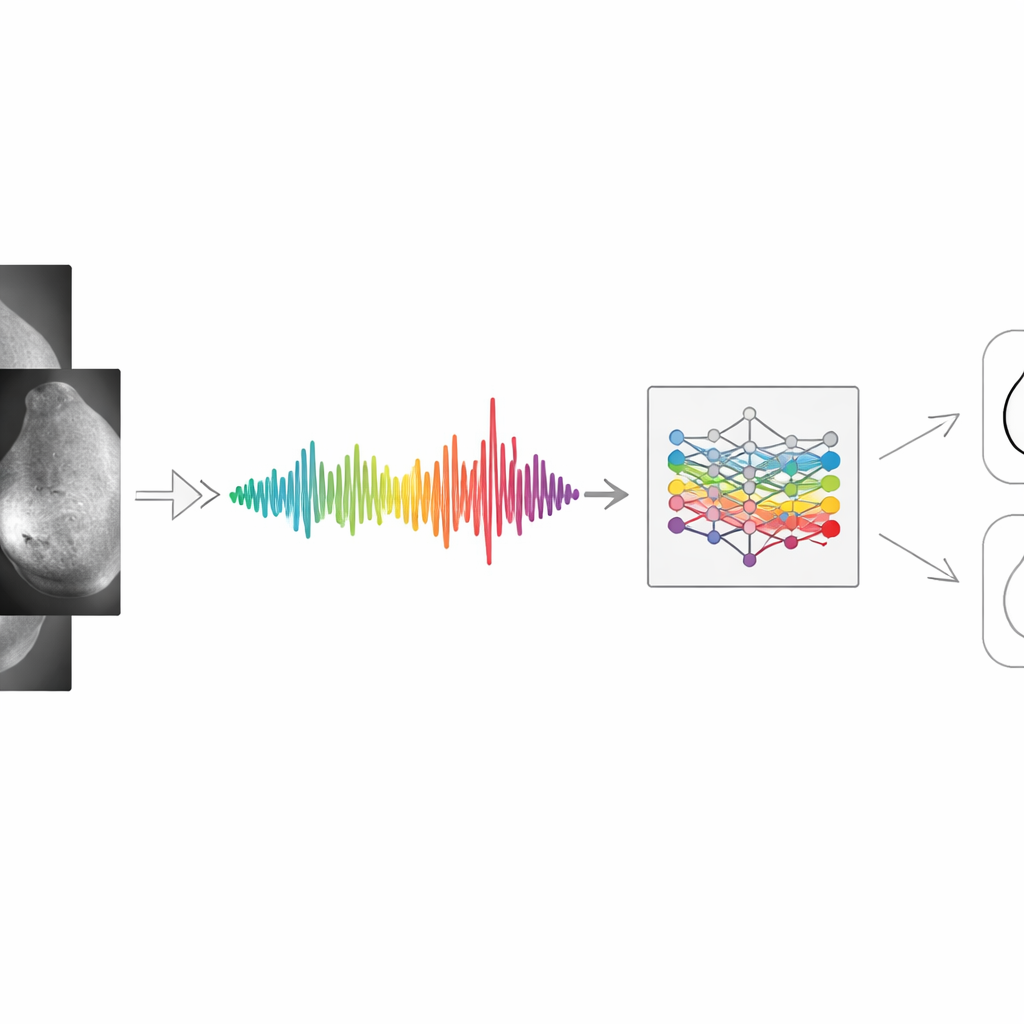
Dodanie warstwy biologii za pomocą równań
Wiele obecnych systemów głębokiego uczenia działa bezpośrednio na obrazach i bywa krytykowanych jako „czarne skrzynki”, które niewiele wyjaśniają na temat faktycznego zachowania guzów. Aby temu zaradzić, autorzy osadzają w swoim potoku sygnałowym modele matematyczne wzrostu guza. Wykorzystują równania całkowo‑różniczkowe — równania opisujące, jak coś zmienia się w czasie, jednocześnie uwzględniając wpływ przeszłości — aby naśladować rozmnażanie się komórek nowotworowych, ich rozprzestrzenianie i tworzenie układu naczyniowego. Równania te zawierają terminy odpowiadające za tempo wzrostu, ograniczenia związane z zagęszczeniem, ruch komórek oraz formowanie nowych naczyń. Symulując, jak guz może ewoluować i wpływać na rozkład jasności na mammogramie, ramowy model generuje dodatkowe cechy oparte na znanej biologii, a nie jedynie na rozpoznawaniu wzorców. Tak wzbogacone sygnały mają uczynić końcowe prognozy bardziej zrozumiałymi dla klinicystów.
Nauka kompaktowej sieci neuronowej do podejmowania decyzji
Gdy obraz zostanie przekształcony w matematycznie wzbogacony sygnał, uproszczona jednowymiarowa konwolucyjna sieć neuronowa (CNN) przeprowadza faktyczną klasyfikację. Sieć przesuwa małe filtry wzdłuż sygnału, aby wykrywać istotne kształty — ostre skoki, płynne narastania czy powtarzalne fale — które mogą wskazywać na tkankę nieprawidłową. Model trenuje się na publicznie dostępnych zestawach mammograficznych (INbreast i MIAS), dzieląc dane na zestawy treningowe, walidacyjne i testowe, aby zapobiec przeuczeniu. Autorzy stosują też augmentację sygnałów i starannie dobierają parametry modelu, by poprawić jego odporność. Aby dodatkowo rozjaśnić działanie „czarnej skrzynki”, stosują narzędzia wyjaśnialności, które wskazują, które fragmenty sygnału najbardziej wpłynęły na decyzję, łącząc je z obszarami oryginalnego obrazu piersi, gdzie zmiany gęstości tkanki lub granic były podejrzane. 
Jak to sprawdza się w praktyce
W testach na tych rzeczywistych zbiorach mammogramów ramowy model poprawnie rozróżniał przypadki z rakiem od niezłośliwych w około 96,4% przypadków, przewyższając standardowe sieci CNN, maszyny wektorów nośnych, drzewa decyzyjne oraz kilka współczesnych bazowych modeli głębokiego uczenia. System wykazał też wysoką czułość, co oznacza, że większość nowotworów została prawidłowo wykryta, oraz silną swoistość, czyli mniejsze ryzyko błędnego oznaczenia zdrowych pacjentów. Ponieważ system działa na sygnałach 1D zamiast pełnych obrazów, wymaga mniej pamięci i potrafi generować prognozy szybciej niż wiele ciężkich sieci obrazowych, co ma znaczenie w zatłoczonych klinikach lub na skromniejszym sprzęcie. Dodatkowe modelowanie matematyczne wydaje się wyostrzać istotne cechy, poprawiając dokładność bez ogromnych kosztów obliczeniowych.
Dokąd to może prowadzić
Autorzy konkludują, że połączenie konwersji obrazu w sygnał, modeli matematycznych wzrostu guza oraz głębokiego uczenia oferuje obiecującą drogę do bardziej dokładnych i zrozumiałych narzędzi przesiewowych w kierunku raka. Ich podejście jest wciąż we wczesnej fazie: zostało zwalidowane głównie na obrazach piersi, a podczas konwersji sygnałowej mogą zostać utracone niektóre drobne detale wizualne. Przyszłe prace przetestują metodę na innych nowotworach, dodadzą bogatsze formy wyjaśnień dla lekarzy oraz zintegrują dodatkowe dane, takie jak preparaty tkankowe, markery kliniczne i informacje genetyczne. Po szerszej walidacji tego rodzaju matematycznie ugruntowana AI mogłaby w końcu wspierać systemy decyzji w czasie rzeczywistym, pomagając radiologom wykrywać nowotwory wcześniej i z większą pewnością.
Cytowanie: Gopisairam, T., Thota, S. & Bikku, T. Integrative framework for cancer detection via integro-differential equations using deep learning techniques. Sci Rep 16, 9714 (2026). https://doi.org/10.1038/s41598-026-39283-z
Słowa kluczowe: wykrywanie raka, obrazowanie medyczne, głębokie uczenie, modelowanie matematyczne, mammografia piersi