Clear Sky Science · pl
Model fizyki polimerów jądra komórkowego interfazy do symulacji radiobiologicznych
Dlaczego kształt „domu” naszego DNA ma znaczenie
Promieniowanie to miecz obosieczny w medycynie: może zabijać komórki nowotworowe, ale też uszkadzać tkanki zdrowe. U podstaw zarówno ryzyka, jak i korzyści leży nasze DNA, ciasno upakowane wewnątrz jądra komórkowego. W pracy tej pokazano, jak szczegółowy, inspirowany fizyką model 3D tej „metropolii DNA” może pomóc naukowcom przewidywać, w jaki sposób promieniowanie powoduje pęknięcia i nieprawidłowe reperacje chromosomów, co może poprawić leczenie raka i oszacowania ryzyka związanego z promieniowaniem w przestrzeni kosmicznej.
Postrzeganie genomu jako struktury żywej
W każdej komórce człowieka dwa metry DNA są złożone do niewielkiego jądra o wielkości kilku mikrometrów. To składanie nie jest przypadkowe: każdy chromosom zwykle zajmuje własne terytorium, dalej podzielone na sąsiedztwa i domeny pętelkowe. Nowe narzędzia eksperymentalne, takie jak mikroskopia nadrozdzielcza i mapy kontaktów Hi-C, ujawniły tę złożoną trójwymiarową organizację w niezwykłych szczegółach. Mimo to większość modeli promieniowania nadal traktuje DNA jako uproszczone sploty linii lub idealizowane pętle, pomijając tę wyższą organizację. Autorzy postawili sobie za cel zbudowanie modelu całego jądra, który respektuje to, co biolodzy poznali o rzeczywistej architekturze chromatyny, a jednocześnie jest wystarczająco szybki, by działać na zwykłych komputerach laboratoryjnych.
Budowa wirtualnego jądra z użyciem fizyki polimerów
Zespół zamodelował chromosomy jako elastyczne łańcuchy, zapożyczając pomysły z fizyki polimerów — tej samej dziedziny, która wyjaśnia zachowanie tworzyw sztucznych i materiałów miękkich. Podzielili problem na trzy etapy relaksacji, by okiełznać ogromne koszty obliczeniowe. Najpierw rozmieścili duże bloki budulcowe zwane domenami chromatyny w całym jądrze, pozwalając im się wzajemnie odpychać, rozciągać wzdłuż długości i grupować w szersze podkompartmenty. Po drugie, przyjrzeli się zbliżeniu w każdej domenie, aby rozwinąć drobniejsze włókna chromatyny, w tym regiony pętlowe utrzymywane przez białka wiążące. Po trzecie, ponownie pozwolili wszystkim włóknom swobodnie oddziaływać wewnątrz granic jądra, dążąc do realistycznej końcowej konfiguracji. Dzięki takiemu podziałowi procesu oraz zastosowaniu hierarchicznego wyszukiwania i trików obliczeń równoległych skrócili czas działania z niepraktycznych czterech miesięcy do około trzech godzin na jedno wirtualne jądro na stacji roboczej 64-rdzeniowej.
Od torów promieniowania do złamań i napraw DNA
Gdy wirtualne jądro było gotowe, autorzy nałożyli szczegółowe tory promieniowania wygenerowane przez symulacje Geant4-DNA. Użyli hierarchicznego wyszukiwania, aby dla każdego zdarzenia jonizacji odnaleźć, która domena chromatyny, segment włókna, a wreszcie który nukleotyd był najbliżej, bez konieczności przechowywania wszystkich dziesięciu miliardów pozycji nukleotydów w pamięci. Zamiast tego trzymali wielokrotnego użytku szablon chromatyny i stosowali sprytne transformacje współrzędnych „w locie”. Jonizacje w szkielecie DNA traktowano jako złamania nici, a sąsiadujące złamania na przeciwległych nićach uznawano za podwójne złamania. Aby naśladować mechanizmy naprawcze komórki, autorzy wprowadzili regułę ponownego łączenia opartą na odległości: wolne końce DNA, które leżą blisko siebie, mają większe prawdopodobieństwo ponownego połączenia. Decyzje o łączeniu podejmowano krok po kroku, aż wszystkie końce były albo sparowane, albo pozostawione nieodtworzone, odtwarzając zarówno prawidłowe naprawy, jak i błędne połączenia fragmentów.
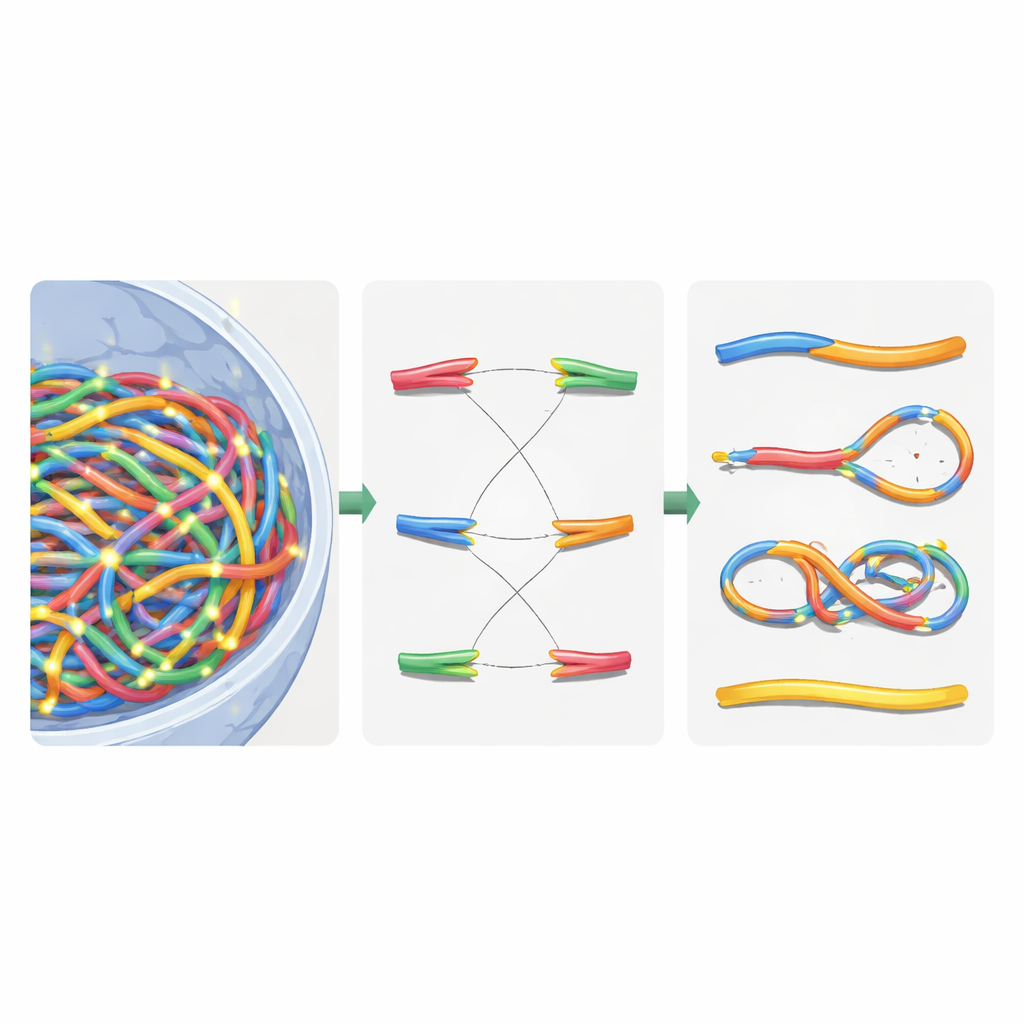
Sortowanie złamanych chromosomów za pomocą logiki sieciowej
Po tej wirtualnej naprawie jądro zawierało mieszaninę zrekonstruowanych chromosomów i pozostałych fragmentów. Aby sklasyfikować zaistniałe zmiany, autorzy przetłumaczyli naprawiony genom na graf nieukierunkowany: segmenty chromosomów stały się krawędziami, a ich końce i miejsca złamań — węzłami. Przy użyciu standardnego algorytmu znajdowania składowych spójnych mogli automatycznie odtworzyć każdy nowy obiekt przypominający chromosom i policzyć kluczowe cechy, takie jak liczba centromerów (miejsca przyczepu podczas podziału komórki) i telomerów (naturalnych końców). Na tej podstawie zidentyfikowali dikentryki (chromosomy z dwoma centromerami), pierścienie i delecje. Następnie porównali swoje symulacje z klasycznymi eksperymentami na ludzkich komórkach skóry narażonych na promieniowanie gamma i cząstki alfa, wykazując, że całkowite aberracje chromosomowe zostały odtworzone w przybliżeniu w granicach 20% wartości zmierzonych — istotna poprawa w stosunku do wcześniejszych modeli.
Co to oznacza dla pacjentów i astronautów
Mówiąc najprościej, praca ta pokazuje, że „gdzie” DNA znajduje się w jądrze i „jak” się składa, silnie wpływa na to, jak uszkodzenia promieniowaniem kumulują się do niebezpiecznych zmian chromosomowych. Łącząc realistyczną trójwymiarową architekturę genomu, wydajną symulację opartą na fizyce i grafowy sposób odczytu złamanych chromosomów, autorzy stworzyli potężny most między biologią strukturalną a radiobiologią. Twierdzą, że przyszłe udoskonalenia — takie jak dodanie szczegółowego czasu naprawy i wykorzystanie danych z sekwencjonowania całego genomu — mogłyby uczynić to podejście jeszcze lepszym w przewidywaniu biologicznych skutków wysokoenergetycznych cząstek stosowanych w terapii nowotworów lub spotykanych w głębokiej przestrzeni kosmicznej. Ostatecznie lepsze modele „domu” DNA w naszych komórkach mogą pomóc dopasować bezpieczniejsze i bardziej skuteczne terapie radiacyjne oraz ulepszyć nasze rozumienie długoterminowych ryzyk związanych z promieniowaniem.
Cytowanie: Zhao, M., Huang, G., Xu, Z. et al. A polymer physics model of the interphase cell nucleus for radiobiological simulations. Sci Rep 16, 7913 (2026). https://doi.org/10.1038/s41598-026-39234-8
Słowa kluczowe: uszkodzenia DNA wywołane promieniowaniem, 3D architektura chromatyny, aberacje chromosomowe, modelowanie fizyki polimerów, terapia cząstkami