Clear Sky Science · pl
Aktywacja transkrypcyjna PPP1R14C przez KLF7 uwalnia aktywność CDK1, sprzyjając rakowi płaskonabłonkowemu płuca
Dlaczego to odkrycie w raku płuca ma znaczenie
Rak płuca wciąż pozostaje główną przyczyną zgonów z powodu nowotworów na świecie, a jeden z istotnych typów — rak płaskonabłonkowy płuca — pozostaje w tyle w erze leków ukierunkowanych. W przeciwieństwie do niektórych innych nowotworów płuca, które można leczyć lekami celującymi w konkretne mutacje, ten podtyp często zmusza lekarzy do polegania na chemioterapii i immunoterapii, które nie działają u wszystkich chorych. Badanie odkrywa wcześniej ukryty obwód kontrolny wewnątrz komórek raka płaskonabłonkowego, który działa jak odcięcie hamulców podziału komórkowego, i wskazuje na namacalny słaby punkt, który mogą wykorzystać przyszłe leki.
Brakujące ogniwo w trudnym do leczenia raku płuca
Naukowcy zaczęli od przeszukania dużych publicznych baz danych dotyczących nowotworów, aby sprawdzić, czy któryś gen wyróżnia się w raku płaskonabłonkowym płuca. Jeden, nazywany PPP1R14C, konsekwentnie występował na wysokim poziomie w próbkach nowotworowych w porównaniu z normalną tkanką płucną. Jego obfitość wzrastała w miarę zaawansowania choroby, a pacjenci, których guzy produkowały więcej tej cząsteczki, mieli krótsze przeżycie. Wzorce te były widoczne zarówno na poziomie RNA — nośników informacji do produkcji białek — jak i na poziomie samego białka, co sugeruje, że PPP1R14C nie jest tylko obecny, lecz aktywnie uczestniczy w napędzaniu choroby. 
Jak guzy płuca uwalniają hamulce
Aby zrozumieć, dlaczego PPP1R14C jest tak liczny w tych nowotworach, zespół zwrócił się do wyłącznika genowego, jego promotora. Łącząc kilka baz danych śledzących miejsca wiązania różnych białek regulatorowych do DNA, wytypowali czynnik o nazwie KLF7 jako głównego podejrzanego. W komórkach raka płaskonabłonkowego płuca hodowanych w laboratorium zwiększenie poziomu KLF7 powodowało wzrost PPP1R14C, podczas gdy jego zmniejszenie wyraźnie obniżało poziom tego genu. Doświadczenia, w których promotor PPP1R14C połączono z raportorem emitującym światło, potwierdziły, że KLF7 może bezpośrednio przełączać ten wyłącznik; zmiana krótkiego fragmentu DNA, gdzie KLF7 się wiąże, likwidowała efekt. Technika wyciągania DNA związanego z KLF7 z nieuszkodzonych komórek wykazała, że czynnik ten fizycznie siedzi na promotorze PPP1R14C, zamykając sprawę, że KLF7 bezpośrednio włącza ten gen.
Od przełącznika genowego do agresywnego zachowania
Kiedy poznali już to, co podnosi poziom PPP1R14C, naukowcy zapytali, co ta cząsteczka właściwie robi. Używając linii komórkowych raka płaskonabłonkowego płuca, obniżyli poziom PPP1R14C za pomocą narzędzi genetycznych i obserwowali zachowanie komórek. Komórki pozbawione PPP1R14C rosły wolniej, tworzyły mniej kolonii, rzadziej penetrowały przez żelową barierę i częściej ulegały zaprogramowanej śmierci. Odwrotność również była prawdziwa: komórki zaprojektowane do wytwarzania dodatkowego PPP1R14C dzieliły się szybciej, tworzyły więcej kolonii i naciekały bardziej agresywnie. Gdy takie zmodyfikowane komórki wszczepiono myszom, guzy z obniżonym PPP1R14C rosły słabiej i ważyły mniej. Razem te wyniki pokazują, że PPP1R14C nie jest biernym obserwatorem, lecz aktywnym czynnikiem promującym cechy nowotworowe.
Krok po kroku: wewnątrz silnika cyklu komórkowego
Idąc dalej, zespół zbadał, które programy komórkowe zależą od PPP1R14C. Szerokie analizy aktywności genów wykazały, że usunięcie PPP1R14C szczególnie zaburza geny kontrolujące krytyczny punkt kontrolny G2/M — moment, w którym komórka decyduje się na podział. W centrum tego punktu kontrolnego znajduje się CDK1, główny przełącznik wejścia w mitoza. W komórkach nowotworowych z wysokim PPP1R14C CDK1 nosił aktywującą grupę fosforanową, a jego elementy docelowe były aktywowane, sygnalizując zielone światło dla podziału. Kiedy PPP1R14C został zmniejszony, ta aktywacja się zmniejszała. Doświadczenia biochemiczne wyjaśniły dlaczego: PPP1R14C wiąże się z enzymem „gumkującym” komórkowe oznaczenia, nazywanym PP1, który normalnie usuwa aktywującą fosforanową grupę z CDK1. Poprzez blokowanie PP1, PPP1R14C uniemożliwia mu dotarcie do CDK1, więc sygnał aktywacji utrzymuje się, a komórki nadal przechodzą przez cykl. 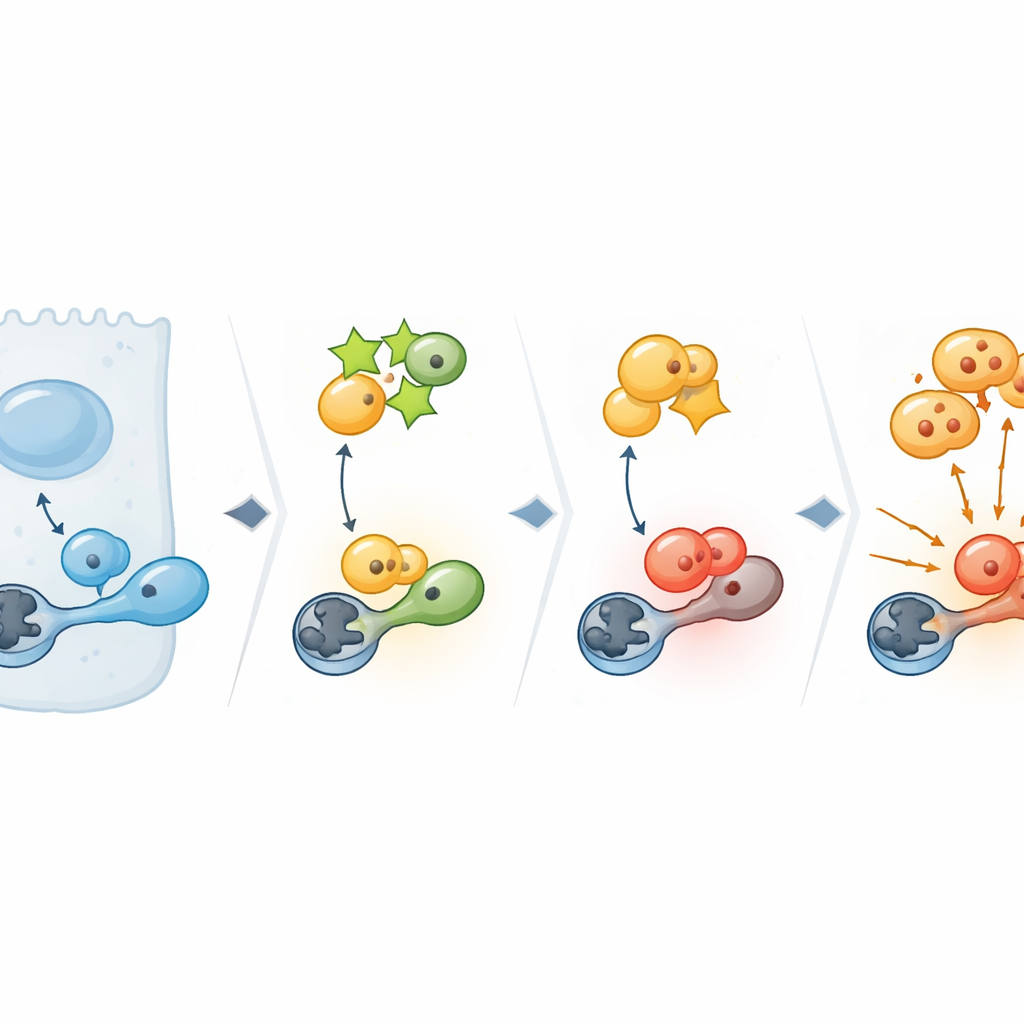
Przekucie odkrycia molekularnego w pomysł na leczenie
Najbardziej zachęcająca część pracy pojawiła się, gdy badacze przetestowali lek bezpośrednio blokujący CDK1. W komórkach przeładowanych PPP1R14C inhibitor CDK1 likwidował przewagę wzrostu, ograniczał formowanie kolonii i hamował inwazję, skutecznie ponownie stosując hamulce, które PPP1R14C wcześniej zwolnił. Składając elementy w całość, badanie opisuje jasny ciąg zdarzeń: KLF7 włącza PPP1R14C; PPP1R14C neutralizuje PP1; CDK1 pozostaje nadaktywne; a komórki raka płaskonabłonkowego płuca dzielą się bez kontroli. Dla osób niebędących specjalistami oznacza to, że naukowcy zidentyfikowali zarówno sygnał ostrzegawczy — wysoki poziom PPP1R14C, wskazujący na bardziej agresywne guzy — jak i obiecujący dźwignię terapeutyczną: leki blokujące CDK1, szczególnie u pacjentów, których guzy zależą od tego wymykającego się spod kontroli obwodu.
Cytowanie: Xing, L., Yuan, C., Shen, X. et al. Transcriptional activation of PPP1R14C by KLF7 unleashes CDK1 activity to promote lung squamous cell carcinoma. Sci Rep 16, 9244 (2026). https://doi.org/10.1038/s41598-026-39174-3
Słowa kluczowe: rak płaskonabłonkowy płuca, cykl komórkowy, CDK1, PPP1R14C, terapia ukierunkowana