Clear Sky Science · pl
Zwiększona miażdżyca i ekspresja „inflammarafts” w komórkach piankowatych makrofagów u myszy pozbawionych AIBP.
Dlaczego zatkane tętnice to coś więcej niż nadmiar tłuszczu
Miażdżyca — stopniowe zatykanie i stwardnienie tętnic — jest główną przyczyną zawałów serca i udarów. Często wyobrażamy sobie ten proces jedynie jako gromadzenie tłuszczu w naczyniach krwionośnych, ale rzeczywistość jest bardziej złożona: komórki układu odpornościowego w ścianie naczynia mogą albo łagodzić stan zapalny, albo go zaogniać. Badanie to wyjaśnia, dlaczego w pewnych warunkach te komórki zmieniają się z „załóg sprzątających” gromadzących tłuszcz w niebezpiecznych prowokatorów, które przyczyniają się do przekształcania blaszek w bardziej zagrażające życiu stadia.
Komórki odpornościowe magazynujące tłuszcz
W rozwijających się blaszkach miażdżycowych makrofagi — rodzaj białych krwinek — pochłaniają duże ilości cholesterolu i przekształcają się w tzw. komórki piankowate — napęczniałe komórki wypełnione kroplami tłuszczu. Wcześniejsze badania na mysich modelach sugerowały, że mimo niezdrowego wyglądu te komórki piankowate bywają zaskakująco mało zapalne, podczas gdy szczuplejsze makrofagi w ich pobliżu częściej wydzielają sygnały zapalne. Nowe badanie pyta, co się dzieje, gdy organizm nie ma białka AIBP, które zwykle pomaga usuwać cholesterol z powierzchni komórek i kontroluje określone „gorące punkty” w błonie komórkowej.
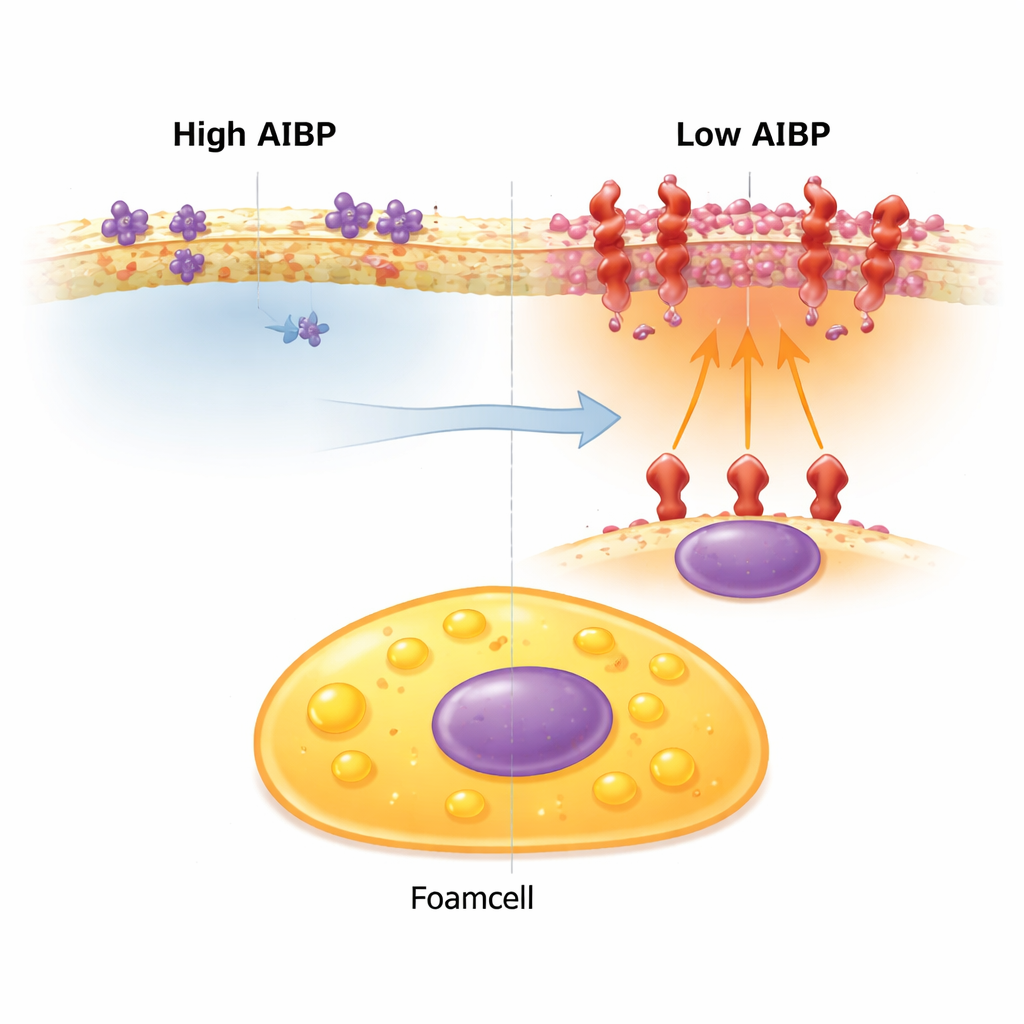
Gorące punkty błony, które wzmacniają sygnały alarmowe
Powierzchnia komórki nie jest jednorodna. Cholesterol i niektóre tłuszcze grupują się w maleńkie platformy, na których mogą gromadzić się receptory wykrywające zagrożenia. Gdy te platformy powiększają się i zagęszczają receptory zapalne, autorzy nazywają je „inflammarafts”. Jeden z takich receptorów, TLR4, pomaga komórkom wyczuwać zagrożenia, ale jego nadmierna aktywacja może podtrzymywać przewlekły stan zapalny. U normalnych myszy podatnych na wysoki poziom cholesterolu makrofagi nienasycone w lipidy zwykle mają więcej tych inflammarafts, podczas gdy komórki piankowate pozostają w nich stosunkowo ubogie — to jedna z przyczyn, dla których komórki piankowate bywały postrzegane jako mniej zapalne.
Gdy komórki obładowane tłuszczem stają się zapalne
Zespół badawczy porównał myszy pozbawione zarówno AIBP, jak i kluczowego receptora usuwającego cholesterol (co czyni je wysoce podatnymi na chorobę tętnic) z myszami kontrolnymi pozbawionymi tylko tego receptora. Po 16 tygodniach diety wysokotłuszczowej myszy pozbawione AIBP miały blaszki zawierające więcej komórek piankowatych, z każdą wypełnioną większą ilością neutralnych tłuszczów. Co istotne, te komórki piankowate wykazywały teraz wysoki poziom par TLR4 i cholesterolowo‑bogatych fragmentów błony — cech charakterystycznych dla inflammarafts — stając się głównym typem komórek zapalnych w blaszce zamiast dotąd spokojniejszych, nastawionych na magazynowanie. W hodowlach laboratoryjnych makrofagi z myszy pozbawionych AIBP, które zamieniono w komórki piankowate za pomocą utlenionego cholesterolu, uruchamiały geny związane z zapaleniem, degradacją tkanek i przebudową naczyń oraz wykazywały większy stres oksydacyjny i uszkodzenia mitochondriów.
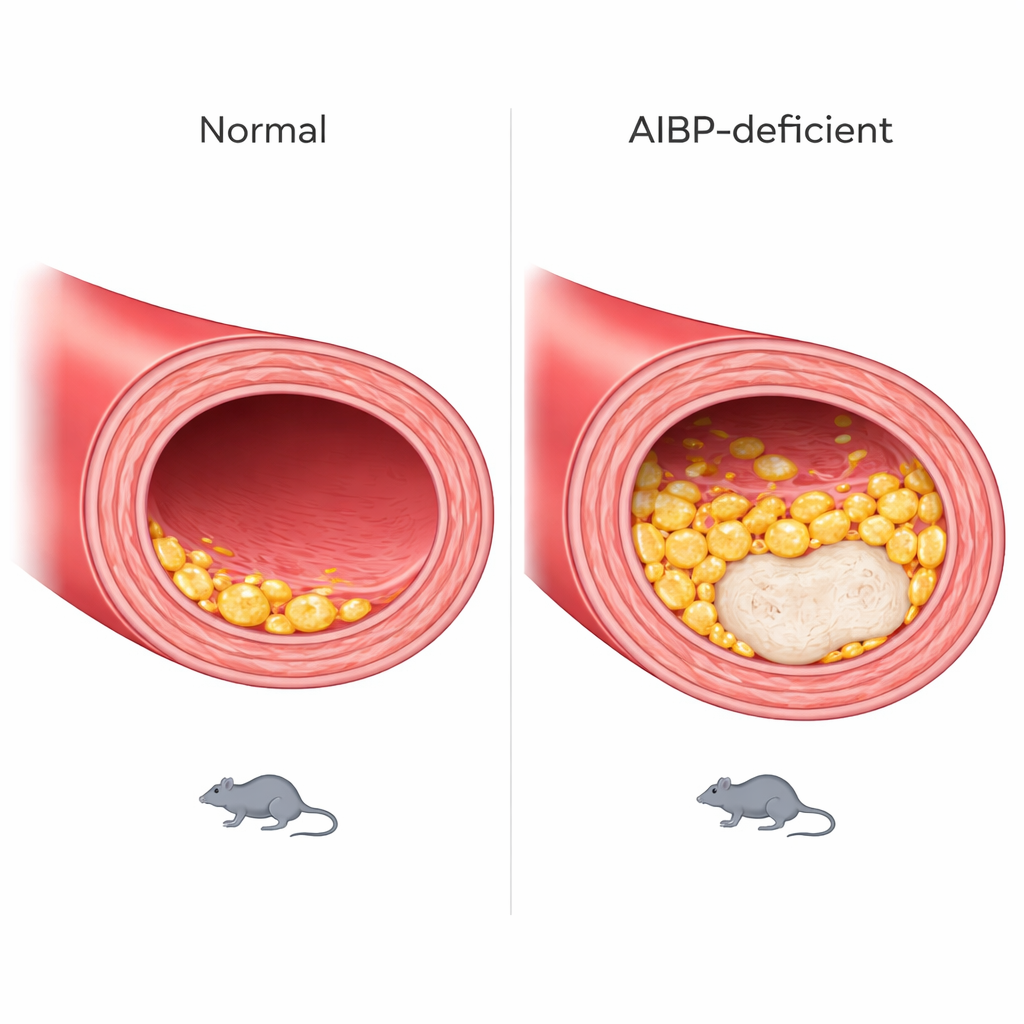
Rosnące, niestabilne blaszki w ścianie naczynia
Te zmiany komórkowe przekładały się na cięższy przebieg choroby w tętnicach. Przekroje głównego naczynia wychodzącego z serca wykazały, że myszy pozbawione AIBP rozwijały większe blaszki i, co ważne, większe jądra martwicze — martwe obszary w obrębie blaszki związane z pękającymi, „wrażliwymi” zmianami. Zarówno samce, jak i samice były dotknięte, choć wzór rozmieszczenia największych uszkodzeń wzdłuż naczynia różnił się między płciami. Zwierzęta szybciej przybierały na wadze i miały wyższy poziom trójglicerydów we krwi, co wskazuje na szersze zaburzenia w gospodarce tłuszczowej.
Co to może oznaczać dla przyszłych terapii
Dla osoby niezajmującej się na co dzień tematem kluczowy wniosek jest taki, że nie wszystkie komórki naładowane cholesterolem w blaszce są takie same. Gdy AIBP jest obecne, komórki piankowate mają skłonność do pełnienia roli magazynów, cicho przechowując nadmiar tłuszczu. Gdy AIBP brakuje, te same komórki przebudowują powierzchnię, tworzą inflammarafts i zaczynają nadawać głośne sygnały zapalne, które popychają blaszki ku niebezpiecznym, zaawansowanym stadom. Choć praca została wykonana na myszach, wskazuje ona na AIBP i kontrolę tych błonowych „gorących punktów” jako potencjalne dźwignie dla przyszłych terapii mających na celu zapobieganie niestabilności i zagrażającym życiu konsekwencjom blaszki miażdżycowej.
Cytowanie: Li, S., Nazarenkov, N., Alekseeva, E. et al. Increased atherosclerosis and expression of inflammarafts in macrophage foam cells in AIBP-deficient mice.. Sci Rep 16, 7645 (2026). https://doi.org/10.1038/s41598-026-39113-2
Słowa kluczowe: miażdżyca, komórki piankowate makrofagów, zapalność, metabolizm cholesterolu, AIBP