Clear Sky Science · pl
Sztuczna inteligencja do diagnozy ostrego zespołu aortalnego oparta na fuzji informacji multimodalnych
Dlaczego to ma znaczenie dla osób z bólem w klatce piersiowej
Ostry zespół aortalny to nagły przypadek medyczny, w którym główna tętnica organizmu może nagle pęknąć lub rozwarstwić się, co bez rozpoznania i szybkiego leczenia może prowadzić do śmierci w ciągu kilku godzin. Objawy często udają zawał serca, naciągnięcie mięśni lub nawet niestrawność, co sprawia, że rozpoznanie bywa trudne. W pracy opisano nowy system sztucznej inteligencji, który łączy obrazy TK z wynikami badań krwi, aby pomóc lekarzom wcześniej i dokładniej rozpoznawać te ciche katastrofy naczyniowe oraz wyróżniać przypadki graniczne wymagające ponownej oceny.
Niebezpieczne rozdarcie skryte na widoku
Ostry zespół aortalny (OZA) obejmuje kilka powiązanych problemów w ścianie aorty, takich jak klasyczne rozwarstwienie, krwiak ścienny czy owrzodzenia penetrujące. Łączy je jedno ryzyko: krew wdziera się do lub przez ścianę naczynia, co może szybko doprowadzić do pęknięcia lub utraty przepływu krwi do ważnych narządów. Największe ryzyko występuje w ciągu pierwszych dni od pojawienia się objawów, gdy śmiertelność bez szybkiego leczenia może sięgać nawet około 70%. Lekarze używają angiografii TK do oceny aorty oraz badań krwi, takich jak D-dimer i markery zapalne, aby ocenić krzepliwość i aktywność układu odpornościowego. Jednak dolegliwości pacjentów często są nieostre, badanie fizykalne może wydawać się prawidłowe, a obrazy TK mogą być subtelne lub zniekształcone przez ruchy czy artefakty, dlatego w rutynowej praktyce około jedna trzecia przypadków bywa początkowo przeoczona.
Co przeoczają obecne narzędzia AI
W ostatnich latach pojawiły się zaawansowane systemy rozpoznawania obrazu, które potrafią przeszukiwać skany TK lub zdjęcia rentgenowskie pod kątem oznak rozdarcia aorty. Jednak większość z nich analizuje wyłącznie obrazy i pomija wyniki badań krwi, albo łączy różne strumienie danych w sposób powierzchowny, bez realnego uczenia się ich wzajemnych zależności. To stoi w sprzeczności z podejściem klinicznym: lekarze integrują informacje z obrazu, wyniki badań i historię choroby umysłowo w jeden obraz. Proste „doklejanie” cech obrazowych i liczb z badań krwi może wręcz pogorszyć sytuację, ponieważ dane laboratoryjne są hałaśliwe, niepełne i matematycznie powiązane. Wiele modeli AI działa też jak czarna skrzynka, wydając ocenę bez wyjaśnienia procesu rozumowania, co zniechęca lekarzy na dyżurze do polegania na nich w sytuacjach, gdy życie pacjenta jest zagrożone.
Nowe podejście do łączenia skanów i badań krwi
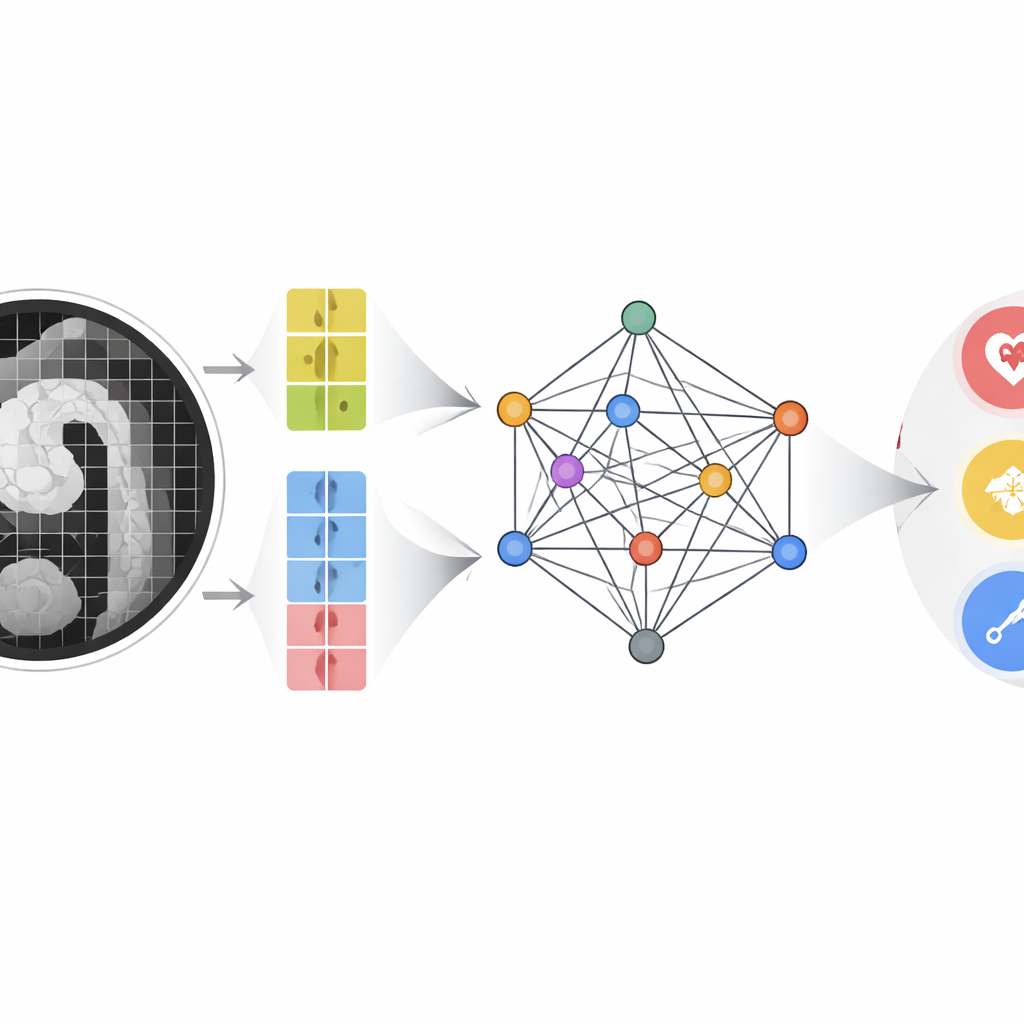
Autorzy opracowali model multimodalnej fuzji wieloskalowej (MMMF), zaprojektowany tak, by naśladować sposób rozumowania doświadczonych radiologów i kardiologów. Najpierw dwutorowy enkoder obrazów analizuje skan angiograficzny TK na dwóch poziomach szczegółowości: duże fragmenty obrazu oddają ogólny kształt i przebieg aorty, podczas gdy mniejsze fragmenty skupiają się na drobnych detalach, takich jak mikroskopijne pęknięcia intimy czy niewielkie kieszonki krwi w ścianie naczynia. Równocześnie kluczowe wskaźniki krwi — w tym D-dimer oraz panel markerów zapalnych wyprowadzonych z liczby białych krwinek i płytek krwi — są przekształcane w numeryczne punkty cech. Te cechy obrazowe i laboratoryjne stają się węzłami w strukturze przypominającej graf, w którym zaawansowana grafowa sieć neuronowa przekazuje między nimi „wiadomości”, ucząc się, jak określone wzorce krwi potwierdzają lub przeczą subtelnym obserwacjom obrazowym.
Jak dobrze działa system
Zespół trenował i testował model MMMF na skanach TK oraz jednoczesnych badaniach krwi od 493 pacjentów badanych w latach 2019–2024, obejmujących potwierdzone przypadki OZA różnych typów oraz grupę kontrolną bez OZA. Porównano ich podejście z dobrze znanymi modelami opartymi tylko na obrazach, modelami bazującymi jedynie na danych laboratoryjnych oraz kilkoma nowoczesnymi systemami multimodalnymi pierwotnie zaprojektowanymi do łączenia obrazów z tekstem. W miarach takich jak dokładność, precyzja, czułość i F1 model MMMF okazał się najlepszy. Pole pod krzywą ROC przekroczyło 0,9, co wskazuje na silną zdolność rozróżniania między prawidłową aortą, klasycznymi rozwarstwieniami obejmującymi aortę wstępującą lub zstępującą oraz formami nietypowymi. Dane obrazowe pozostały najsilniejszym pojedynczym źródłem informacji, ale starannie skonstruowana fuzja z danymi laboratoryjnymi przyniosła wymierny wzrost wydajności, zwłaszcza w trudnych lub granicznych przypadkach. Eksperymenty ablacjyjne wykazały, że kluczowe były dwa elementy: dwuskala ścieżka obrazowania oraz oparty na transformerze graf modelujący zależności na długim zasięgu między cechami.
W kierunku partnerstwa lekarzy i maszyn
Powyżej liczb dotyczących dokładności, ważnym wkładem tej pracy jest nacisk na współpracę zamiast zastępowania specjalistów. System świetnie sprawdza się w szybkim wykluczaniu oczywiście prawidłowych skanów i jednoznacznie chorobowych przypadków nietypowych, pełniąc rolę inteligentnego wstępnego sortera. Równie istotne jest to, że potrafi rozpoznać, kiedy jego własne zaufanie jest niskie — często w sytuacjach, które także dla ekspertów są trudne, np. w wczesnych lub łagodniejszych postaciach rozwarstwienia — i wtedy oznaczać tych pacjentów do pilnej ponownej oceny, dodatkowych badań obrazowych lub konsultacji starszego specjalisty. W istocie badanie pokazuje, że gdy detale obrazowe i wskazówki z badań krwi są splecione w uporządkowany, klinicznie inspirowany sposób, AI może zarówno usprawnić wczesne rozpoznawanie ostrego zespołu aortalnego, jak i stworzyć siatkę bezpieczeństwa przed przeoczonymi nagłymi przypadkami, jednocześnie pozostawiając lekarzy w roli decydentów końcowych.
Cytowanie: Yang, Z., Xu, S., Wang, B. et al. AI-driven diagnosis of acute aortic syndrome based on multi-modal information fusion. Sci Rep 16, 8332 (2026). https://doi.org/10.1038/s41598-026-39111-4
Słowa kluczowe: ostry zespół aortalny, rozwarstwienie aorty, sztuczna inteligencja medyczna, diagnostyka multimodalna, grafowe sieci neuronowe