Clear Sky Science · pl
Niedobór Dlgap2 zaburza homeostazę synaptyczną przez promowanie ubikwitynowo‑zależnej degradacji Itsn1 w modelu o cechach autyzmu wywołanym kwasem walproinowym
Dlaczego powszechny lek i okablowanie mózgu mają znaczenie
Kwas walproinowy to lek stosowany od dawna w padaczce i zaburzeniach nastroju, jednak przyjmowany w czasie ciąży wiąże się ze zwiększonym ryzykiem autyzmu u dzieci. W badaniu postawiono pilne pytanie, ważne dla rodzin i lekarzy: co dokładnie ten lek robi z rozwijającym się okablowaniem mózgu? Śledząc zmiany aż do konkretnych cząsteczek w synapsach — punktach komunikacji między komórkami nerwowymi — badacze odkrywają nowy ciąg zdarzeń, który może pomóc wyjaśnić zachowania przypominające autyzm i wskazać kierunki przyszłych strategii terapeutycznych. 
Poszukiwanie wspólnych problemów przez gatunki
Aby znaleźć wiarygodne wskazówki, zespół nie polegał na jednym modelu zwierzęcym. Porównano mózgi lub tkanki przypominające mózg z ludzkich organoidów korowych, małp, szczurów i myszy, którym podano kwas walproinowy przed urodzeniem. Korzystając z szeroko zakrojonych badań genów i białek, zidentyfikowano niewielki zestaw genów, które zmieniały się we wszystkich tych systemach i były powiązane z synapsami oraz osłonkami włókien nerwowych. Jeden z nich wyróżniał się szczególnie: Dlgap2, białko rusztowania, które pomaga organizować stronę postsynaptyczną synaps pobudzających. U myszy leczonych prenatalnie kwasem walproinowym poziom Dlgap2 spadł w korze, a bardziej precyzyjnie — w małych synaptycznych przedziałach, co sugeruje, że to strukturalne białko jest istotną ofiarą ekspozycji na lek.
Od zmian molekularnych do zachowań
Autorzy zapytali następnie, czy sama utrata Dlgap2 wystarczy, by zaburzyć funkcjonowanie mózgu. Wykorzystali wirusy niosące krótkie włosowe RNA, by zmniejszyć Dlgap2 w hodowanych neurony mysich i u nowo narodzonych myszy. W hodowli neurony z obniżonym Dlgap2 rozwijały krótsze rozgałęzienia i miały mniej punktów postsynaptycznych — oznaki osłabionych połączeń. U żywych zwierząt celowe wyciszenie Dlgap2 w mózgu wywołało zachowania przypominające autyzm: młode samce miały trudności ze znalezieniem ukrytej platformy w teście wodnego labiryntu i wykazywały mniejsze zainteresowanie partnerami społecznymi oraz nowością społeczną w teście trzech komór. Zmiany te naśladują deficyty uczenia się i społeczne obserwowane u zwierząt wystawionych na kwas walproinowy, co wzmacnia hipotezę, że utrata Dlgap2 nie jest tylko skutkiem ubocznym, lecz czynnikiem napędzającym zmienione zachowanie.
Odnalezienie wrażliwego partnera w synapsie
Aby zrozumieć, jak utrata Dlgap2 rozchodzi się w synapsie, badacze przyjrzeli się bliżej białkom zakotwiczonym w gęstości postsynaptycznej — gęstym molekularnym podkładzie odbierającym sygnały chemiczne. Dzięki proteomice stwierdzili, że redukcja Dlgap2 zmieniała obfitość setek białek synaptycznych, zwłaszcza tych zaangażowanych w organizację synaps i recykling pęcherzyków przez endocytozę. Jedno białko, Intersectin‑1 (Itsn1), spadło wyjątkowo gwałtownie. Dalsze badania biochemiczne wykazały, że Dlgap2 i Itsn1 fizycznie występują w tych samych kompleksach białkowych w frakcjach wzbogaconych w synapsy i że oba pojawiają się wśród genów powiązanych z autyzmem. Wskazuje to na ukierunkowane regulatoryjne partnerstwo tych dwóch cząsteczek w zatłoczonym synaptycznym środowisku. 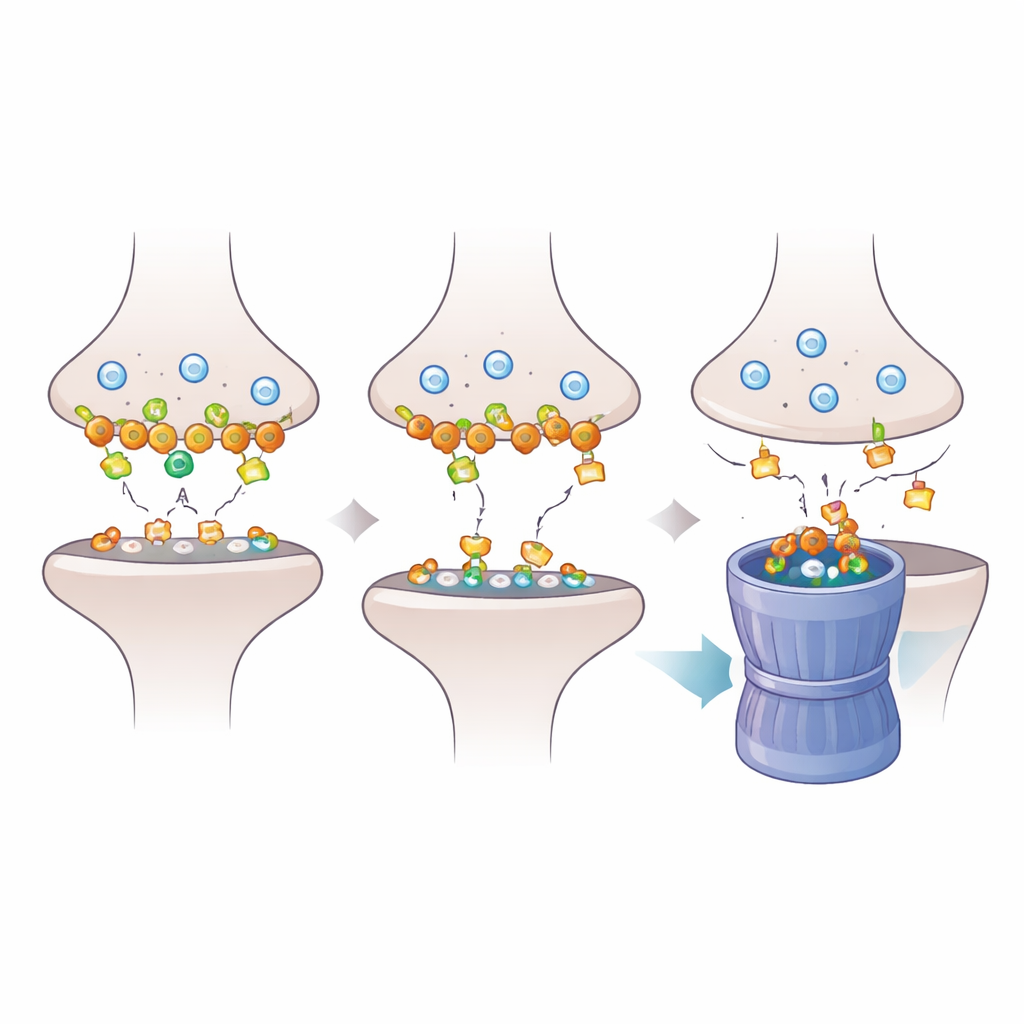
Na jaw wychodzi ukryta ścieżka utylizacji
Zespół zapytał następnie, dlaczego poziomy Itsn1 spadają, gdy brakuje Dlgap2. Zaobserwowano, że w przedziałach synaptycznych wyciszenie Dlgap2 wywołuje formę znakowania białek zwaną ubikwitynacją K48‑związaną, która oznacza białka do rozkładu przez proteasom komórkowy — „niszczarkę”. Zablokowanie tego systemu utylizacji lekiem MG132 zapobiegło utracie Itsn1, co wskazuje, że Dlgap2 normalnie chroni Itsn1 przed oznaczaniem i zniszczeniem. Bez Dlgap2 Itsn1 jest coraz częściej znakowane, trafia do proteasomu i jest uszczuplane w synapsach, podważając recykling endocytarny i równowagę aktywności synaptycznej. Praca sugeruje, że subtelne zmiany w tempie, w jakim kluczowe białka są wymieniane, mogą destabilizować synapsy podczas rozwoju mózgu.
Co to oznacza dla autyzmu i przyszłych terapii
Podsumowując, badanie proponuje prosty, lecz silny obraz dla szerokiego odbiorcy: prenatalna ekspozycja na kwas walproinowy może osłabić strukturalne „wzmocnienie” białka (Dlgap2) w synapsach. Gdy to wzmocnienie zostaje utracone, jego białkowy partner (Itsn1) staje się nadmiernie celowany do komórkowej utylizacji, co prowadzi do nieprawidłowego recyklingu składników synaptycznych, a w konsekwencji do niepoprawnie okablowanych obwodów i zachowań przypominających autyzm u myszy. Choć wiele genów i czynników środowiskowych przyczynia się do autyzmu, oś Dlgap2–Itsn1 daje konkretne molekularne powiązanie między prenatalną ekspozycją na lek a zmienioną funkcją mózgu. W dłuższej perspektywie strategie, które zachowają to partnerstwo lub precyzyjnie wyregulują maszynerię utylizacji białek w synapsach, mogłyby pomóc chronić rozwijające się mózgi przed podobnymi zaburzeniami.
Cytowanie: Guo, X., Zhang, L. & Zhuang, K. Dlgap2 deficiency disrupts synaptic homeostasis by promoting ubiquitin-mediated Itsn1 degradation in a valproic acid-induced autism-like model. Sci Rep 16, 8305 (2026). https://doi.org/10.1038/s41598-026-39099-x
Słowa kluczowe: kwas walproinowy a ciąża, białka rusztowania synaptycznego, mechanizmy spektrum autyzmu, droga ubikwityna‑proteasom, mysie modele autyzmu