Clear Sky Science · pl
Zintegrowane przesiewowe badania in silico, profilowanie ADMET i symulacje dynamiki molekularnej nowych naturalnych inhibitorów HDAC6 o potencjale łagodzenia degeneracji mięśni szkieletowych
Dlaczego warto chronić nasze mięśnie
Mięsień szkieletowy to nie tylko narzędzie do podnoszenia ciężarów czy biegania; stanowi największe zasoby białka w organizmie, jest ważnym motorem metabolizmu i niezbędny do codziennej aktywności. Gdy mięśnie zanikają z powodu starzenia, choroby lub braku aktywności, ludzie tracą siłę, niezależność i jakość życia. W tym badaniu autorzy badają komputerowo ukierunkowany sposób odkrywania nowych kandydatów na leki pochodzących z substancji naturalnych, które mogłyby spowolnić lub zapobiec takiemu ubytku mięśni, celując w kluczowy molekularny przełącznik wewnątrz komórek mięśniowych.
Problematyczna cząsteczka osłabiająca mięśnie
W wnętrzu włókien mięśniowych białko o nazwie HDAC6 pomaga kontrolować organizację wewnętrznego rusztowania komórkowego i rozkład innych białek. W warunkach prawidłowych przyczynia się do utrzymania zdrowia mięśni. Jednak gdy aktywność HDAC6 staje się nadmierna, destabilizuje sieć mikrotubul, która utrzymuje kształt mięśnia i połączenia między nerwami a włóknami mięśniowymi. To zakłócenie sprzyja uszkodzeniom białek i kurczeniu się mięśnia. Badania na zwierzętach wykazały, że blokada HDAC6 może zachować rozmiar mięśni i poprawić ich funkcję, co czyni ten enzym atrakcyjnym celem terapeutycznym w walce z atrofią mięśniową.
Szukanie nowych pomysłów na leki w naturze
Wiele istniejących inhibitorów HDAC6 zostało zaprojektowanych syntetycznie i może powodować niepożądane skutki uboczne lub brakować im precyzji wobec tego konkretnego celu. Autorzy zwrócili się zamiast tego ku chemicznej różnorodności natury, wychodząc z założenia, że produkty naturalne często mają struktury, które w sposób subtelny, lecz skuteczny oddziałują z ludzkimi białkami. Wykorzystali kolekcję SuperNatural 3.0, zawierającą niemal pół miliona unikalnych związków naturalnych, i postawili proste pytanie: które z tych cząsteczek mogą wpasować się w aktywne zagłębienie HDAC6 w sposób go wyłączający, a jednocześnie zachowywać cechy rokujące na dobrą substancję leczniczą? 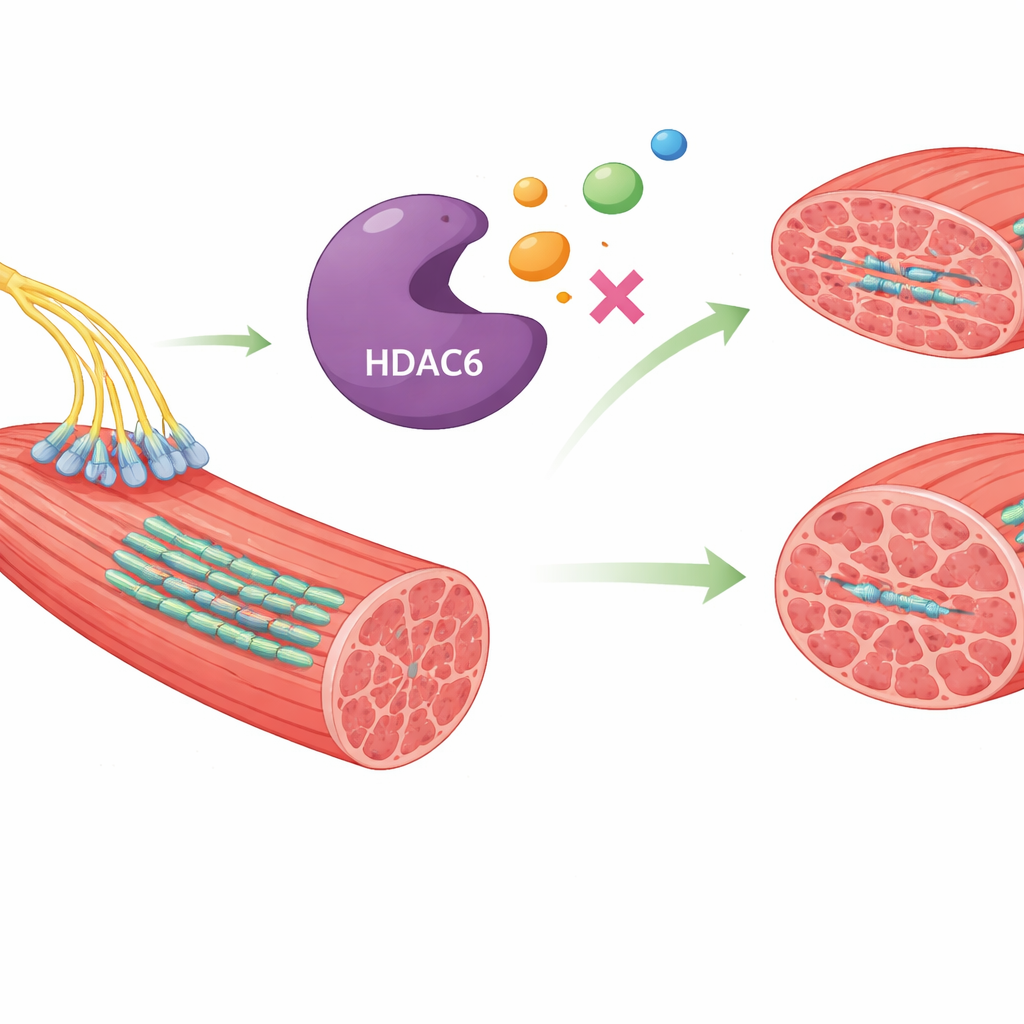
Szybkie komputerowe przesiewanie setek tysięcy cząsteczek
Aby na to odpowiedzieć, zespół zastosował zintegrowany pipeline „screeningu in silico”. Najpierw przygotowali szczegółowy trójwymiarowy model tunelu katalitycznego HDAC6, oparty na eksperymentalnej strukturze enzymu związanej z znanym inhibitorem. Następnie, używając specjalistycznego oprogramowania, dokowali 449 058 związków naturalnych w tym tunelu, oceniając, jak ciasno i korzystnie każda z nich pasuje. Z tej obszernej puli początkowej 146 cząsteczek wypadło lepiej niż lek referencyjny trichostatyna A. Badacze zastosowali potem serię filtrów imitujących kryteria deweloperów leków: odpowiedni rozmiar i polarność, zdolność do wchłaniania przez przewód pokarmowy, akceptowalna rozpuszczalność, ograniczona przewidywana toksyczność i realistyczne perspektywy syntezy chemicznej. Po tych etapach wyłoniły się dwa wyróżniające się kandydaty, oznaczone jako SN0000021 i SN0000043.
Badanie stabilności i zachowania w wirtualnej komórce
Znalezienie dobrej pozycji dokowania to za mało; potencjalne leki muszą pozostawać związane pod ciągłym ruchem rzeczywistych systemów biologicznych. Aby to sprawdzić, zespół przeprowadził długie symulacje dynamiki molekularnej — w zasadzie filmy o wysokiej rozdzielczości przedstawiające kompleksy HDAC6–cząsteczek przez 200 miliardowych części sekundy. Monitorowali, jak bardzo chwieje się szkielet białka, jak głęboko każda cząsteczka osiada w tunelu, jak bardzo jest eksponowana na otaczającą wodę i jak ściśle kompleks pozostaje upakowany. Oba związki naturalne tworzyły stabilne, długotrwałe interakcje z kluczowymi aminokwasami, o których wiadomo, że kontrolują aktywność HDAC6. Wykazały mniejsze fluktuacje i ściślejsze upakowanie niż inhibitor referencyjny, co sugeruje mocniejsze dopasowanie. Zaawansowane obliczenia energii, które szacują korzystność wiązania z perspektywy termodynamicznej, dodatkowo potwierdziły, że te dwa związki prawdopodobnie wiążą się silniej niż lek kontrolny. 
Od trafień komputerowych do przyszłych leków ratujących mięśnie
Dla osoby niebędącej specjalistą podsumowanie jest proste: wykorzystując wyłącznie narzędzia komputerowe, badacze przesiągnęli ogromny katalog substancji naturalnych i wskazali dwa, które wydają się szczególnie dobrze przystosowane do przyczepienia się i wyciszenia HDAC6 — białka związanego z zanikiem mięśni. Kandydaci ci nie tylko mocno wiążą się w symulacjach, ale także wykazują korzystne przewidywane profile wchłaniania, dystrybucji i bezpieczeństwa, co czyni je obiecującymi punktami wyjścia do opracowania nowych leków. Praca nie dowodzi jeszcze, że te cząsteczki pomogą prawdziwym mięśniom; to będzie wymagać testów laboratoryjnych na oczyszczonym enzymie, komórkach i modelach zwierzęcych. Jednak badanie dostarcza przekonującego planu działania, jak cyfrowy screening produktów naturalnych może odkrywać potencjalne terapie chroniące mięsień szkieletowy przed degeneracją.
Cytowanie: Ahmad, K., Ahmad, S.S. & Choi, I. Integrated virtual screening, ADMET profiling, and molecular dynamics simulations of novel natural HDAC6 inhibitors with the potential to ameliorate skeletal muscle degeneration. Sci Rep 16, 7840 (2026). https://doi.org/10.1038/s41598-026-39066-6
Słowa kluczowe: atrofia mięśni szkieletowych, hamowanie HDAC6, odkrywanie leków z produktów naturalnych, screening in silico, regeneracja mięśni