Clear Sky Science · pl
Receptor sensujący wapń (casr) u danio pręgowanego modyfikuje strukturę i funkcję serca
Dlaczego serca ryb mają znaczenie dla zdrowia ludzi
Nasze serca polegają na wapniu, prostym pierwiastku, aby bić prawidłowo. Gdy sygnały wapniowe zawodzą, skutkiem mogą być niewydolność serca lub inne poważne choroby. W tym badaniu wykorzystano małe danio pręgowane — przezroczyste ryby słodkowodne często używane w laboratoriach — aby zbadać, jak komórkowy przełącznik wykrywający wapń wpływa na siłę skurczu serca i przeżycie. Wyłączając pojedynczy gen, który pomaga komórkom wyczuwać wapń, naukowcy odkryli łańcuch problemów w pracy pompy serca, kształcie ciała, a nawet wypełnionym powietrzem pęcherzu pławnym ryby. Ich praca pokazuje także, że szersze tło genetyczne zwierzęcia może zdecydowanie złagodzić lub nasilić skutki szkodliwej mutacji — wniosek mający wyraźne implikacje dla medycyny ludzkiej.
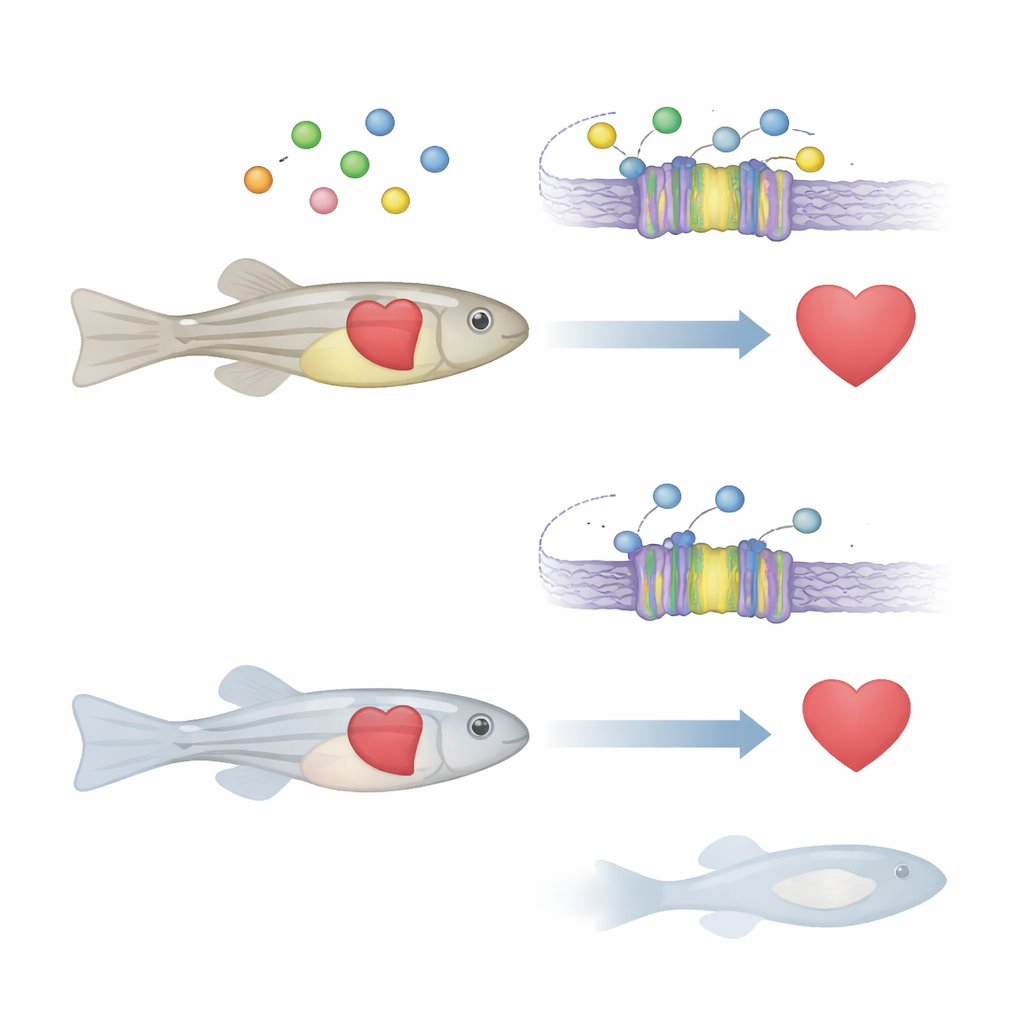
Komórkowy „termostat” dla wapnia
Wapń wewnątrz i na zewnątrz komórek działa jak uniwersalny sygnał kontrolujący ruch mięśni, uwalnianie hormonów, a nawet to, które geny są aktywowane. Wiele narządów polega na białku zwanym receptorem wyczuwającym wapń, które działa jak termostat poziomu wapnia. Gdy stężenie wapnia na zewnątrz komórki się zmienia, ten receptor reguluje uwalnianie hormonów i inne procesy, aby przywrócić równowagę. U ludzi wady tego receptora już powiązano z zaburzeniami kości i metabolizmu minerałów, a podejrzewa się jego udział w chorobach serca i niektórych nowotworach. Jednak wciąż nie było jasne, w jaki sposób ten czujnik wapnia wpływa na rozwój i funkcję serca w całym organizmie.
Co się dzieje, gdy czujnik wapnia zostaje wyłączony
Zespół skupił się na wersji tego genu u danio, zwanej casr, która jest silnie zachowana w porównaniu z ludzkim odpowiednikiem. Korzystając z nowoczesnych narzędzi edycji genów, stworzyli danio, u których obie kopie casr zostały unieruchomione. Początkowo młode ryby wyglądały niemal normalnie. Jednak do piątego dnia po zapłodnieniu wiele mutantów nie zdołało napompować pęcherza pławnego, małego narządu wypełnionego gazem kontrolującego wyporność. Te ryby tonęły na dno, słabo pływały, wkrótce rozwijały skrzywienie kręgosłupa i wszystkie umierały w ciągu dwóch tygodni. Zewnętrzne objawy wskazywały na poważne problemy wewnętrzne wpływające na więcej niż jeden układ narządów.
Słabsze, mniejsze i wolniejsze serce
Filmy o dużej szybkości i analiza obrazów bijących serc ujawniły, jak głęboko brak czujnika wapnia zaburzył wydajność serca. U normalnych larw danio komora serca napełnia się i opróżnia w silnym rytmicznym rytmie. U mutantów komora była wyraźnie mniejsza podczas napełniania, serce biło wolniej, a każdy skurcz wyrzucał mniej krwi. Miary skracania mięśnia sercowego i zmiany pola komory przy każdym skurczu były zmniejszone, co świadczy o osłabionym skurczu. Całkowita wydajność serca — objętość krwi przepompowywana na minutę — gwałtownie spadła. Na poziomie genów zmieniły się setki transkryptów, a kluczowe sieci kontrolujące gospodarkę wapniową i aparaturę skurczu mięśniowego zostały stłumione, łącząc edycję genu z molekularną i mechaniczną niewydolnością serca.
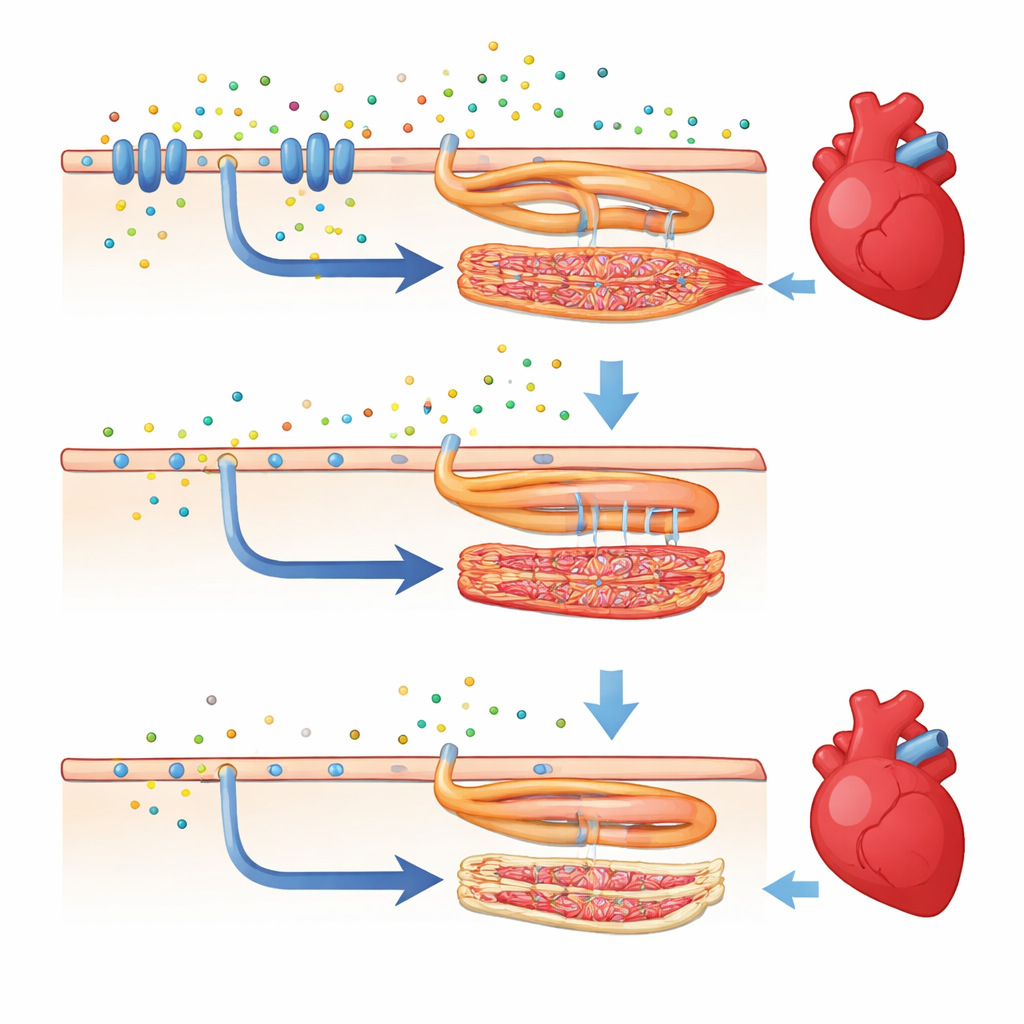
Jak geny tła mogą uratować chore serce
Zaskakująco, ta sama mutacja casr zachowywała się bardzo różnie w innej powszechnej linii danio, znanej jako TL (Tupfel long-fin). Gdy knockout genu przeniesiono na to nowe tło genetyczne, ryby potrafiły napompować pęcherz pławny, przeżyć do dorosłości i miały znacznie lepszą wydajność pompowania serca. Ich serca wciąż były częściowo upośledzone — częstość bicia pozostała niższa niż normalnie — ale miary siły skurczu komory i objętości krwi przepompowywanej na minutę niemal dorównywały zdrowym rybom. U tych „uratowanych” zwierząt wiele genów powiązanych z sygnalizacją wapniową i skurczem mięśnia sercowego powróciło do poziomów pośrednich, wyższych niż w pierwotnej chorej linii. To pokazuje, że inne geny rozrzucone po całym genomie mogą buforować lub nasilać skutki szkodliwej zmiany.
Sygnały kształtujące serce i wyporność
Ponad sercem, utrata czujnika wapnia zaburzyła także główne układy kontrolujące wzrost w zarodku. Geny z szlaków sygnałowych Wnt i Hedgehog — dobrze znanych architektów formowania narządów — zostały stłumione u mutantów. Te zmiany prawdopodobnie przyczyniają się do niepowodzenia napompowania pęcherza pławnego, co z kolei może pogarszać przeżywalność poprzez utrudnianie rybom żerowania i sprawnego poruszania się. Markery różnicowania komórek mięśnia sercowego również były zmniejszone, a komory były mniejsze, co sugeruje, że czujnik wapnia pomaga kierować wzrostem i dojrzewaniem komórek mięśnia sercowego.
Co to oznacza dla zrozumienia ryzyka choroby
Podsumowując, praca ta pokazuje, że receptor wyczuwający wapń jest kluczowym strażnikiem zarówno funkcji serca, jak i prawidłowego rozwoju narządów u danio pręgowanego. Gdy ten czujnik zostaje utracony, sygnały wapniowe zawodzą, mięsień sercowy kurczy się słabiej, pęcherz pławny nie napompowuje się, a zwierzęta umierają młodo. Jednak dramatyczne uratowanie w innej linii genetycznej podkreśla ważny przekaz: reszta genomu może silnie modyfikować, jak niebezpieczna jest dana mutacja. Dla zdrowia ludzi podkreśla to, dlaczego osoby noszące podobne ryzykowne warianty genetyczne mogą mieć bardzo różne przebiegi choroby oraz dlaczego zrozumienie zarówno podstawowych genów choroby, jak i ich tła genetycznego jest niezbędne do przewidywania i leczenia schorzeń serca.
Cytowanie: Liu, L., Hu, Y., Xie, B. et al. Zebrafish casr modulates cardiac structure and function. Sci Rep 16, 8543 (2026). https://doi.org/10.1038/s41598-026-39063-9
Słowa kluczowe: sygnalizacja wapniowa, rozwój serca, model danio pręgowanego, tło genetyczne, funkcja serca