Clear Sky Science · pl
Przenoszenie sił trakcyjnych przez bioaktywny hydrożel macierzy sprzyja zbiorowej migracji nabłonka mediowanej przez integryny
Jak komórki ciągną razem, by się zregenerować
Kiedy przetniesz skórę lub uszkodzisz narząd, warstwy komórek muszą przesunąć się w skoordynowany sposób, by zamknąć ranę. To badanie stawia pozornie proste pytanie: gdy komórki poruszają się razem, czy tylko ciągną za sobą sąsiadów, czy też „rozmawiają” przez miękki materiał pod nimi? Odtwarzając w laboratorium realistyczne, żelopodobne środowisko, autorzy pokazują, że komórki mogą przesyłać siły mechaniczne przez tę miękką macierz, kierując ruchem grupy — odsłaniając ukrytą warstwę komunikacji, która może być kluczowa dla gojenia ran, naprawy tkanek, a nawet szerzenia się nowotworu.
Miękka podstawa, która przenosi siłę
W naszych ciałach wiele komórek spoczywa na miękkim, bogatym w białka szkielecie, a nie na twardej powierzchni jak szkło czy plastik. Aby to naśladować, badacze hodowali komórki nabłonka nerkowego jako ciągłą warstwę na bioaktywnym hydrożelu z Matrigelu i kolagenu, dwóch powszechnych składników tkanek naturalnych. Następnie stworzyli w środku żelu małą pustą przestrzeń, niczym drobną ranę, i obserwowali, jak warstwa komórek przesuwa się do środka, by wypełnić lukę. Aby śledzić aktywność kluczowej ścieżki sygnałowej w komórkach, użyli fluorescencyjnego biosensora raportującego aktywność ERK — białka często reagującego na sygnały mechaniczne. Ta konfiguracja pozwoliła im obserwować na żywo, jak siły mechaniczne w miękkim żelu wiążą się zarówno z ruchem komórek, jak i z ich wewnętrznym sygnalizowaniem. 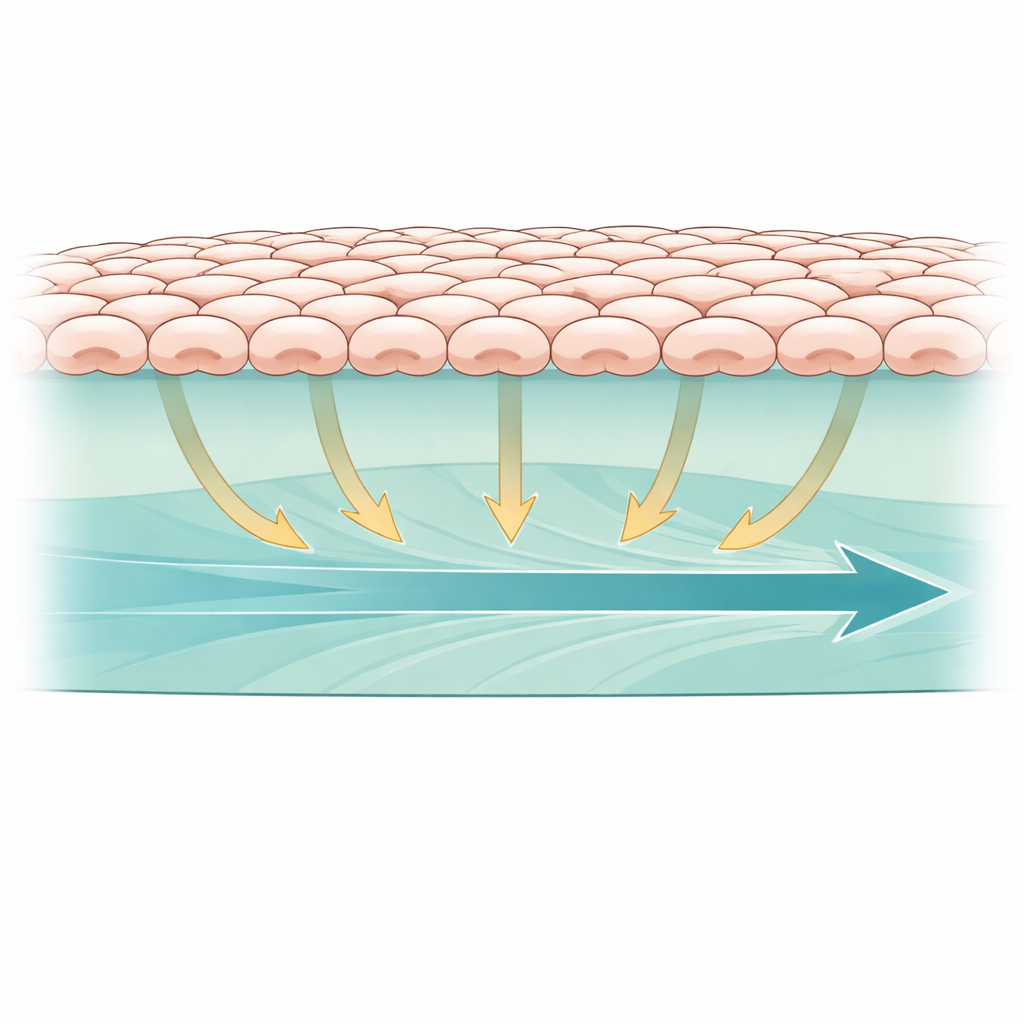
Obserwowanie, jak grunt przesuwa się pod komórkami
Aby ustalić, czy żel rzeczywiście przenosi siłę, zespół wymieszał w materiale drobne magnetyczne kuleczki i śledził ich ruch podczas migracji komórek. Na normalnym żelu zawierającym zarówno Matrigel, jak i kolagen, kuleczki powoli przesuwały się do przodu w tym samym kierunku co posuwająca się warstwa komórek, co wskazuje, że komórki chwytały i ciągnęły macierz pod sobą. Na żelach z samego Matrigelu kulki poruszały się wolniej, sugerując słabsze przenoszenie sił. Gdy żel został chemicznie usieciowany za pomocą glutaraldehydu, by go usztywnić i „zablokować” sieć, kuleczki praktycznie się nie przesuwały. W tych zablokowanych warunkach komórki nadal przyczepiały się, ale ich zbiorowy postęp znacząco zwolnił, a sygnał ERK osłabł i był mniej skoncentrowany na czołowej krawędzi, łącząc silną trakcję macierzy z szybszym i bardziej ukierunkowanym ruchem grupowym.
Wewnętrzne silniki i bramki jonowe napędzają ruch
Następnie autorzy zbadali, co w obrębie komórek generuje te siły pociągowe i jak ta aktywność jest wyczuwana. Użyli leków blokujących kurczenie oparte na miozynie — tego samego rodzaju mechanizmu molekularnego, który napędza mięśnie. Gdy skurcz został zahamowany, aktywność ERK spadła, a przesuwanie się warstwy komórek zwolniło, co zgadza się z pomysłem, że wewnętrzne pociąganie jest potrzebne, by przekazywać napięcie do macierzy. Interferowali też z kilkoma typami kanałów wapniowych w błonie komórkowej i z wewnętrznymi magazynami wapnia. Zablokowanie tych ścieżek jonowych osłabiło aktywność ERK i spowolniło zbiorową migrację, wskazując na łańcuch zdarzeń, w którym mechaniczne pociąganie macierzy przekształca się w sygnały wapniowe i ERK, które pomagają utrzymać grupę w skoordynowanym ruchu.
Ukierunkowywanie kierunku przez przyczepy powierzchniowe
Szczególnie uderzające odkrycie pochodzi z celowania w integryny — cząsteczki powierzchniowe działające jak maleńkie kotwice łączące komórki ze środowiskiem. Gdy badacze zablokowali główny podtyp integryny, warstwa przestała poruszać się do przodu jako spójne czoło, mimo że pojedyncze komórki nadal mogły lokalnie się poruszać niemal z normalną prędkością. Równocześnie ruch kuleczek w żelu niemal zatrzymał się, pokazując, że integryny są niezbędne do przekazywania siły z kurczących się komórek do macierzy. Dla porównania, zablokowanie kanałów mechanosensytywnych związanych z Piezo1, które pomagają komórkom odczuwać ucisk fizyczny, zmniejszyło zarówno tempo migracji, jak i trakcję obserwowaną w żelu. Razem te wyniki rysują obraz, w którym kurczenie generuje siłę, integryny przekazują ją do macierzy, a kanały mechanosensytyczne i sygnalizacja ERK interpretują tę siłę, koordynując kierunek i wydajność zbiorowego ruchu. 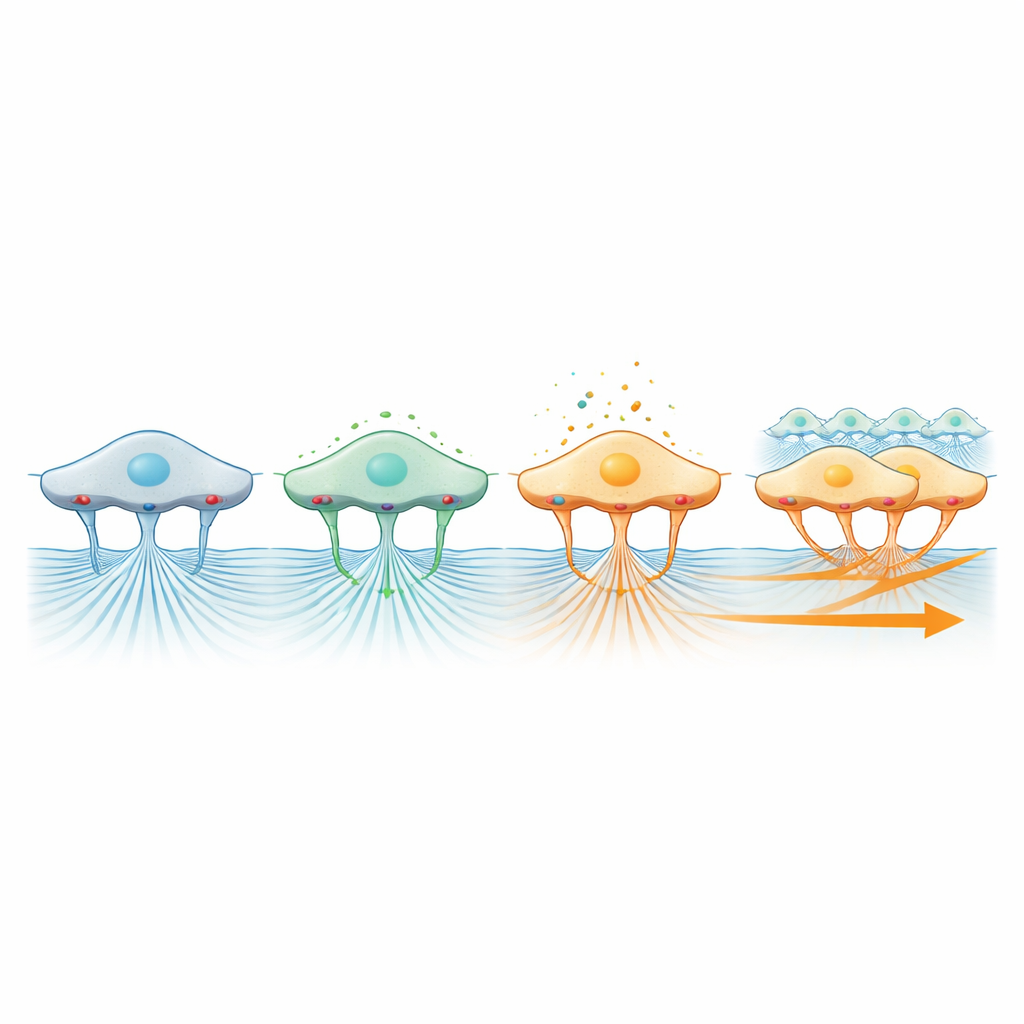
Dlaczego to ma znaczenie dla gojenia i chorób
Krótko mówiąc, praca ta pokazuje, że warstwy komórek nie tylko ciągną za sobą sąsiadów; ciągną też za miękki materiał pod nimi i poprzez niego, wykorzystując go jako rodzaj mechanicznej linii telefonicznej. Kurczenia warstwy komórek wysyłają napięcie przez macierz, a to napięcie — wyczuwane przez integryny i kanały jonowe oraz odczytywane przez aktywność ERK — pomaga grupie poruszać się szybko i w zjednoczonym kierunku. Gdy macierz jest chemicznie zablokowana tak, że siły nie mogą się rozchodzić, lub gdy kluczowe przyczepy i sensory powierzchniowe zostaną zablokowane, zbiorowy marsz słabnie. Te wnioski pogłębiają nasze rozumienie, jak zamykają się rany, jak tkanki utrzymują swoją strukturę oraz jak inwazyjne grupy komórek, na przykład w raku i zwłóknieniach, mogą wykorzystywać mechaniczne ścieżki w swoim otoczeniu, by się rozsiewać.
Cytowanie: Ouyang, M., Cao, Y., Sheng, H. et al. Traction force transmission via bioactive matrix hydrogel promotes epithelial collective migration mediated by integrin. Sci Rep 16, 8923 (2026). https://doi.org/10.1038/s41598-026-39048-8
Słowa kluczowe: zbiorowa migracja komórek, sygnalizacja mechaniczna, macierz zewnątrzkomórkowa, integryna, gojenie ran