Clear Sky Science · pl
MUC14 hamuje gruczolakoraka płuca poprzez integrynę α8β6/PI3K/AKT/MAPK modulując odpowiedź na cisplatynę i odporność
Dlaczego to badanie raka płuca ma znaczenie
Gruczolakorak płuca jest najczęstszą postacią raka płuca i często leczony jest chemioterapią z użyciem cisplatyny. Niestety wiele guzów nabywa oporność na ten lek, a pacjenci nadal mają niską przeżywalność w długim okresie. To badanie ujawnia mało znany białkowy składnik powierzchni komórkowej, MUC14, który wydaje się działać jak naturalny hamulec wzrostu nowotworu. Zrozumienie mechanizmów działania MUC14 może otworzyć nowe drogi zwiększające skuteczność chemioterapii oraz wspomóc układ odpornościowy w rozpoznawaniu i atakowaniu komórek nowotworowych.
Ochronne białko widoczne na pierwszy rzut oka
MUC14, zwany również endomucyną, znajduje się na powierzchni komórek i należy do rodziny glikoprotein znanych jako mucyny. Przez analizę dużych publicznych baz danych o nowotworach oraz badanie próbek od pacjentów, autorzy stwierdzili, że guzy gruczolakoraka płuca zwykle produkują znacznie mniej MUC14 niż przylegająca tkanka normalna. Pacjenci, których guzy utrzymywały wyższe poziomy MUC14, żyli dłużej i mieli wolniejszy przebieg choroby niż osoby z niskim poziomem tego białka. W wielu typach nowotworów MUC14 był często tłumiony, co sugeruje, że częściej pełni rolę blokera guza niż jego promotora. 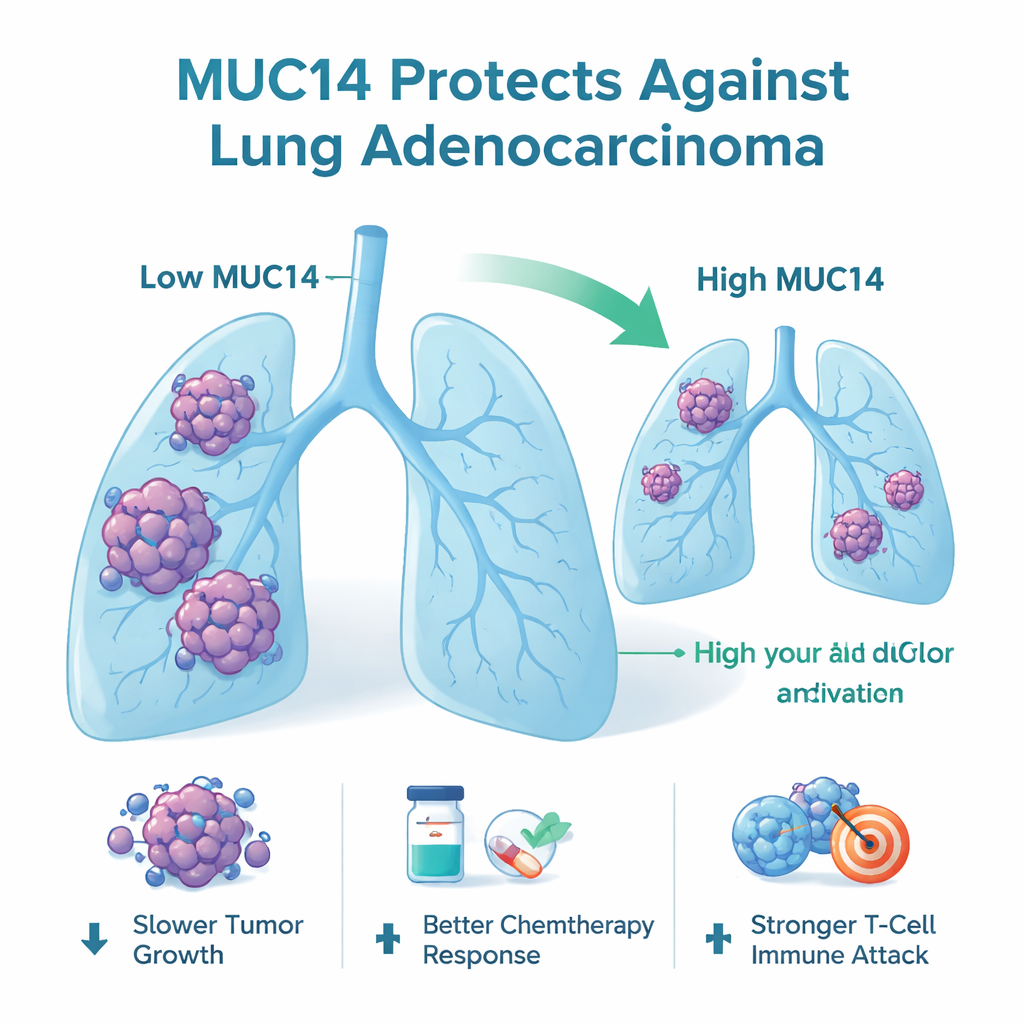
Spowalnianie komórek rakowych i zmniejszanie guzów
Aby sprawdzić, co MUC14 robi w praktyce, zespół manipulował jego poziomem w liniach komórkowych raka płuca. Gdy wymusili nadprodukcję MUC14, komórki dzieliły się wolniej, mniej migrowały i miały mniejszą zdolność inwazji przez żel naśladujący tkankę. Miały też trudności z przyczepianiem się do kluczowych cząsteczek rusztowania i tworzyły mniej oraz mniejsze kolonie. U myszy komórki nowotworowe przeprogramowane do nadprodukcji MUC14 tworzyły mniejsze guzy podskórne i powodowały mniej przerzutów do płuc po wstrzyknięciu do krwiobiegu. Gdy natomiast MUC14 został wyciszony za pomocą małych interferujących RNA, zaobserwowano odwrotny efekt: komórki rosły szybciej, poruszały się więcej, lepiej przylegały i tworzyły więcej kolonii — wszystkie te cechy wskazują na bardziej złośliwe zachowanie nowotworu.
Odcinanie sygnałów wzrostu na powierzchni komórki
Autorzy zbadali następnie, w jaki sposób MUC14 wywiera te silne efekty. Skoncentrowali się na integrynach, rodzinie receptorów, które kotwiczą komórki w otoczeniu i przekazują sygnały wzrostu oraz przeżycia do wnętrza komórki. Dane z setek guzów płuca wskazały na silne powiązanie między MUC14 a dwoma podjednostkami integryn, oznaczonymi jako α8 i β6, które łączą się w kompleks na powierzchni komórkowej. Przy użyciu techniki optycznej wykrywającej białka w odległościach rzędu miliardowych części metra, badacze potwierdzili, że MUC14 i kompleks integryny α8β6 występują obok siebie w błonie komórkowej. Nadmiar MUC14 zaburzał gromadzenie się tych integryn i osłabiał dwie główne ścieżki wzrostu, które normalnie przez nie przechodzą: PI3K/AKT i MAPK/ERK. Gdy MUC14 było zmniejszone, te szlaki stawały się bardziej aktywne, co pomaga wyjaśnić, dlaczego komórki nowotworowe szybciej rosły i szerzyły się.
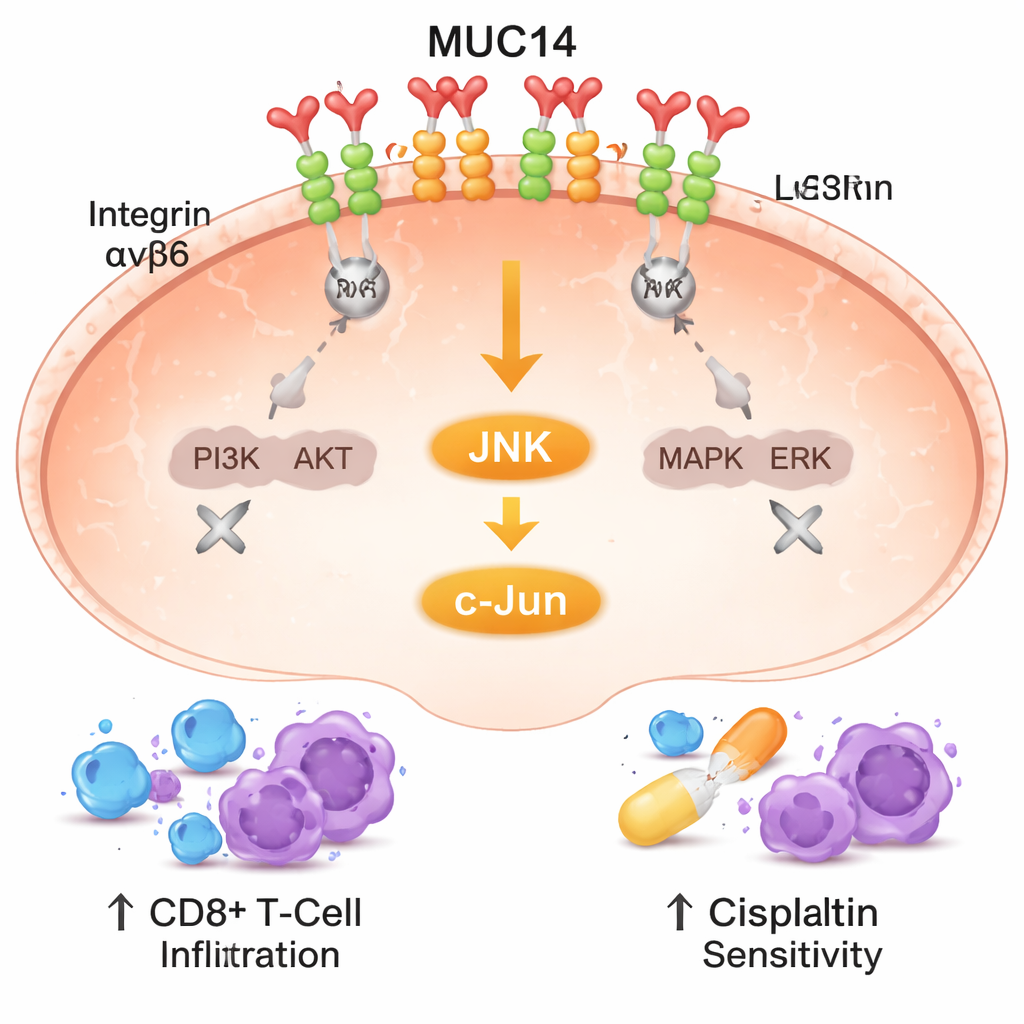
Wspieranie współdziałania układu odpornościowego i chemioterapii
Los choroby zależy nie tylko od samych komórek nowotworowych, lecz także od otaczających je komórek odpornościowych. Analizując bazy danych z profilowaniem odporności oraz barwiąc ludzkie fragmenty guza, zespół odkrył, że nowotwory z wyższym poziomem MUC14 zawierały więcej komórek T CD3+ i CD8+ — komórek odpornościowych zdolnych bezpośrednio niszczyć komórki rakowe — zgromadzonych w pobliżu regionów nowotworu pozytywnych na MUC14. To sugeruje, że MUC14 pomaga tworzyć środowisko sprzyjające atakowi immunologicznemu. Badacze zbadali również cisplatynę, powszechnie stosowany lek w gruczolakoraku płuca. W hodowlach komórkowych guzy z nadmiarem MUC14 wymagały znacznie niższych dawek cisplatyny, aby zostać zahamowane, podczas gdy komórki pozbawione MUC14 stawały się bardziej oporne na lek. Co istotne, MUC14 nie powodowało po prostu większej skłonności komórek do obumierania w stanie spoczynkowym; zamiast tego wzmacniało efekt zabijający cisplatyny, częściowo przez aktywację szlaku stresowego JNK/c-Jun uruchamianego przez uszkodzenia DNA.
W kierunku mądrzejszych kombinacji w leczeniu raka płuca
Mówiąc wprost, praca przedstawia MUC14 jako wbudowany system obronny przeciwko gruczolakorakowi płuca. Obecność tego białka blokuje kluczowe przełączniki wzrostu na powierzchni komórki, spowalnia rozsiew nowotworu, przyciąga komórki T zwalczające nowotwór i sprawia, że leczenie cisplatyną działa silniej bez dodatkowego uszkodzenia narządów w testach na zwierzętach. Gdy MUC14 zostaje utracone, guzy stają się bardziej odporne, bardziej ruchome i mniej wrażliwe na standardowe terapie. Wyniki sugerują, że pomiar poziomu MUC14 mógłby pomóc przewidywać rokowanie i odpowiedź na leczenie, a przyszłe terapie mające na celu zwiększenie aktywności MUC14 — lub naśladowanie jego wpływu na sygnalizację integryn — mogłyby pozwolić lekarzom na skuteczniejsze łączenie chemioterapii i immunoterapii u pacjentów z zaawansowanym rakiem płuca.
Cytowanie: Li, X., Li, M., Huang, S. et al. MUC14 suppresses lung adenocarcinoma via integrin α8β6/PI3K/AKT/MAPK modulating cisplatin response and immunity. Sci Rep 16, 7784 (2026). https://doi.org/10.1038/s41598-026-39019-z
Słowa kluczowe: gruczolakorak płuca, MUC14, oporność na cisplatynę, sygnalizacja integryn, odporność przeciwnowotworowa