Clear Sky Science · pl
Peptyd z pyłku pszczelego o podwójnym hamowaniu DPP‑IV i modulacji transportu glukozy
Dlaczego pyłek pszczeli może mieć znaczenie dla poziomu cukru
Cukrzycę typu 2 często opisuje się jako problem nadmiaru cukru i niedoboru insuliny, ale za kulisami sieć enzymów i transporterów dyskretnie kieruje tym, jak organizm obchodzi się z glukozą. W badaniu tym eksplorowano intrygującą hipotezę: że pyłek pszczeli, naturalne „superżywność”, może być źródłem drobnych fragmentów białek (peptydów), które zarówno chronią sygnały hormonalne kontrolujące poziom cukru, jak i łagodnie modulują, jak cukier jest wchłaniany z jelit. Praca koncentruje się na jednym takim peptydzie, nazwanym AA‑7, i bada, czy mógłby on stać się inspiracją dla bezpieczniejszych, opartych na żywności strategii wspomagających kontrolę cukrzycy.
Ze ula na ławę laboratoryjną
Pyłek pszczeli to mieszanina pyłków roślinnych i materiałów pochodzenia pszczelego, bogata w białka, witaminy i inne składniki odżywcze. Aby naśladować trawienie u człowieka, badacze potraktowali białka z pyłku enzymami trawiennymi — pepsyną i pancreatyną — podobnymi do tych występujących w żołądku i jelicie cienkim. Proces ten rozbił duże białka na wiele mniejszych fragmentów, niektóre zaledwie kilka aminokwasów długości. Następnie rozdzielili te fragmenty według rozmiaru i właściwości chemicznych, testując każdą frakcję pod kątem zdolności blokowania enzymu DPP‑IV, który normalnie rozcina i unieszkodliwia hormony stymulujące wydzielanie insuliny. Wyodrębniona frakcja bardzo małych, względnie oleistych (hydrofobowych) peptydów wyróżniała się silnym działaniem hamującym DPP‑IV. 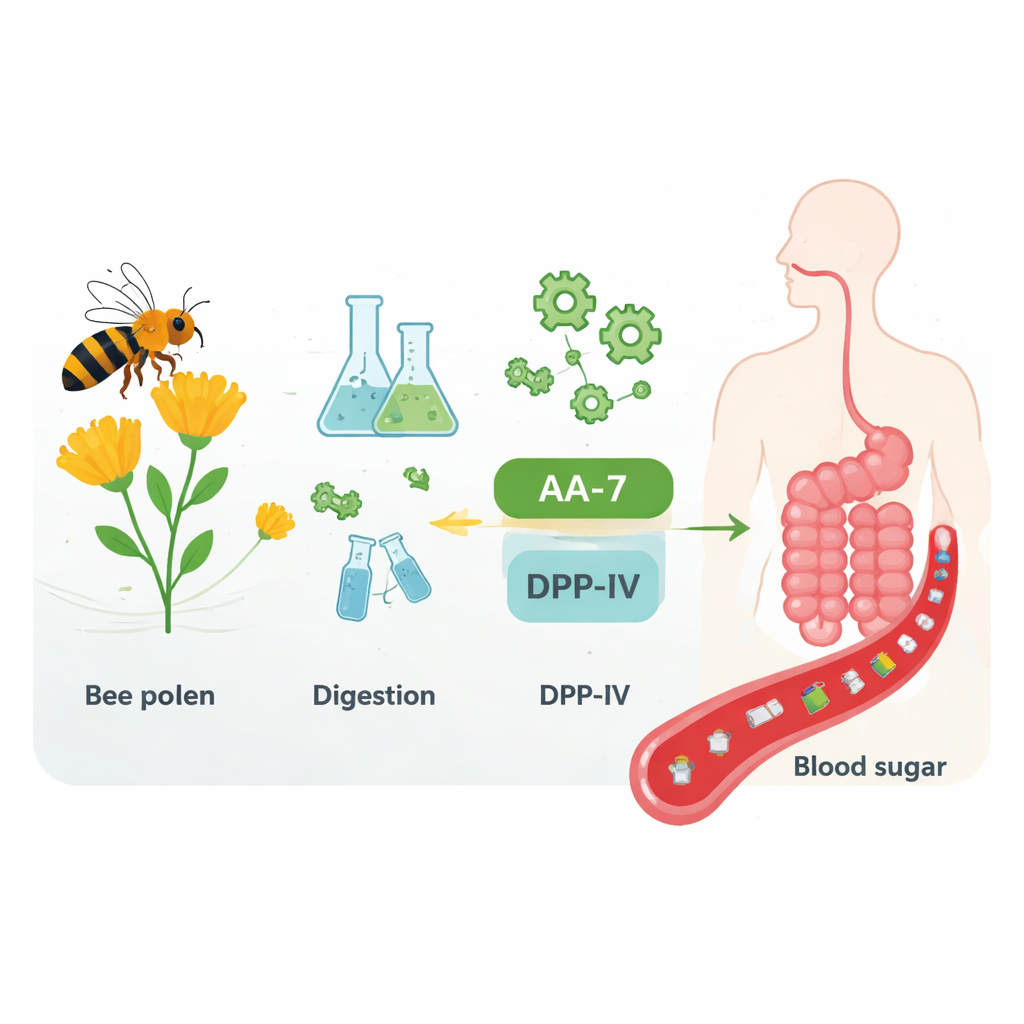
Odnalezienie wyróżniającego się peptydu
Przy użyciu spektrometrii mas o wysokiej rozdzielczości zespół zidentyfikował siedmioaminokwasowy peptyd o sekwencji Ala‑Thr‑His‑Ala‑Leu‑Leu‑Ala, który nazwano AA‑7. Peptyd ten został zsyntezowany, aby przetestować go w izolacji. W testach enzymatycznych AA‑7 hamował DPP‑IV w stężeniach mikromolowych, nieco słabiej niż standardowy lek laboratoryjny, ale porównywalnie lub lepiej niż wiele peptydów pochodzenia żywnościowego opisanych w literaturze naukowej. Analiza zmian szybkości reakcji przy różnych ilościach peptydu i substratu wykazała, że AA‑7 działa jako inhibitor konkurencyjny: zajmuje tę samą kieszeń aktywną DPP‑IV, której używają naturalne substraty, blokując dostęp bez niszczenia enzymu.
Interakcje peptyd–enzym w szczegółach atomowych
Aby zrozumieć, dlaczego AA‑7 działa, badacze użyli symulacji komputerowych do zadokowania peptydu w trójwymiarowym modelu DPP‑IV, a następnie uruchomili symulacje dynamiki molekularnej w czasie. Modele sugerowały, że AA‑7 osiada w kieszeni katalitycznej enzymu, kontaktując kluczowe aminokwasy znane z istotnego znaczenia dla aktywności DPP‑IV. Przewidywano, że wiązanie jest co najmniej tak stabilne, jak wiązanie inhibitora referencyjnego. Dalsze analizy komputerowe właściwości ADMET (wchłanianie, dystrybucja, metabolizm, toksyczność) wskazały realistyczne ostrzeżenie: AA‑7 prawdopodobnie jest bezpieczny, ale nie jest efektywnie wchłaniany przez ścianę jelita w formie niezmienionej, co jest częstym ograniczeniem małych peptydów. To sugeruje konieczność strategii dostarczania lub modyfikacji strukturalnych, jeśli AA‑7 lub cząsteczki na jego wzór miałyby być stosowane u ludzi.
Regulacja sposobu, w jaki jelito radzi sobie z cukrem
Badanie nie ograniczyło się do enzymów w probówkach. Zespół poddał hodowane ludzkie komórki jelitowe (komórki Caco‑2) działaniu AA‑7 i zmierzył zarówno pobieranie glukozy, jak i aktywność genów kodujących dwa główne jelitowe transportery glukozy, SGLT1 i GLUT2. Przy dawkach nietoksycznych AA‑7 zmieniał tempo, w jakim fluorescencyjna forma glukozy wchodziła do komórek, przy czym efekt zależał od dawki i czasu. Również wpływał na poziomy ekspresji genów SGLT1 i GLUT2 w różny sposób w krótkich (30 minut) i dłuższych (24 godziny) przedziałach czasowych. Dokowanie komputerowe sugerowało, że AA‑7 może wchodzić w interakcje z częściami strukturalnymi tych transporterów, choć modele te należy traktować jako hipotezy, a nie ostateczny dowód. Razem dane z komórek i modelowania wskazują, że AA‑7 robi coś więcej niż hamuje DPP‑IV — delikatnie modyfikuje też mechanizmy przenoszenia cukru z jelita do krwi. 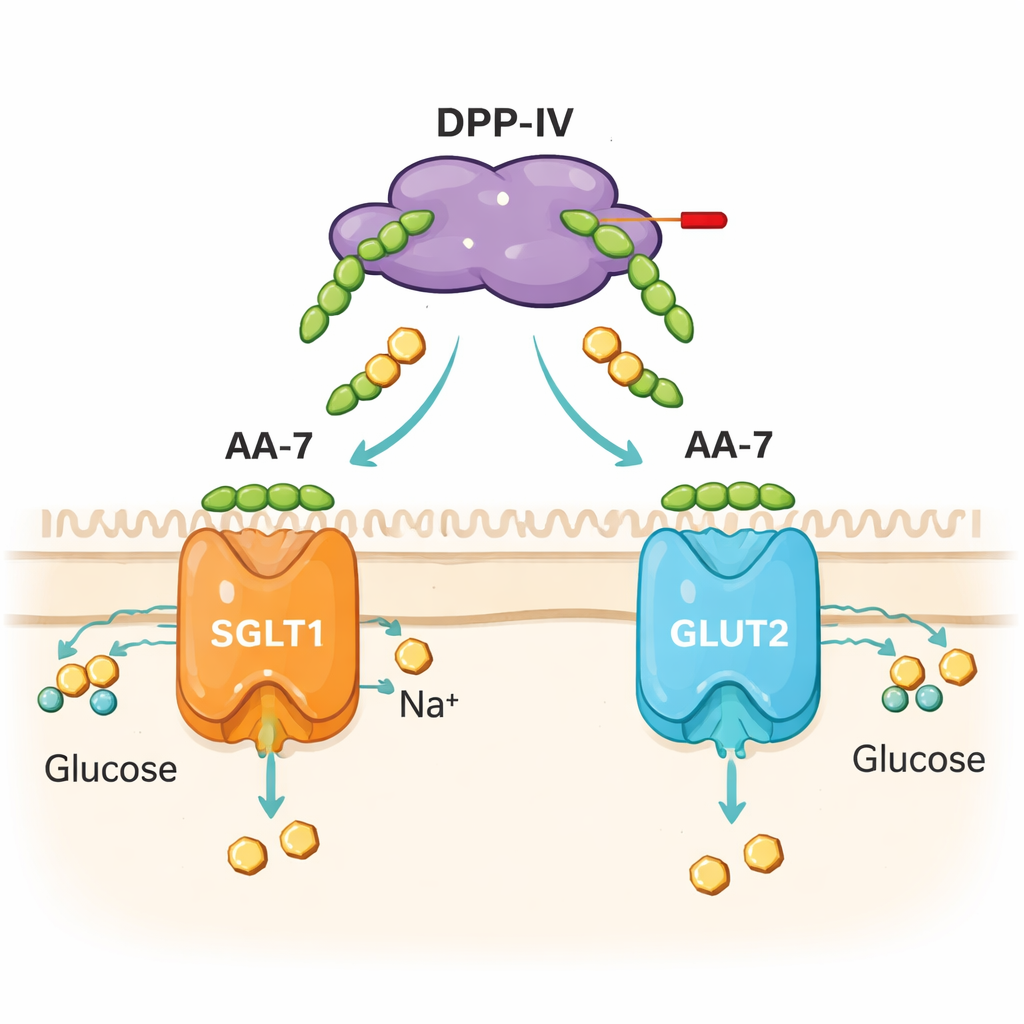
Co to może znaczyć dla przyszłej żywności
Dla czytelnika niebędącego specjalistą kluczowy wniosek brzmi: peptyd z pyłku pszczelego AA‑7 wydaje się działać na dwóch frontach istotnych dla cukrzycy typu 2 — spowalnia kluczowy enzym rozkładający hormony stymulujące insulinę oraz wpływa na to, jak komórki jelitowe pobierają glukozę. Sam AA‑7 nie jest jeszcze gotowy, by stać się lekiem czy suplementem, częściowo dlatego, że może być słabo wchłaniany. Wskazuje jednak, że pyłek pszczeli — a być może inne produkty bogate w białko — mogą być rezerwuarem małych, wielozadaniowych peptydów, które mogą inspirować nowe żywności funkcjonalne lub peptydowe terapie. Przy dalszych badaniach na zwierzętach i ludziach oraz lepszych metodach dostarczania takich peptydów, tego rodzaju cząsteczki o podwójnym działaniu mogłyby stać się elementem bardziej zniuansowanego, opartego na żywności podejścia do utrzymania prawidłowego poziomu glukozy we krwi.
Cytowanie: Mongkolnkrajang, U., Kuptawach, K., Sangtanoo, P. et al. Bee pollen-derived peptide with dual DPP-IV Inhibition and glucose transport modulation. Sci Rep 16, 7616 (2026). https://doi.org/10.1038/s41598-026-39009-1
Słowa kluczowe: peptydy z pyłku pszczelego, inhibicja DPP‑IV, transport glukozy, cukrzyca typu 2, żywność funkcjonalna