Clear Sky Science · pl
Modelowanie oparte na strukturze ujawnia molekularne podstawy nowej aktywności CYP153A6 wobec pochodnych toluenu
Powierzyć trudne zadania chemii naturze
Chemicy i przemysł polegają na reakcjach, które wprowadzają tlen do opornych wiązań węgiel–wodór, na przykład przy oczyszczaniu zanieczyszczeń lub w syntezie składników leków i zapachów. Wykonanie tego w sposób czysty, bez ostrych chemikaliów czy odpadów metali ciężkich, jest trudne. W tym badaniu przyjrzano się naturalnemu katalizatorowi — enzymowi CYP153A6 z bakterii glebowej — i zadano proste pytanie o dalekosiężnych konsekwencjach: czy ten enzym można pokierować, by selektywnie „ulepszał” związki podobne do toluenu — powszechne składniki paliw i rozpuszczalników — przekształcając je w produkty bardziej użyteczne i przyjazne dla środowiska?
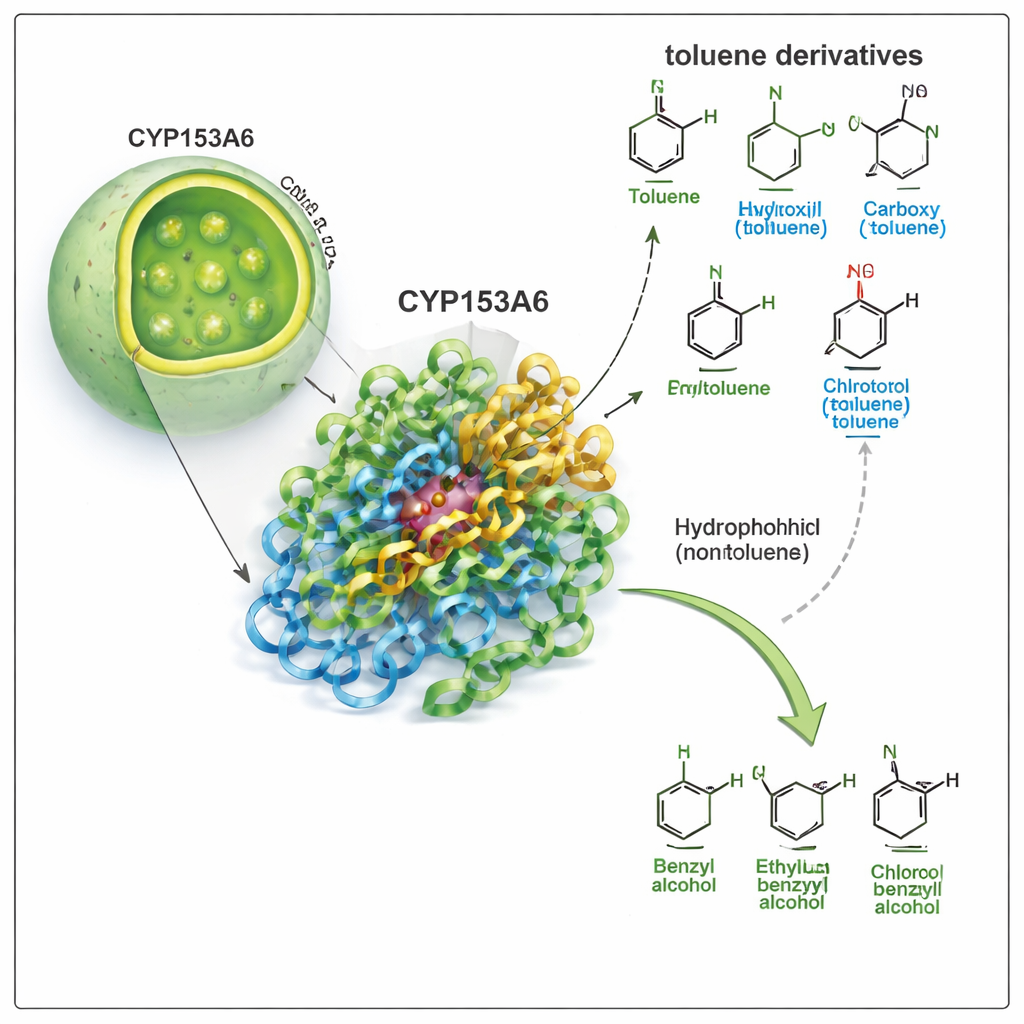
Enzym, który wybiera jedno konkretne miejsce
CYP153A6 należy do dużej rodziny cytochromów P450, wszechstronnych specjalistów od utleniania w przyrodzie. W przeciwieństwie do wielu katalizatorów przemysłowych, ten enzym działa w wodzie, w umiarkowanej temperaturze i wybiera bardzo konkretne pozycje w cząsteczce. Wcześniejsze badania wykazały, że CYP153A6 wprowadza tlen na końcach łańcuchów węglowodorowych oraz w niektórych roślinnych molekułach zapachowych. Tutaj autorzy sprawdzają, czy może on również atakować pozycję benzyliczną — mały łańcuch boczny przy pierścieniu benzenowym — w toluenie i związkach pokrewnych. Ta przemiana zamienia pochodne toluenu w alkohole benzylowe, cenne cegiełki do syntezy farmaceutyków, aromatów i chemii specjalistycznej.
Testowanie, które cząsteczki enzym lubi
Zespół najpierw przeprowadził eksperymenty biotransformacji przy użyciu zmodyfikowanych komórek E. coli produkujących CYP153A6, zarówno jako całe komórki, jak i ekstrakty bezkomórkowe. Narażono enzym na panel pochodnych toluenu, zmieniając grupę przy pierścieniu aromatycznym (takie jak metyl, chlor, metoksy, hydroksyl czy nitro) oraz jej położenie (para, meta lub orto). Enzym sprawował się bardzo dobrze w przypadku związków apolarnych lub słabo polarowych, takich jak p-cymen, p-ksylen, p-metylanizol i p-chlorotoluen, konsekwentnie przekształcając benzyliczną grupę metylową w alkohol benzylowy. Co istotne, całkowicie zignorował silniej polarne związki, takie jak p-krezol, p-metyloalkohol benzylowy czy p-nitrotoluen, mimo że są strukturalnie podobne. Ten wzorzec sugeruje, że kieszeń enzymu jest silnie hydrofobowa i nie sprzyja grupom polarnym.
Budowa trójwymiarowej mapy tej molekularnej maszyny
Ponieważ trójwymiarowa struktura CYP153A6 nie była rozwiązana eksperymentalnie, badacze zbudowali wysokiej jakości model komputerowy, wykorzystując blisko spokrewniony P450 o znanej strukturze. Zwalidowali model, sprawdzając jego geometrię i prowadząc długie symulacje dynamiki molekularnej, aby zobaczyć, czy białko pozostaje stabilne w czasie — co potwierdziły symulacje. Odkryły one ukryte miejsce aktywne połączone z zewnętrzem wąskimi tunelami, przez które wchodzą substraty, a wychodzą produkty. Tunelami tymi kształtują i zamykają ruchome pętle na powierzchni białka, co pomaga wyjaśnić, jak enzym prowadzi hydrofobowe molekuły do reaktywnego centrum z żelazem hemu, jednocześnie pozwalając na ucieczkę wody i utlenionych produktów.
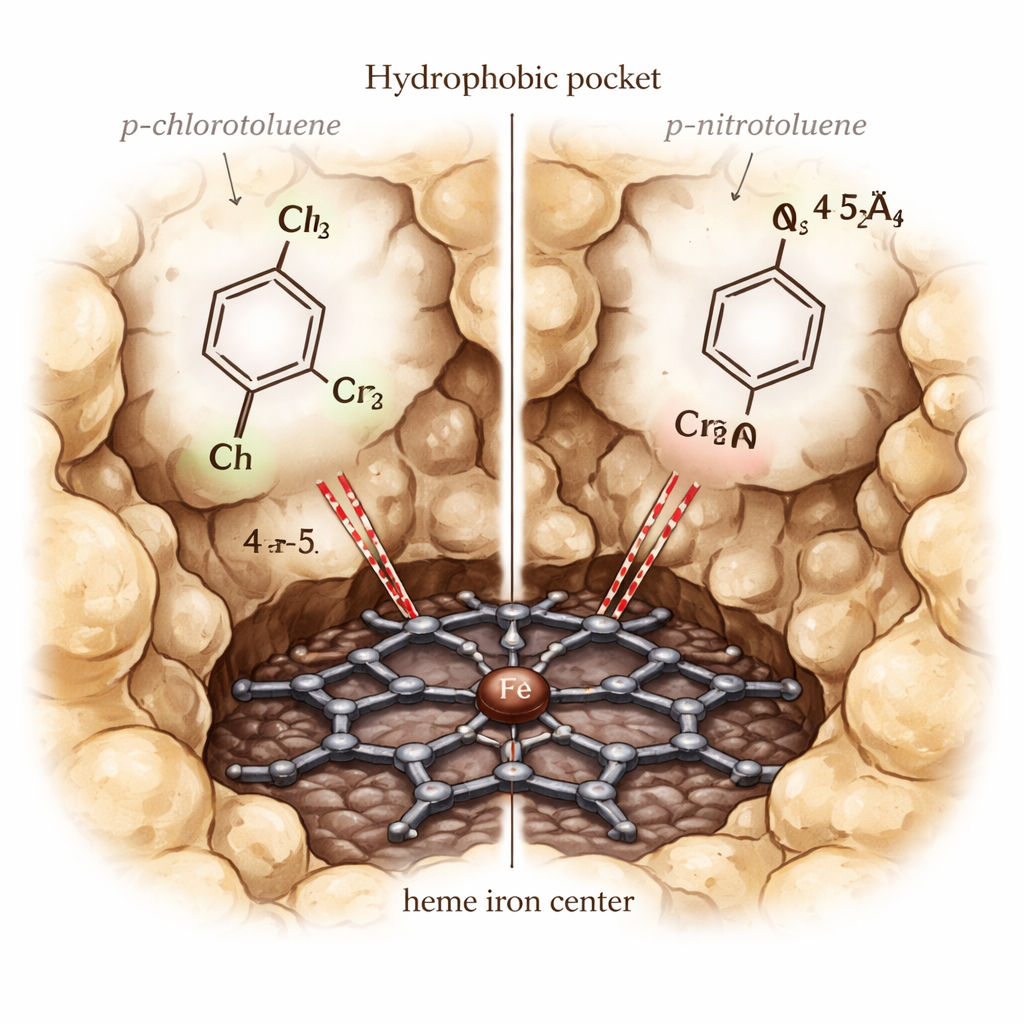
Obserwowanie, jak molekuły dokują, poruszają się i reagują
Mając model, autorzy symulowali, jak różne pochodne toluenu wiążą się wewnątrz CYP153A6. Użyli podejścia zwanego układaniem w zespole (ensemble docking), próbując wielu nieco różnych kształtów białka i kilku stanów elektronowych żelaza hemu, aby zidentyfikować konfiguracje najlepiej odróżniające prawdziwe substraty od niesubstratów. Zwycięska konstelacja używała żelaza w stanie spoczynkowym ferrycznym i bez dodatkowych cząsteczek wody w kieszeni, i poprawnie faworyzowała znane substraty. Kolejne symulacje śledziły, klatka po klatce, jak każda cząsteczka ustawiała się względem hemu. Dobre substraty, takie jak p-cymen i p-ksylen, utrzymywały się blisko żelaza z benzyliczną grupą metylową skierowaną ku niemu, a ich przewidywane energie wiązania były wyraźnie korzystne. Słabe substraty miały tendencję do odpływania, przyjmowania niezręcznych orientacji lub niekorzystnych interakcji z głównie „oleistymi” łańcuchami bocznymi wyścielającymi kieszeń.
Dlaczego jeden sobowtór reaguje, a inny nie
Pojawiła się jedna zagadka: p-chlorotoluen jest efektywnie utleniany przez CYP153A6, podczas gdy p-nitrotoluen nie, mimo że oba mieszczą się w kieszeni i w symulacjach wiążą się z podobną siłą. Aby to wyjaśnić, autorzy przeprowadzili bardziej szczegółowe obliczenia mechaniki kwantowej/klasycznej (QM/MM) na wysoce reaktywnym stanie „Kompleks I” enzymu. Obliczenia wykazały, że grupa nitrowa tak silnie odciąga gęstość elektronową z atomu węgla benzylicznego, że utlenienie tego węzła staje się bardzo trudne, mimo odpowiedniej geometrii. Natomiast grupa chloro pozwala na lepszą komunikację elektronową między hemem a substratem, co odzwierciedla się w wyższej gęstości spinowej na pierścieniu aromatycznym i grupie metylowej oraz w bardziej reaktywnym ustawieniu do krytycznego kroku abstrakcji wodoru.
Co to znaczy dla czystszej chemii
Mówiąc prościej, CYP153A6 zachowuje się jak mała, oleista rękawiczka, która trzyma niektóre molekuły przypominające paliwa w taki sposób, że tlen może być dodany w konkretnym miejscu — przekształcając je w związki bardziej rozpuszczalne w wodzie, użyteczne i ostatecznie łatwiejsze do degradacji. Badanie pokazuje, że enzym preferuje podstawnik niepolarny oraz że zarówno kształt, jak i przepływ elektronów decydują, czy dana pochodna toluenu zostanie przekształcona. Poprzez wyjaśnienie, jak CYP153A6 rozpoznaje i aktywuje te cząsteczki, praca dostarcza planu do inżynieryjnego udoskonalania enzymu, które mogłoby pomóc w oczyszczaniu zanieczyszczeń aromatycznych lub w bardziej zrównoważonej produkcji złożonych chemikaliów.
Cytowanie: Wei, Y., Donzella, S., Foiadelli, S. et al. Structure-based modeling reveals molecular basis for CYP153A6’s novel activity toward toluene derivatives. Sci Rep 16, 7570 (2026). https://doi.org/10.1038/s41598-026-38986-7
Słowa kluczowe: biokataliza, cytochrom P450, hydroksylacja toluenu, inżynieria enzymów, zielona chemia