Clear Sky Science · pl
Transplastomiczna biofabryka do produkcji funkcjonalnej ludzkiej α‑laktoalbuminy do zastosowań żywieniowych i terapeutycznych
Przekształcanie roślin w wytwórnie białek mlecznych
Współczesne diety w dużej mierze opierają się na białkach mleka, ale hodowla krów na światową skalę wiąże się z kosztami dla środowiska i pytaniami etycznymi. W tym badaniu pokazano bardzo odmienny sposób wytwarzania kluczowego białka mleka ludzkiego — ucząc liście roślin produkcji tego białka. Praca dowodzi, że tytoń można przeprogramować tak, by wytwarzał ludzką α‑laktoalbuminę, białko ważne dla żywienia niemowląt i mające potencjalne właściwości przeciwnowotworowe, otwierając drogę do składników formulek bez udziału zwierząt oraz nowych żywnościowych komponentów przeciwnowotworowych.
Dlaczego to białko mleczne ma znaczenie
Mleko matki to więcej niż pożywienie; to precyzyjnie zestrojona mieszanka białek, tłuszczów i cukrów, która zmienia się wraz z potrzebami niemowlęcia. Jednym z najważniejszych białek jest α‑laktoalbumina, która pomaga w syntezie laktozy — głównego cukru w mleku i krytycznego źródła energii dla niemowląt. α‑Laktoalbumina jest bogata w egzencjalne aminokwasy, w tym tryptofan, prekursor „dobrego samopoczucia” — serotoniny, i powiązano ją z lepszą odpornością na stres oraz potencjalną ochroną przed niektórymi nowotworami. Ponieważ jest łatwo przyswajalna, ma łagodny smak i pozostaje stabilna w szerokim zakresie kwasowości, jest szeroko stosowana w formułach dla niemowląt i napojach odżywczych — a popyt rośnie.
Problem z tradycyjnym mleczarstwem
Poleganie na krów jako źródle białek mleka ma wady. Zwierzęta gospodarskie odpowiadają za znaczną część globalnych emisji gazów cieplarnianych, a duże gospodarstwa mleczne wymagają ogromnych ilości ziemi, wody i paszy. Dodatkowo zarządzanie hodowlą może rodzić obawy dotyczące hormonów, antybiotyków i patogenów trafiających do łańcucha mlecznego. Te naciski pobudziły zainteresowanie podejściami „rolnictwa komórkowego”, gdzie białka mleczne wytwarzają mikroby lub hodowane komórki zamiast zwierząt. Jednak wiele z tych systemów wciąż jest kosztownych, trudnych do skalowania lub produkuje białka nie do końca identyczne z ludzkimi wersjami. Rośliny, a w szczególności ich chloroplasty — drobne zielone fabryki fotosyntezy — oferują obiecującą alternatywną platformę.
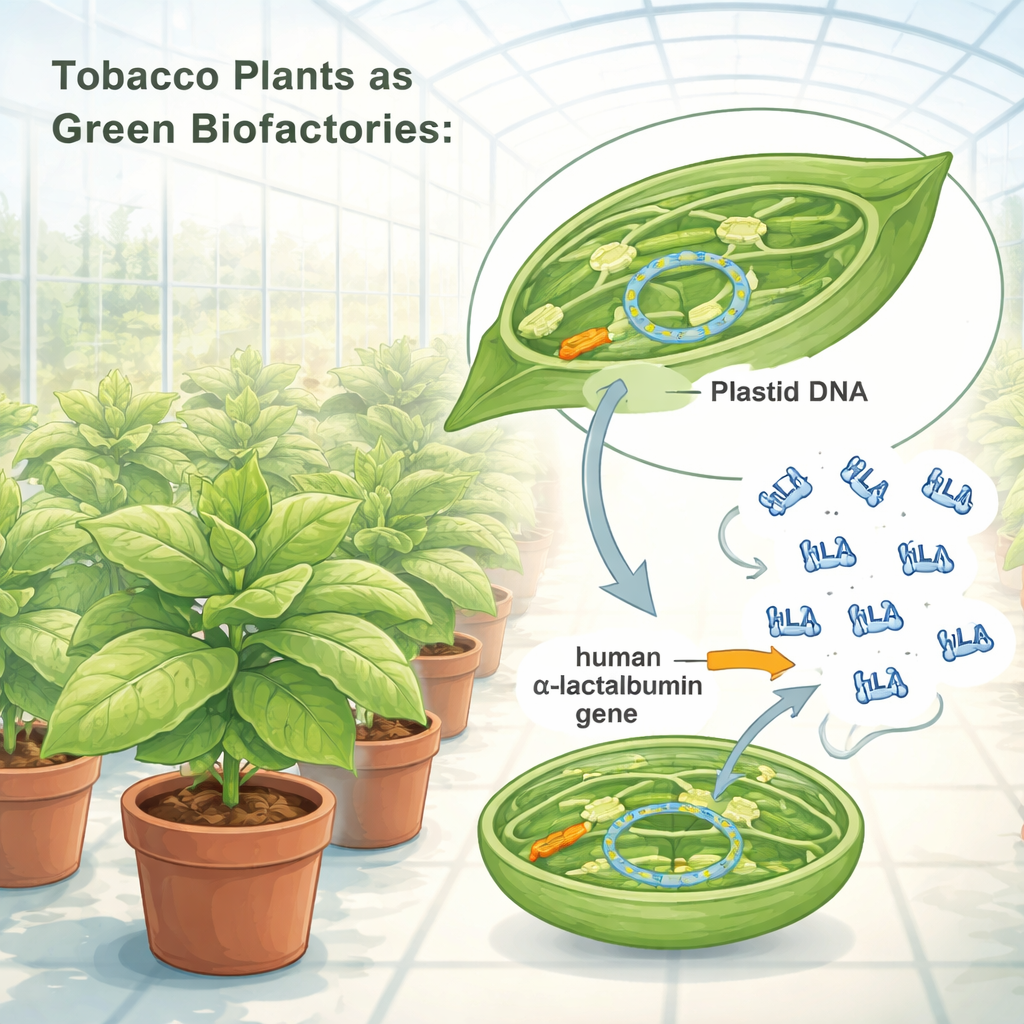
Przeprogramowanie chloroplastów na biofabryki
Naukowcy przeprojektowali instrukcje genetyczne dla ludzkiej α‑laktoalbuminy tak, aby chloroplasty tytoniu mogły je wydajnie odczytywać. Wstawili zoptymalizowany gen do DNA chloroplastów, używając „kasety genowej” zbudowanej z silnych roślinnych elementów regulacyjnych działających jak potężne włączniki. Metodą bombardowania cząsteczkowego dostarczyli tę kasetę do komórek liści tytoniu, a następnie wyselekcjonowali siewki, których chloroplasty w pełni przyjęły nowy gen. Testy genetyczne potwierdziły, że wszystkie kopie DNA chloroplastów w tych roślinach zawierały teraz plan budowy ludzkiego białka. Zmodyfikowane rośliny rosły normalnie w warunkach szklarniowych, wydając nasiona i nie wykazując widocznych strat w wielkości, kształcie ani płodności, co sugeruje, że dodatkowe obciążenie białkowe nie zaszkodziło zdrowiu roślin.
Dowód, że białko produkowane przez roślinę działa
Następnie zespół sprawdził, czy roślinna α‑laktoalbumina zachowuje się jak autentyczne ludzkie białko. Wyizolowali rozpuszczalne białka z liści, oczyścili α‑laktoalbuminę i przebadali jej strukturę techniką ukazującą sposób fałdowania białek. Widmo — swoisty „odcisk palca” białka pochodzącego z rośliny — prawie pokrywało się z widmem komercyjnej ludzkiej α‑laktoalbuminy, co wskazuje na podobne fałdowanie. Funkcjonalnie roślinne białko aktywowało enzym syntetyzujący laktozę niemal tak samo dobrze jak natywna wersja, napędzając tworzenie laktozy w około 93% szybkości standardowego białka. Co istotne, α‑laktoalbumina akumulowała się do około 23% wszystkich rozpuszczalnych białek w liściach — jeden z najwyższych poziomów zgłaszanych dla ludzkich białek wytwarzanych w chloroplastach roślin — co sugeruje, że system ten może dostarczyć wydajności istotnych przemysłowo.
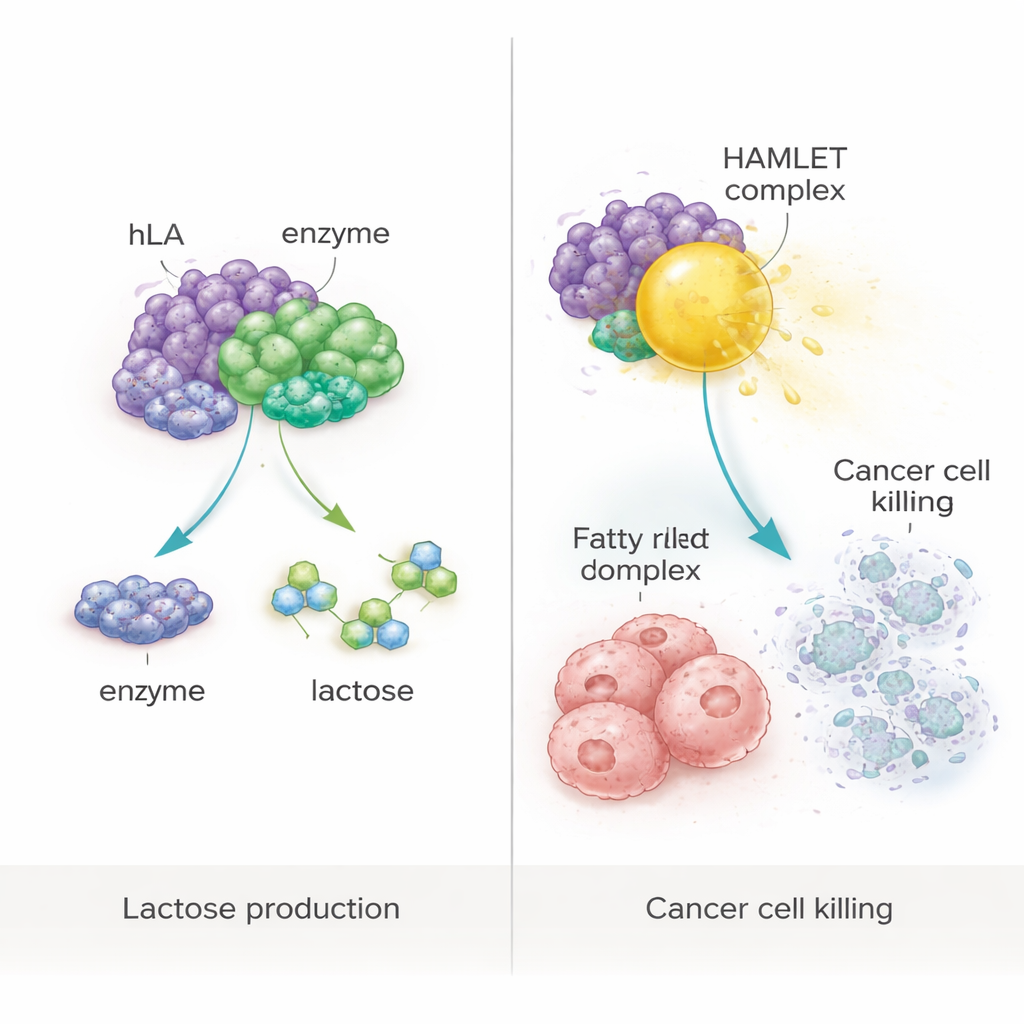
Od żywienia do kompleksów walczących z rakiem
Badanie przetestowało także bardziej ambitny pomysł: użycie roślinnego białka jako cegiełki do znanego kompleksu przeciwnowotworowego HAMLET, powstającego, gdy α‑laktoalbumina ściśle wiąże się z oleiną, powszechnym kwasem tłuszczowym. Poprzez delikatne podgrzewanie oczyszczonego białka z oleiną w kontrolowanych warunkach, badacze stworzyli kompleks przypominający HAMLET. Zastosowany do hodowli ludzkich komórek raka jelita grubego (WiDr) i raka piersi (MCF‑7), ten kompleks drastycznie zmniejszył przeżywalność komórek do poniżej 10%. Analizy uzupełniające wykazały, że większość dotkniętych komórek przechodziła apoptozę — formę zaprogramowanej śmierci komórkowej, a nie niekontrolowanego rozpadu. Co ważne, ani samo białko, ani sam kwas tłuszczowy, ani ekstrakty z niemodyfikowanych roślin nie wywołały istotnej śmierci komórek, potwierdzając, że efekt zabijania komórek zależał od specyficznego kompleksu.
Co to może znaczyć dla przyszłego żywienia i medycyny
Podsumowując, praca pokazuje, że chloroplasty roślinne mogą niezawodnie produkować duże ilości ludzkiego białka mlecznego, które jest zarówno istotne żywieniowo, jak i biologicznie aktywne terapeutycznie. Dla laika oznacza to, że przyszłe formulek dla niemowląt, żywności funkcjonalnej czy suplementów mogłyby być kiedyś produkowane przy użyciu białek hodowanych w liściach zamiast pozyskiwanych od krów, zmniejszając wpływ na środowisko przy jednoczesnym lepszym dopasowaniu do biologii człowieka. Równocześnie to samo białko pochodzące z roślin można przekształcić w laboratorium w ukierunkowany kompleks przeciwnowotworowy, dając dowód na roślinne ścieżki ku przystępnym biologicznym terapiom. Choć potrzebne są dalsze badania potwierdzające bezpieczeństwo i skuteczność u zwierząt i ludzi — oraz przeniesienie tej technologii na jadalne uprawy — badanie daje przekonujący wgląd w możliwość użycia roślin jako mini‑fabryk dla żywienia i medycyny następnej generacji.
Cytowanie: Ehsasatvatan, M., Kohnehrouz, B.B. Transplastomic biofactory for the production of functional human α-lactalbumin for nutritional and therapeutic applications. Sci Rep 16, 7359 (2026). https://doi.org/10.1038/s41598-026-38965-y
Słowa kluczowe: białka mleczne produkowane w roślinach, chloroplastowa biofabryka, ludzka alfa‑laktoalbumina, zrównoważone alternatywy dla produktów mlecznych, terapia przeciwnowotworowa HAMLET