Clear Sky Science · pl
Autofluorescencja i analizy FTIR śledzą dietetyczne fluorofory i ujawniają zanieczyszczenie plastikiem w przewodzie pokarmowym larw komarów
Dlaczego to badanie komarów ma znaczenie
Komary są znane z przenoszenia chorób, lecz zanim w ogóle ugryzą, spędzają dni jako drobne larwy żerujące w zbiornikach z wodą. Te wczesne stadia są motorem wzrostu komarów i stanowią ważny cel strategii kontroli. Badanie pokazuje, jak naukowcy mogą „widzieć”, co larwy jedzą — bez dodawania barwników — i nawet wykrywać ślady plastiku, które cicho uwalniają się z powszechnych laboratoryjnych naczyń do ich jelit. Wnioski są istotne zarówno przy projektowaniu bezpieczniejszych metod zwalczania komarów, jak i przy zrozumieniu, jak zanieczyszczenie mikroplastikiem może przemieszczać się przez małe organizmy wodne.
Świecące wskazówki w mikroskopijnych ciałach
Wiele naturalnych cząsteczek słabo świeci pod wpływem określonych barw światła — to zjawisko zwane autofluorescencją. Naukowcy wykorzystali ten wrodzony blask do śledzenia pokarmu u larw tygrysiego komara azjatyckiego, ważnego wektora chorób. Przy użyciu potężnych mikroskopów i obrazowania spektralnego badali komercyjne pożywienie dla larw, ich jelita oraz cienkie skrawki tkanek. Cząstki pokarmu wykazywały dwa główne sygnały świetlne: szerokie niebieskawe pasmo pochodzące od materiałów bogatych w białko oraz ostre czerwone pasmo od pigmentów związanych z chlorofilem pochodzących z roślin i glonów. Gdy larwy spożywały ten pokarm, zawartość ich jelit pokazywała te same sygnatury, co potwierdza, że te sygnały świetlne mogą służyć jako naturalne markery tego, co zostało połknięte.
Pigmenty pokarmowe przemieszczają się poza jelito
Przybliżając obserwacje mikroskopią konfokalną, zespół odkrył coś bardziej zaskakującego: czerwony sygnał podobny do chlorofilowego nie ograniczał się do światła jelitowego. Pojawiał się także w otaczającej jamie ciała, ale nie w zewnętrznej kutykuli. Ten wzorzec sugeruje, że niektóre pigmenty pochodzące z pokarmu przetrwają trawienie i przechodzą do wewnętrznych płynów ustrojowych, potencjalnie gromadząc się w innych tkankach. Ten sam czerwony emisję wykryto także w wodzie, w której hodowano larwy, mimo że była nieobecna w wodzie zawierającej jedynie pokarm. Wskazuje to, że larwy pobierają związki powiązane z chlorofilem i później wydalają część z nich z powrotem do środowiska, co daje możliwość śledzenia, jak naturalnie fluorescencyjne składniki diety krążą w organizmie i jego habitatcie.
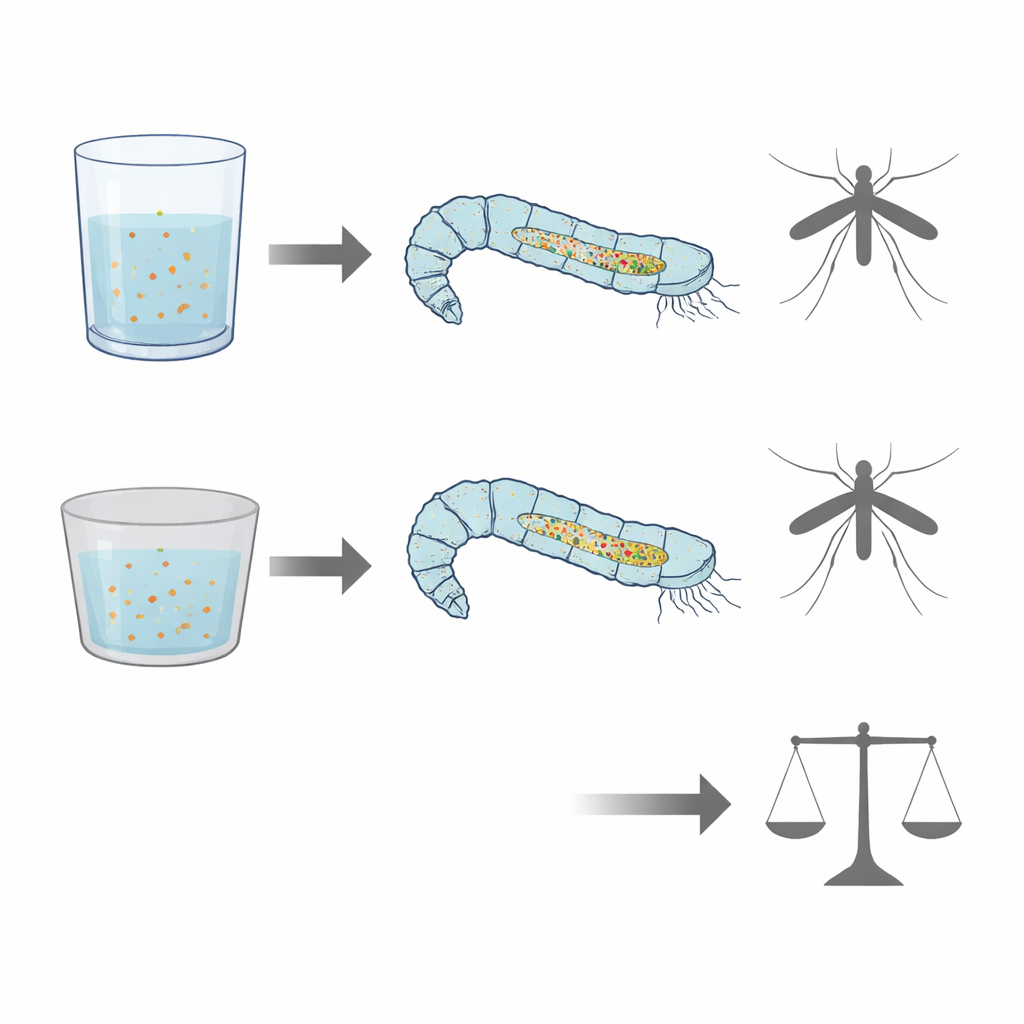
Materiał pojemnika zmienia to, co larwy przyswajają
Aby sprawdzić, jak środowisko hodowli może wpływać na karmienie, larwy hodowano albo w szklanych naczyniach, albo w naczyniach z polistyrenu przy identycznych warunkach. Ogólny blask od pokarmu w jelicie był konsekwentnie silniejszy i bardziej obfity u larw z plastikowych pojemników niż u tych ze szkła, co sugeruje różnice w ilości lub wydajności pobieranego i przetwarzanego pokarmu. Pomiary spektrofluorymetryczne wody otaczającej wykazały zmiany innej grupy fluorescencyjnych związków — flawin, związanych z metabolizmem energetycznym i witaminami z grupy B. Te przesunięcia sugerują, że larwy wychowywane w różnych materiałach pojemników mogą inaczej gospodarować niektórymi składnikami odżywczymi, nawet jeśli ich dieta była taka sama.
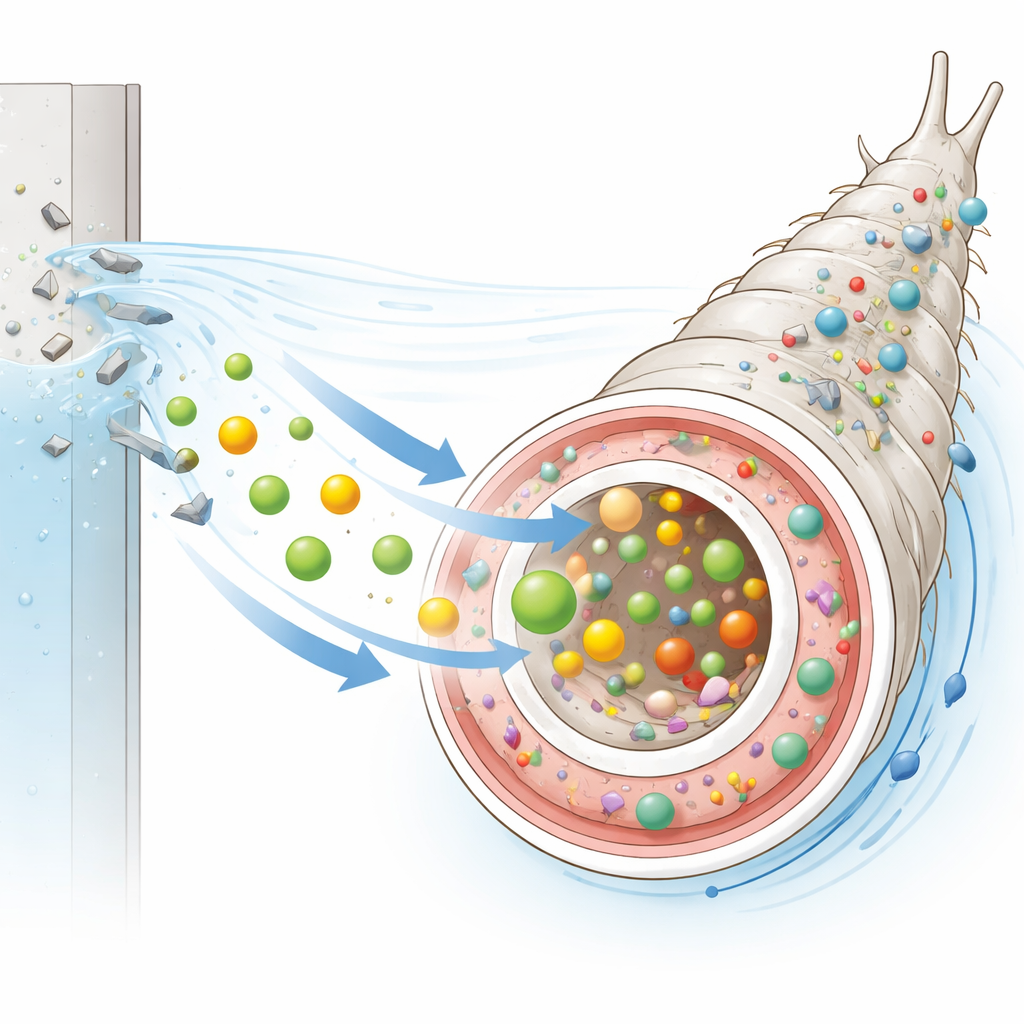
Ukryte odciski plastiku w jelicie
Ponad obrazowaniem świetlnym naukowcy zastosowali technikę ATR-FTIR, by odczytać chemiczne „odciski palców” jelit larw i materiałów hodowlanych. Jelita larw hodowanych w plastikowych naczyniach wykazały wyróżniający się sygnał w obszarze podczerwieni, który bardzo dobrze odpowiadał charakterystycznemu pasmu polistyrenu oraz jelit larw eksperymentalnie eksponowanych na kuleczki polistyrenowe. Ten pik nie występował w jelitach larw hodowanych w szkle ani w samym pokarmie, co mocno wskazuje na obecność materiału pochodzącego z plastiku u larw wychowanych w plastikowych pojemnikach. Chociaż mikroskopia elektronowa nie ujawniła oczywistych śladów obgryzienia czy zarysowań wewnętrznej powierzchni naczyń, wcześniejsze prace wykazały, że plastik może uwalniać mikroskopijne, a nawet nanometryczne fragmenty podczas normalnego użytkowania, które mogą być pobierane przez organizmy wodne.
Co to wszystko oznacza dla kontroli komarów i zanieczyszczeń
Mimo tych subtelnych różnic chemicznych i optycznych standardowe miary, takie jak przeżywalność larw, czas rozwoju i rozmiar dorosłych, nie zmieniały się znacząco między grupami hodowanymi w szkle i w plastiku, z wyjątkiem umiarkowanej różnicy w czasie rozwoju larwalnego. Dla powierzchownego obserwatora komary wyglądałyby niemal identycznie. Tymczasem ich jelita ujawniają bardziej złożoną historię: różnią się ilością blasku związanego z pokarmem, sposobem przetwarzania niektórych witamin i roślinnych pigmentów oraz tym, czy fragmenty plastiku dostały się do ich tkanek. Dla programów zwalczania wektorów, które opierają się na masowej hodowli komarów — szczególnie tych stosujących technikę owadów sterylnych — takie ukryte efekty mogą wpływać na długoterminową wydajność i kondycję. Szerzej, praca demonstruje, że naturalna fluorescencja i spektroskopia w podczerwieni mogą służyć jako czułe, niedestrukcyjne narzędzia do monitorowania diety, warunków hodowli i zanieczyszczenia plastikiem u małych organizmów wodnych. Metody te mogą pomóc w dopracowaniu bardziej ekologicznych strategii kontroli larw i pogłębić nasze rozumienie, jak mikroplastiki cicho przemieszczają się przez ekosystemy słodkowodne.
Cytowanie: Soldano, S., Weththimuni, M.L., Oldani, A. et al. Autofluorescence and Fourier transform infrared analyses trace dietary fluorophores and reveal plastic contamination in the gut of mosquito larvae. Sci Rep 16, 7841 (2026). https://doi.org/10.1038/s41598-026-38938-1
Słowa kluczowe: larwy komarów, autofluorescencja, mikroplastiki, pigmenty chlorofilowe, zwalczanie wektorów