Clear Sky Science · pl
A2-pancortiny współdziałają z Bcl-xL i WAVE1, aby promować miejsca kontaktu mitochondria–RE (MERCs) i nasilać wzrost wapnia mitochondrialnego prowadzący do śmierci komórkowej w udarze
Dlaczego maleńkie połączenia w mózgu mają znaczenie w udarze noworodków
Udar często postrzegany jest jako choroba dorosłych, ale gdy dotyka noworodków, może potajemnie uszkadzać rozwijający się mózg i powodować problemy na całe życie. Badanie to zagłębia się w to, co dzieje się głęboko wewnątrz komórek nerwowych podczas takiego kryzysu. Autorzy koncentrują się na mało znanej rodzinie białek zwanych pancortynami i pokazują, jak dwie formy występujące w trakcie rozwoju działają jak niebezpieczne „wzmacniacze”, zaciskając połączenia między kluczowymi strukturami komórkowymi i wywołując napływ wapnia, który może pchnąć młode neurony w kierunku śmierci.
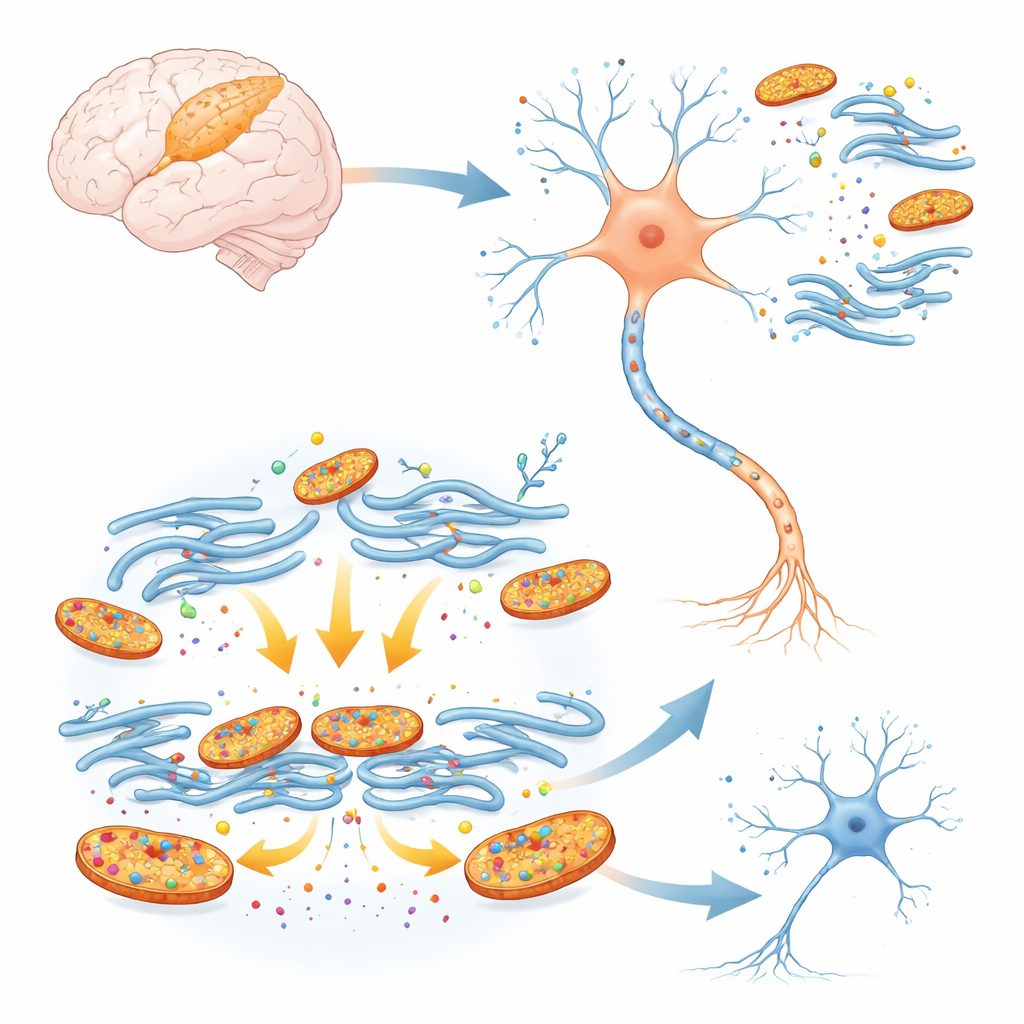
Ukryci sprawcy w mózgu noworodka
Pancortyny to białka pełniące rolę rusztowania, które pomagają kształtować rozwijający się mózg. Dwie postaci, określane jako A2-pancortyny, występują w obfitości w okresie wczesnego rozwoju, a następnie w dużym stopniu zanikają w miarę dojrzewania mózgu. Ponieważ mózgi noworodków są szczególnie wrażliwe na utratę tlenu, badacze sprawdzili, czy te białka występujące we wczesnym życiu mogą pogłębiać uszkodzenia, gdy dopływ krwi do kory jest krótko przerwany, jak ma to miejsce w udarze noworodkowym. W hodowanych komórkach korowych myszy użyli narzędzi genetycznych do obniżenia poziomów wszystkich pancortyn, a następnie poddali komórki niedoborowi tlenu i glukozy naśladującemu udar. Neurony z obniżonym poziomem pancortyn miały znacznie większe szanse na przetrwanie, co sugeruje, że te białka, zamiast chronić młode komórki, przyczyniają się do ich uszkodzenia pod wpływem stresu.
Od modeli udaru u myszy do uratowanej tkanki mózgowej
Aby sprawdzić, czy ta szkodliwa rola występuje także w żywym mózgu, zespół stworzył myszy pozbawione specyficznie rozwojowych form A2-pancortyn. Młode, dwutygodniowe myszy knockout i ich normalne mioty zostały poddane zamknięciu dużej tętnicy mózgowej, standardowemu modelowi udaru niedokrwiennego. Po jednym dniu obie grupy wykazywały uszkodzenia w głębokich obszarach mózgu, ale kora mózgowa myszy pozbawionych A2-pancortyn miała około połowy obrażeń w porównaniu z normalnymi zwierzętami. Co uderzające, ten efekt ochronny zniknął u pięciotygodniowych myszy, gdy dominują dorosłe warianty pancortyn. Wyniki zależne od wieku wskazują na A2-pancortyny jako kluczowe czynniki pro-śmierci w korze noworodków, łącząc program rozwojowy z podatnością na udar.
Niebezpieczne strefy kontaktowe wewnątrz neuronów
Wewnątrz komórek mitochondria produkujące energię leżą blisko siateczki endoplazmatycznej (RE), pofałdowanej sieci błon magazynującej wapń. Tam, gdzie dwie błony znajdują się w bliskim kontakcie, tzw. miejsca kontaktu mitochondria–RE działają jak mikroskopijne tunele, przez które może przechodzić wapń. Umiarkowany transfer wspiera produkcję energii, ale nadmiar może przeciążyć mitochondria i wywołać śmierć komórki. Badacze odkryli, że A2-pancortyny wraz z dwoma partnerami — Bcl-xL i WAVE1 — tworzą trójskładnikowy kompleks zlokalizowany w tych miejscach kontaktowych. Gdy wymusili nadprodukcję A2-pancortyn wraz z tymi partnerami, mitochondria i RE stykały się częściej i bardziej ściśle, co wykazał specjalistyczny sensor fluorescencyjny rozdzielony na części. Do kompleksu dołączyło białko kotwiczące GRP75, pomagając stabilizować strefy kontaktowe.
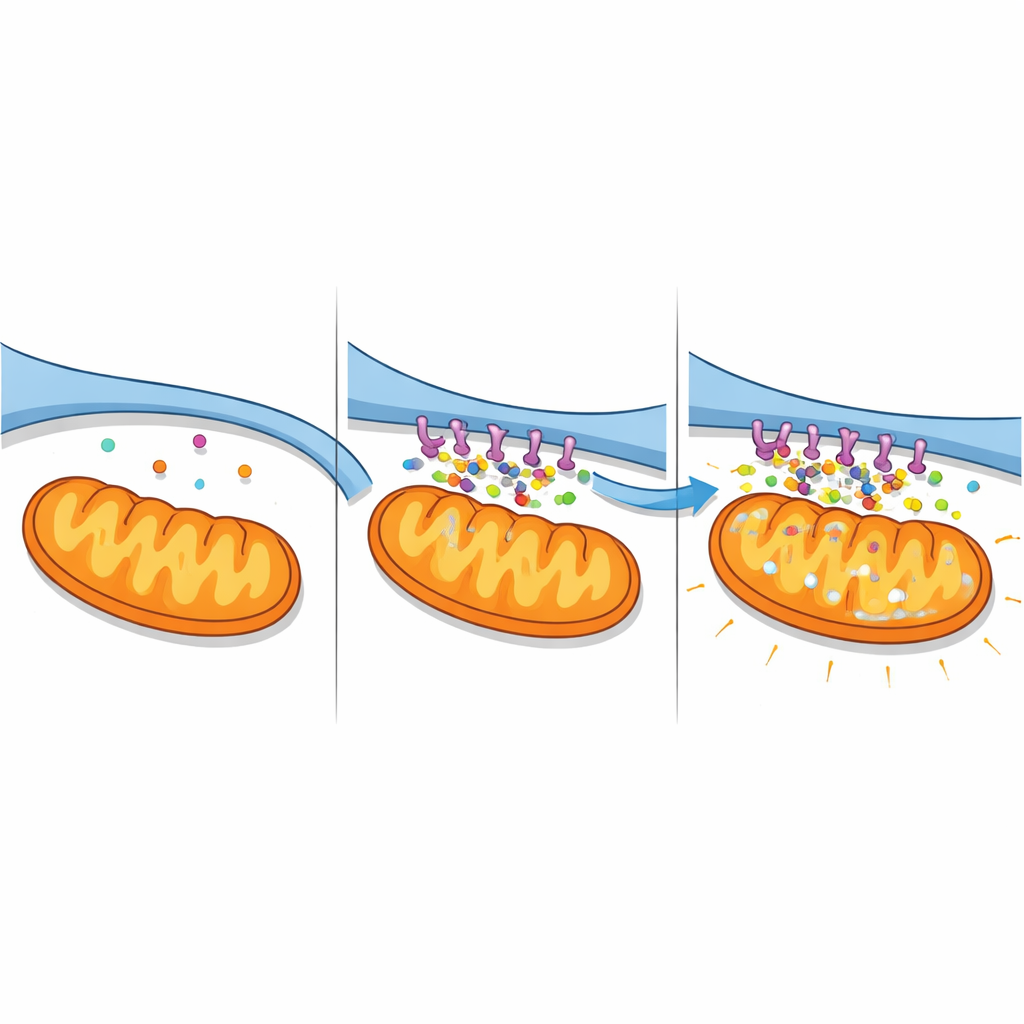
Fale wapnia i zawodzące elektrownie
Wzmocnione kontakty miały poważne konsekwencje dla równowagi wapniowej. Używając wskaźników fluorescencyjnych raportujących oddzielnie wapń w cytosolu, RE i mitochondriach, autorzy obserwowali zmiany poziomów w czasie. Komórki eksprymujące kompleks A2-pancortyn wykazywały stały wzrost wapnia w mitochondriach i w otaczającym płynie, wraz ze spadkiem zapasów w RE, co jest sygnaturą masywnego transferu z RE do mitochondriów. Zablokowanie kluczowego kanału uwalniającego wapń na powierzchni RE (IP3R) w dużej mierze zapobiegło tym zmianom, potwierdzając, że kompleks wzmacnia specyficzną drogę RE→mitochondria. W komórkach neuronopodobnych narażonych na niedobór tlenu i glukozy przypominający udar, wyciszenie pancortyn działało odwrotnie: przeciążenie wapniowe było złagodzone, a zapasy w RE lepiej zachowane. Razem te wyniki ukazują A2-pancortyny jako organizatory wapniowej „superautostrady”, która staje się śmiertelna w warunkach niedokrwiennych.
Co to oznacza dla ochrony mózgów noworodków
Dla osób niezajmujących się specjalistycznie tematem, główne przesłanie jest takie: praca identyfikuje nowy molekularny przełącznik, który pomaga zdecydować, czy młode neurony przeżyją czy umrą po udarze. Poprzez zaciskanie mikroskopijnych złączy między błonami magazynującymi wapń a komórkowymi elektrowniami, A2-pancortyny powodują, że mitochondria duszą się od nadmiaru wapnia i zawodzą. Usunięcie tych białek u młodych myszy łagodzi skutki eksperymentalnego udaru, co sugeruje, że leki lub terapie genowe mające na celu zaburzenie kompleksów A2-pancortyn — lub rozluźnienie wzmacnianych przez nie miejsc kontaktowych — mogłyby kiedyś zmniejszyć uszkodzenia mózgu u dotkniętych noworodków. Choć takie terapie pozostają perspektywą na przyszłość, badanie wyznacza jasną i testowalną ścieżkę od białek rozwojowych do przeładowania wapniem i utraty neuronów w udarze noworodków.
Cytowanie: Yang, Q., Wang, CC., Matsuyama, T. et al. A2-pancortins interact with Bcl-xL and WAVE1 to promote mitochondria-ER contact sites (MERCs) and exacerbate mitochondrial calcium elevation to mediate cell death in stroke. Sci Rep 16, 8467 (2026). https://doi.org/10.1038/s41598-026-38928-3
Słowa kluczowe: udar noworodkowy, miejsca kontaktu mitochondria–RE, przeciążenie wapniowe, białka pancortyn, śmierć komórek nerwowych