Clear Sky Science · pl
Zmieniona ekspresja osi CD26/ADA w zapaleniu o podłożu immunologicznym w mononukleozie zakaźnej
Dlaczego ten dziecięcy wirus ma znaczenie
Wielu rodziców zna mononukleozę zakaźną, często nazywaną „mono”, jako poważną, lecz zwykle przejściową chorobę objawiającą się gorączką, bólem gardła i powiększonymi węzłami chłonnymi. Jednak u niewielkiej liczby dzieci zakażenie może przybrać ciężką postać i uszkodzić narządy, np. wątrobę. To badanie przygląda się, jak układ odpornościowy dzieci reaguje na wirusa Epsteina–Barra, główną przyczynę mono, i koncentruje się na parze małych partnerów na powierzchni komórek — CD26 oraz enzymie nazywanym ADA — które mogą pomóc wyjaśnić, dlaczego niektóre odpowiedzi immunologiczne stają się niebezpiecznie intensywne.
Obrońcy organizmu w nadmiernym uruchomieniu
Kiedy wirus Epsteina–Barra wnika do organizmu, głównie infekuje określone komórki krwi białej i wywołuje silną reakcję odpornościową. W badaniu lekarze porównali krew 30 dzieci z ostrą mononukleozą z krwią 30 zdrowych dzieci. Stwierdzili, że chorzy mieli ogólnie więcej białych krwinek, zwłaszcza podgrupę zwaną limfocytami CD8, wyspecjalizowanych w zabijaniu komórek zakażonych. Jednocześnie inna ważna grupa pomocnicza, limfocyty CD4, była względnie zmniejszona, więc zwykła równowaga między komórkami „atakującymi” a „wspierającymi” uległa odwróceniu. W surowicy krwi poziomy białek zwalczających zakażenia, w tym kilku cząsteczek sygnałowych modulujących stan zapalny, były również podwyższone, co świadczy o pełnej aktywacji układu odpornościowego.
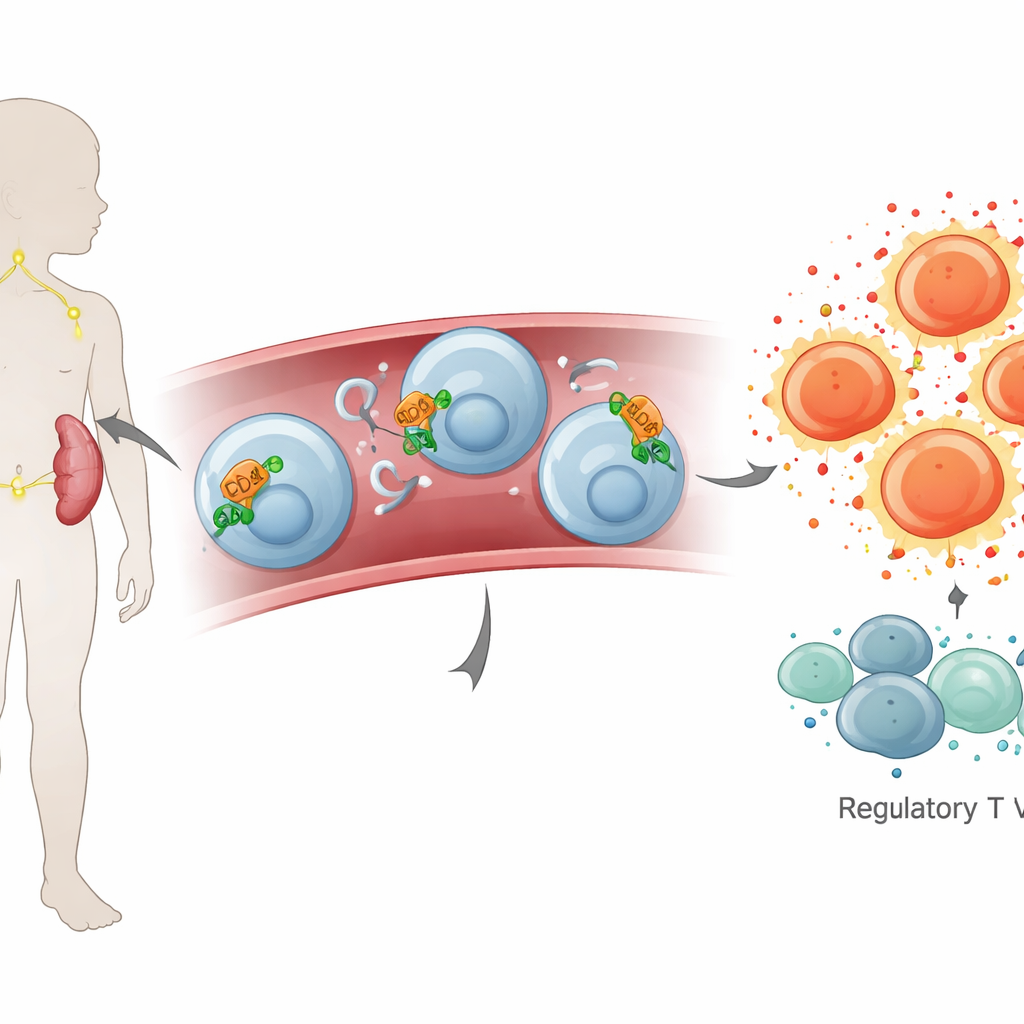
Bliższe spojrzenie na mały przełącznik sterujący
Naukowcy następnie skupili się na CD26 i ADA, dwóch cząsteczkach znajdujących się na styku między aktywacją komórkową a sygnalizacją chemiczną poza komórkami. Przy użyciu badań genetycznych na komórkach krwi odkryli, że dzieci z mononukleozą miały wyższe poziomy instrukcji dla CD26 i ADA (mRNA), co sugeruje, że komórki odpornościowe przygotowują się do produkcji większej ilości tych białek. Badania biochemiczne potwierdziły, że sama aktywność ADA była podwyższona. Co ciekawe, ilość krążącego białka CD26 w osoczu nie różniła się znacząco między chorymi a zdrowymi dziećmi, co sugeruje, że w mononukleozie ta cząsteczka może pozostawać głównie przyłączona do powierzchni komórek, zamiast krążyć w postaci rozpuszczalnej.
Przesunięta równowaga między atakiem a hamowaniem
Aby zrozumieć, jak ten przełącznik zachowuje się na różnych komórkach układu odpornościowego, zespół zastosował cytometrię przepływową, metodę liczenia i charakteryzowania komórek pojedynczo. Na limfocytach CD8, które dramatycznie się rozrastają podczas mononukleozy, CD26 był częstszy, niezależnie od tego, czy komórki nosiły inny marker zwany CD39, związany z silnym systemem hamującym opartym na sygnałach chemicznych. Ten wzorzec sugeruje, że w tych „komórkach zabójczych” CD26 może pomagać przezwyciężać lokalne sygnały chemiczne, które normalnie tłumiłyby ich aktywność, wspierając silny atak na komórki zakażone wirusem. Jednocześnie wśród limfocytów CD4, które zwykle koordynują odpowiedzi immunologiczne, obraz był bardziej zróżnicowany. Komórki noszące zarówno CD4, jak i CD39 — często kojarzone z rolami regulacyjnymi i uspokajającymi — występowały względnie częściej, co może pomóc wyjaśnić podwyższone poziomy sygnałów kojących, takich jak cytokinina IL-10.
Gdy regulacja słabnie
Jednak w populacji CD4 pozbawionej CD39, zwykle złożonej z aktywnych komórek pomocniczych, odsetek komórek wykazujących CD26 był faktycznie niższy u dzieci z mononukleozą niż u zdrowych rówieśników. Utrata CD26 na komórkach pomocniczych może osłabić ich zdolność do proliferacji i koordynowania zrównoważonych odpowiedzi, nawet gdy komórki CD8 są pchane w kierunku silniejszej aktywności. Badanie wykazało także, że ilość CD26 w osoczu korelowała z poziomami ADA i interferonu gamma — silnego sygnału zapalnego — i była odwrotnie związana z odsetkiem limfocytów CD4 oraz z relacją CD4 do CD8. Razem te wzorce wskazują, że oś CD26/ADA jest ściśle powiązana z siłą odpowiedzi immunologicznej podczas zakażenia.
Co to oznacza dla chorych dzieci
Dla rodzin i klinicystów wyniki te dają jaśniejszy obraz, dlaczego powszechny wirus czasami prowadzi do niepokojącej choroby. W ostrym przebiegu mononukleozy układy odpornościowe dzieci wydają się mocno polegać na limfocytach CD8 uzbrojonych w zwiększoną aktywność osi CD26–ADA, napędzając silną odpowiedź przeciwwirusową, która ryzykuje przesadnym działaniem i uszkodzeniem tkanek. Jednocześnie niektóre komórki pomocnicze i regulacyjne tracą lub przekształcają swoje wzorce ekspresji CD26, co może osłabiać hamulec, który normalnie utrzymuje zapalenie w ryzach. Choć potrzebne są dalsze badania — szczególnie w bardzo ciężkich przypadkach — badanie sugeruje, że mierzenie, a w przyszłości modulowanie osi CD26/ADA mogłoby pomóc lekarzom oceniać ciężkość choroby lub projektować terapie łagodzące szkodliwe reakcje immunologiczne, nie wyłączając przy tym obrony organizmu.
Cytowanie: Shi, T., Shi, W., Tian, J. et al. Altered expression of the CD26/ADA axis in immune-mediated inflammation of infectious mononucleosis. Sci Rep 16, 9316 (2026). https://doi.org/10.1038/s41598-026-38891-z
Słowa kluczowe: mononukleoza zakaźna, wirus Epsteina-Barr, limfocyty T, regulacja odporności, ścieżka adenozynowa