Clear Sky Science · pl
Ocena ewolucyjnego pokrewieństwa białka wiążącego TATA (TBP) z różnymi wzorcami fałdowania domen białkowych przy użyciu maszyny wektorów nośnych (SVM)
Jak białko „włącznik” DNA łączy się z wieloma innymi
Białko wiążące TATA‑box, czyli TBP, to jedna z podstawowych maszyn naszych komórek: pomaga włącząć geny, chwytając DNA przy wielu promotorach. To badanie stawia pozornie proste, ale dalekosiężne pytanie: czy istnieją inne białka, o bardzo różnych funkcjach, które skrycie dzielą z TBP jego podstawowy kształt? Łącząc porównania struktur 3D, analizę sekwencji i współczesne narzędzia uczenia maszynowego, autorzy wyśledzili ukryte więzy rodzinne między TBP a białkami zaangażowanymi w metabolizm, chemię neuroprzekaźników, a nawet szlaki związane z rakiem.
Jedno kluczowe białko w centrum kontroli genów
TBP znajduje się u bramy ekspresji genów u organizmów od drożdży po ludzi. Rozpoznaje krótką sekwencję DNA zwaną pudełkiem TATA i zaginając DNA pomaga w składaniu dużego zespołu transkrypcyjnego, który przepisuje geny na RNA. Ponieważ ten krok jest tak centralny, fałd — trójwymiarowe ułożenie — rdzenia TBP jest silnie konserwowany w toku ewolucji. Autorzy koncentrują się na dobrze poznanej strukturze TBP oznaczonej jako 1tba i używają jej jako sondy do wyszukiwania innych białek, które mogą dzielić jego architektoniczny wzorzec, nawet jeśli ich sekwencje aminokwasowe i codzienne funkcje z początku wydają się bardzo różne.
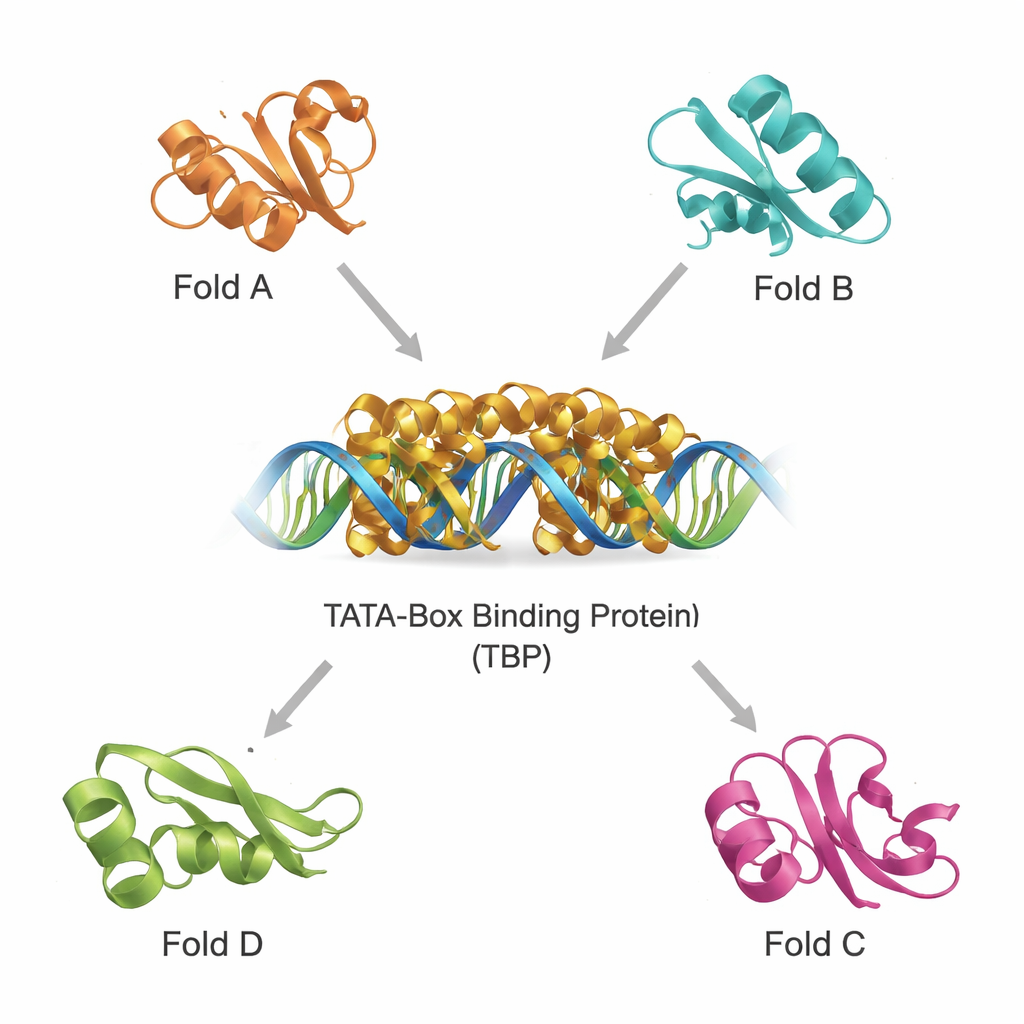
Znajdowanie strukturalnych kuzynów w zatłoczonym świecie białek
Nowoczesne bazy danych zawierają setki tysięcy struktur białkowych, co umożliwia wyszukiwanie dalekich krewnych według kształtu 3D, a nie tylko sekwencji. Korzystając z dwóch wydajnych narzędzi, DALI i TOP‑search, zespół najpierw wyodrębnił białka, których fałdy przypominały TBP. Następnie sklasyfikowali te kandydatury przy użyciu katalogu domen ewolucyjnych i zawęzili zestaw do kilku strukturalnie podobnych, ale funkcjonalnie zróżnicowanych przykładów. Należą do nich enzym syntetyzujący glutaminę ważny w metabolizmie, domena występująca w kilku enzymach obsługujących tRNA, enzym o charakterystycznym „hot‑dog” fałdzie zaangażowany w chemię kwasów tłuszczowych oraz białka uczestniczące w syntezie tetrahydrobiopteryny, molekuły kluczowej dla funkcji mózgu. Nałożenie ich struktur na TBP pokazało, że mimo różnych zadań zachowują rozpoznawalne motywy rdzeniowe.
Nauczanie maszyn rozpoznawania ukrytych rodzin białek
Aby wyjść poza inspekcję przypadek po przypadku, autorzy zbudowali modele uczenia maszynowego, które automatycznie identyfikowały fałdy podobne do TBP. Zgromadzili duże zbiory sekwencji białkowych znanych jako należące do TBP lub do każdej z powiązanych rodzin fałdów, wraz z szerokim zestawem „tła” niezwiązanych białek. Każde białko zamieniono na proste podsumowania numeryczne: jak często występuje każdy aminokwas oraz jak często pojawiają się pary aminokwasów w sekwencji. Te profile zasiliły maszyny wektorów nośnych (SVM) i modele lasu losowego (random‑forest), które nauczyły się rozdzielać jeden typ fałdu od wszystkich innych. Przy użyciu rygorystycznej walidacji krzyżowej modele osiągały bardzo wysoką skuteczność — często powyżej 95 procent — nawet gdy trenowano je tylko na fragmentach sekwencji odpowiadających regionom konserwowanym.
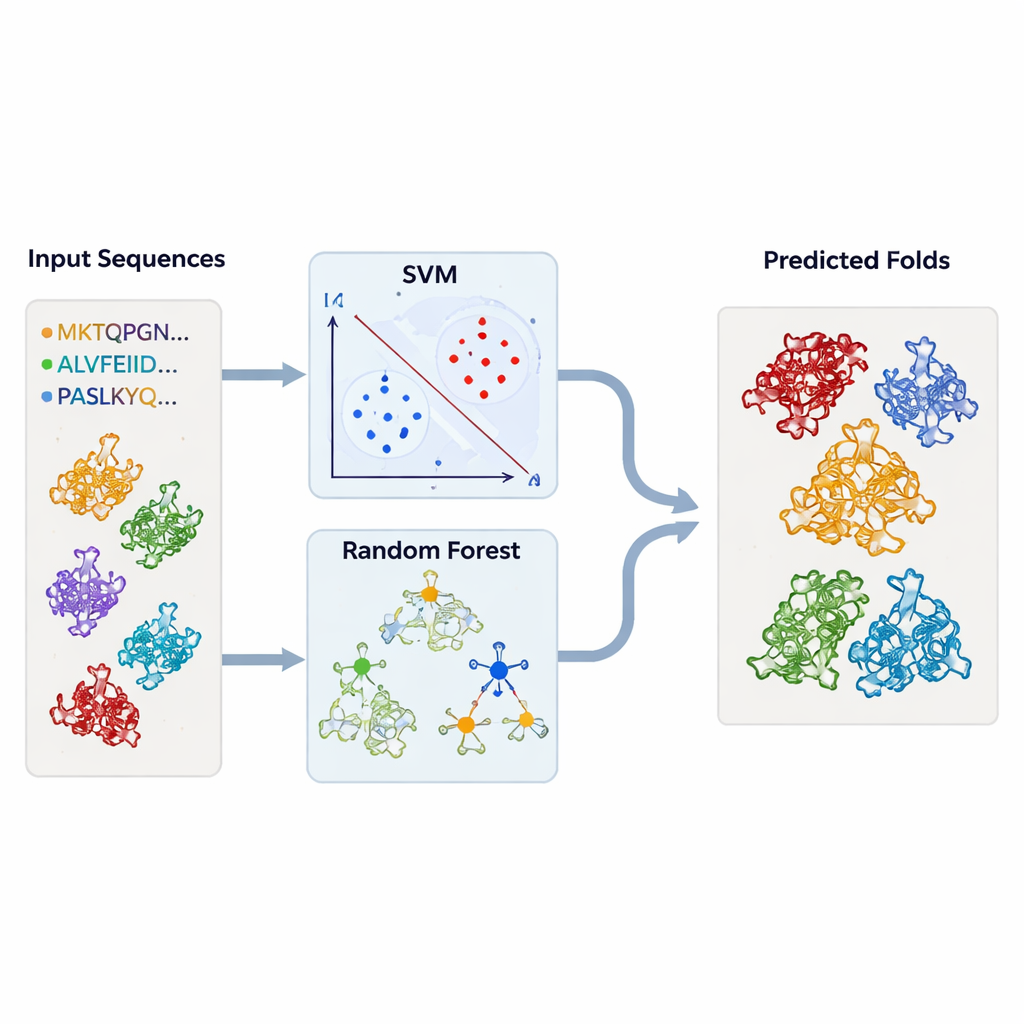
Testowanie modeli na tysiącach nieznanych struktur
Uzbrojeni w wytrenowane klasyfikatory, autorzy wrócili do baz struktur. Przeanalizowali tysiące łańcuchów białkowych — pobranych z DALI i TOP‑search — przez swoje modele, aby sprawdzić, które z nich noszą statystyczne cechy fałdów podobnych do TBP lub pokrewnych. Podejścia SVM i lasu losowego w dużej mierze się zgadzały i wyłoniły wiele kandydatów, które narzędzia strukturalne również wskazały jako podobne. W niektórych przypadkach enzymy o pozornie niezwiązanych aktywnościach silnie grupowały się z TBP lub ze sobą nawzajem, co wzmacnia ideę, że ewolucja może przeznaczać ten sam podstawowy szkielet do wielu różnych ról biochemicznych.
Dlaczego te ukryte więzi są ważne
Badanie konkluduje, że TBP dzieli głębokie strukturalne pokrewieństwo z kilkoma rodzinami enzymów, w tym białkami podobnymi do syntetazy glutaminy i domenami edycyjnymi enzymów przetwarzających tRNA. Nawet gdy sekwencje uległy dryfowi, a funkcje rozeszły się, te białka zachowują wspólne motywy architektoniczne, co sugeruje pochodzenie od wspólnego przodka. Dla czytelnika niebędącego specjalistą kluczowy przekaz jest taki, że natura ma skłonność do powielania udanych rozwiązań: jeden fałd może być wielokrotnie adaptowany do rozwiązywania bardzo różnych problemów, od uruchamiania genów po dostrajanie metabolizmu i chemii mózgu. Łącząc porównania struktur 3D z uczeniem maszynowym, autorzy dostarczają praktycznego zestawu narzędzi do odkrywania takich związków, pomagając biologom przewidywać funkcje nieopisanych białek i wskazując deweloperom leków nowe, kierowane ewolucyjnie cele w ścieżkach istotnych dla chorób.
Cytowanie: Selvaraj, M.K., Kaur, J. Evaluating the evolutionary relationship of TATA binding protein (TBP) with various folding patterns of protein domains using support vector machine (SVM). Sci Rep 16, 7696 (2026). https://doi.org/10.1038/s41598-026-38883-z
Słowa kluczowe: białko wiążące TATA-box, ewolucja białek, uczenie maszynowe, struktura białka, maszyna wektorów nośnych