Clear Sky Science · pl
Szlak Wnt/β-katenina kształtuje zachowanie makrofagów podczas uszkodzenia i naprawy w śliniance podżuchwowej myszy
Dlaczego suchość w ustach ma znaczenie
Kserostomia, czyli przewlekłe uczucie suchości w ustach, to coś więcej niż drobna niedogodność. Może sprawiać, że jedzenie jest bolesne, mowa utrudniona, a ryzyko zakażeń i próchnicy zębów istotnie wzrasta. Wielu pacjentów doświadcza ciężkiej suchości po radioterapii głowy i szyi lub w przebiegu chorób autoimmunologicznych, takich jak zespół Sjögrena. Gdy ślinianki ulegają uszkodzeniu, często regenerują się słabo, a obecne terapie głównie łagodzą objawy, zamiast przywracać funkcję. W tej pracy badano, jak określona grupa komórek układu odpornościowego — makrofagi — oraz kluczowy szlak komunikacji międzykomórkowej zwany sygnalizacją Wnt/β-katenina współdziałają, wpływając na to, czy uszkodzona ślinianka bliznuje, czy się regeneruje.
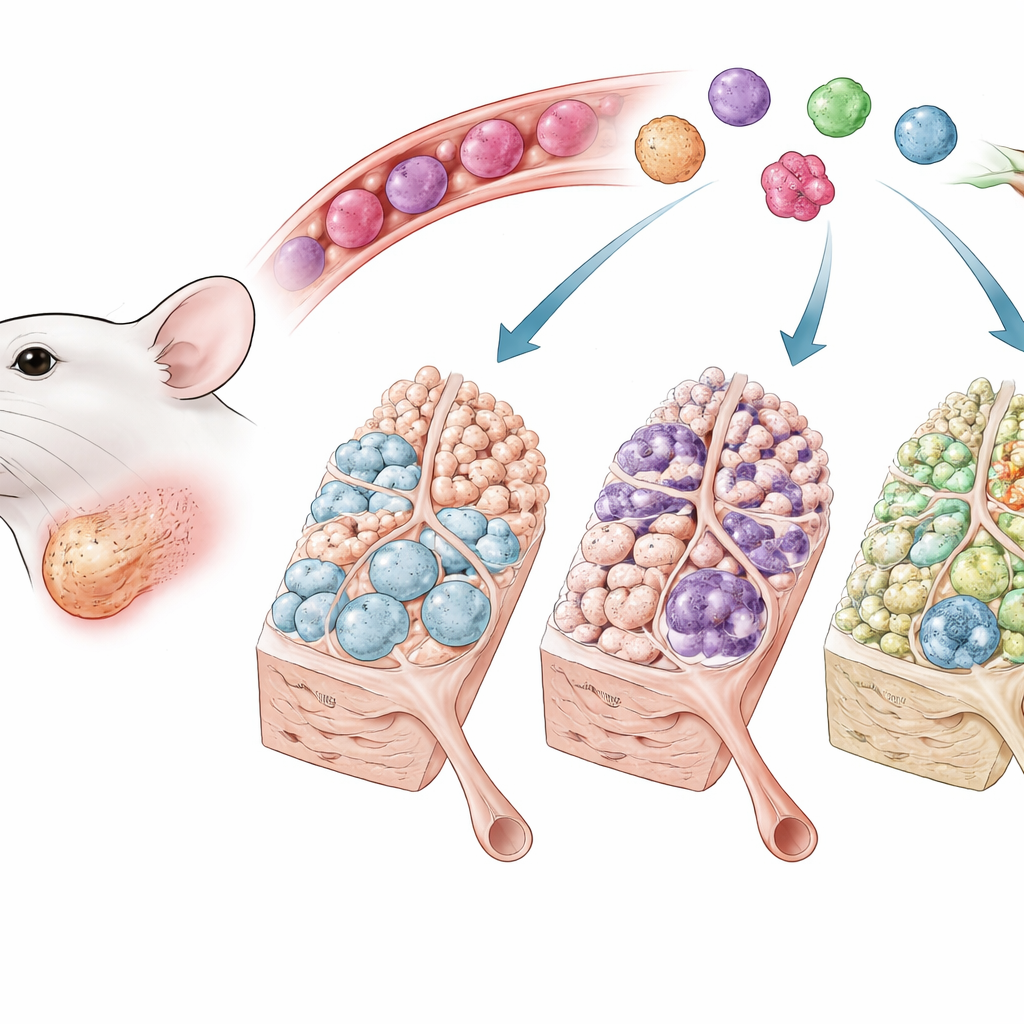
Komórki strażnicze przy bramie
Ślinianki zawierają liczne komórki pęcherzykowe wydzielające ślinę oraz przewody, które odprowadzają ją do jamy ustnej. Gdy główny przewód jest zablokowany, delikatne struktury zapadają się, tkanka ulega zapaleniu, a w miejscu uszkodzenia gromadzi się włóknista tkanka bliznowata. Makrofagi to komórki pierwszej linii obrony, które napływają do uszkodzonej tkanki i mogą albo podsycać stan zapalny i bliznowacenie, albo wspierać łagodną, uporządkowaną naprawę. Autorzy użyli dobrze opisanej mysiej szczepu, w którym tymczasowo zaciskano główny przewód ślinianki podżuchwowej, aby naśladować uraz obturacyjny, a następnie przywracano drożność, by obserwować regenerację. Połączyli ten model z myszami reporterowymi, które aktywują sygnalizację świetlną przy aktywnym szlaku Wnt/β-katenina, co pozwoliło zobaczyć, które komórki odbierają ten sygnał po urazie.
Sygnały w tkankach podporowych
Po zablokowaniu przewodu badacze zauważyli znaczące uszkodzenia tkanki: utratę jednostek pęcherzykowych, obrzęknięte przewody i pogrubioną torebkę bogatą w kolagen. Równocześnie zaobserwowali napływ komórek reagujących na Wnt — nie wewnątrz jednostek produkujących ślinę, lecz głównie w tkance podporowej (stroma): w torebce, wewnętrznych przegrodach i przestrzeniach między przewodami a pęcherzykami. Większość tych komórek reagujących na Wnt nosiła markery komórek odpornościowych i makrofagów, co pokazuje, że makrofagi stanowią znaczącą populację aktywną w szlaku Wnt podczas urazu. Pomiary ekspresji genów w czasie wykazały, że zarówno gen odczytu aktywności Wnt (Axin2), jak i marker makrofagów (F4/80) osiągały szczyt około trzeciego i szóstego dnia po urazie, co wskazuje, że napływ makrofagów i aktywność Wnt są ściśle powiązane we wczesnych i środkowych etapach naprawy.
Makrofagi jako nadawcy i odbiorcy
Aby ustalić, skąd pochodzą sygnały Wnt, zespół zmierzył ekspresję wszystkich znanych genów Wnt w uszkodzonych gruczołach. Kilka z nich było podwyższonych, a Wnt2 i Wnt2b wyróżniały się szczególnie wzrostem zarówno trzeciego, jak i szóstego dnia. Mikroskopia wykazała obecność tych białek Wnt wewnątrz makrofagów, co sugeruje, że te same komórki, które wydzielają sygnały Wnt, także na nie odpowiadają. Dalsze eksperymenty wskazały, że wiele z makrofagów aktywnych w szlaku Wnt to komórki niedawno zrekrutowane z krwi, a nie stałe rezydentne populacje gruczołu. W istocie uraz przyciąga nowe makrofagi, które następnie uruchamiają sprzężenie zwrotne napędzane Wnt, co może wpływać na ich zachowanie i na sposób remodelowania tkanki przez komórki podporowe.
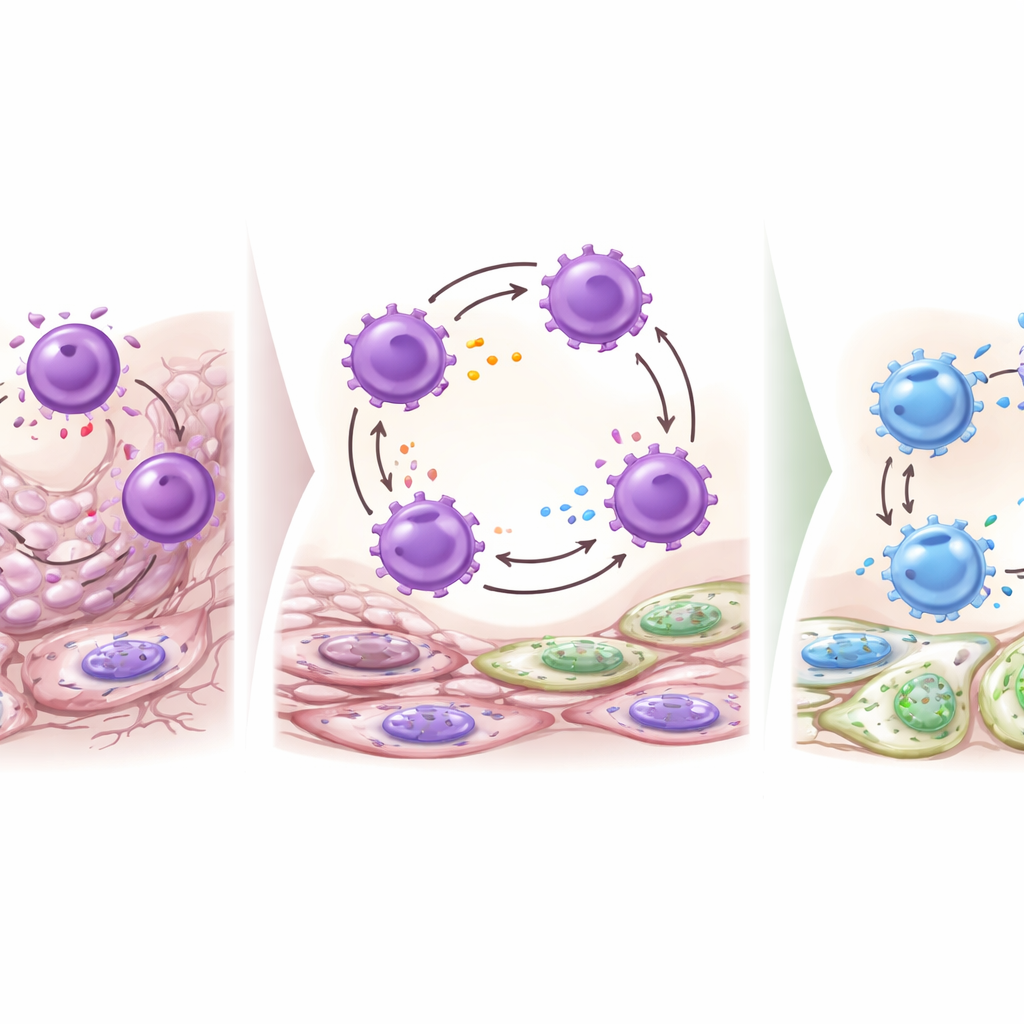
Bliznowacenie kontra łagodna naprawa
Autorzy zapytali również, czy komórki reagujące na Wnt bezpośrednio odbudowują komórki pęcherzykowe produkujące ślinę. Pomimo silnej aktywności Wnt w komórkach stromalnych i przewodowych po urazie, eksperymenty śledzenia linii komórkowych wykazały, że komórki oznaczone przez Axin2 nie przekształcały się w nowe komórki pęcherzykowe po przywróceniu drożności przewodu i wygojeniu gruczołu. Zamiast tego głównie uczestniczyły w utrzymaniu przewodów. Aby sprawdzić, jak sygnalizacja Wnt wpływa na jakość naprawy, zespół częściowo wyłączył wydzielanie ligandów Wnt przez usunięcie genu Wntless (Wls) ogólnie albo specyficznie w komórkach reagujących na Wnt. U tych myszy uszkodzone gruczoły miały cieńsze torebki włókniste, mniej rozdętych przewodów oraz zauważalny wzrost liczby makrofagów CD206-dodatnich — populacji zwykle związanej z profilem bardziej naprawczym, sprzyjającym gojeniu. To sugeruje, że osłabienie sygnału Wnt skłania makrofagi ku łagodniejszej odpowiedzi o mniejszym potencjale bliznowacenia.
Co to oznacza dla osób z suchością w ustach
Razem wyniki stawiają sygnalizację Wnt/β-katenina jako kluczowy przełącznik decydujący o tym, czy makrofagi w uszkodzonej śliniance sprzyjają szkodliwemu zwłóknieniu, czy bardziej konstruktywnej naprawie. Makrofagi w tym układzie nie wydają się bezpośrednio odbudowywać komórek produkujących ślinę, ale ich sygnalizacja silnie wpływa na równowagę między bliznowaceniem a regeneracją w podporowej strukturze gruczołu. Dla pacjentów z suchością spowodowaną radioterapią lub chorobami autoimmunologicznymi precyzyjne ukierunkowanie sygnalizacji Wnt w makrofagach — zamiast ich całkowitej eliminacji — mogłoby pewnego dnia pomóc zmniejszyć bliznowacenie, przywrócić zdrowszą architekturę tkanki i poprawić funkcję gruczołu. Praca ta dostarcza podstaw mechanistycznych dla terapii mających na celu przekształcenie środowiska gojenia w śliniance zamiast jedynie zastąpienia utraconych elementów.
Cytowanie: Ahmed, A., Sachdeva, S., Whawell, S. et al. Wnt/β -catenin signalling shapes macrophage behaviour during injury and repair in the mouse submandibular gland. Sci Rep 16, 8972 (2026). https://doi.org/10.1038/s41598-026-38873-1
Słowa kluczowe: naprawa ślinianki, makrofagi, sygnalizacja Wnt, zwłóknienie, kserostomia