Clear Sky Science · pl
Analizy dynamiki konformacyjnej i swobodnej energii wiązania ujawniają stabilny flawonoidowy inhibitor polimerazy NS5 wirusa dengu
Dlaczego wirus przenoszony przez komary potrzebuje pomocy z roślin
Gorączka denga rozprzestrzeniła się na całym świecie w ostatnich latach, chorując miliony i zabijając tysiące osób. Nadal jednak brakuje powszechnie skutecznej, przystępnej cenowo tabletki przeciwwirusowej, która mogłaby leczyć zakażonych. Niniejsze badanie stawia pozornie proste pytanie o dużych implikacjach: czy naturalnie występujące związki roślinne można przekształcić w precyzyjne molekularne „klucze”, które zablokują jedną z najważniejszych maszyn wirusa dengu?
Silnik wirusa, który naukowcy chcą unieruchomić
Wirus dengu przetrwa, kopiując materiał genetyczny w naszych komórkach. Do tego potrzebny jest kluczowy białkowy element zwany NS5, działający jak maleńki silnik kopiujący RNA wirusa. Gdy NS5 przestaje działać, wirus nie jest w stanie wytwarzać nowych genomów i zakażenie ustaje. Dlatego deweloperzy leków widzą w NS5 — a w szczególności w jego regionie kopiującym RNA, znanym jako RNA-zależna polimeraza RNA — atrakcyjny cel dla nowych terapii. Kilka syntetycznych związków i ekstraktów roślinnych już wykazało, że NS5 można zablokować, lecz wiele z tych wczesnych kandydatów wiąże się słabo, jest nietrwałych lub budzi obawy dotyczące bezpieczeństwa i farmakokinetyki.
Poszukiwanie obiecujących chemicznych igieł w stogu siana wśród roślin
Naukowcy skupili się na flawonoidach — dużej rodzinie związków roślinnych występujących w produktach takich jak jagody, herbata i zioła, znanych od dawna z właściwości przeciwwirusowych i przeciwzapalnych. Z wyselekcjonowanej bazy wtórnych metabolitów roślinnych wybrano 326 flawonoidów i przygotowano trójwymiarowe modele zarówno enzymu NS5 wirusa, jak i każdego kandydata. Za pomocą etapowego dokowania komputerowego zadano pytanie: które kształty najlepiej pasują do specyficznego „tylnego wejścia” na NS5, nazwanego kieszenią N — miejsca alosterycznego, które po zajęciu może wyłączyć enzym i które zwykle mutuje rzadziej niż główne miejsce aktywne?
Na każdym etapie tego wirtualnego przesiewu odrzucano związki, które słabo pasowały lub wyglądały na mało obiecujące pod kątem zachowania się jak prawdziwe leki w organizmie. Pozostałe molekuły oceniano nie tylko pod względem geometrycznego dopasowania, lecz także szacowanej siły wiązania przy użyciu metody przybliżającej energie związane z przyłączaniem się związku do NS5 w warunkach wodnych, zbliżonych do komórkowych. Ten proces zawęził pole do kilku najlepszych flawonoidów, z jednym kandydatem oznaczonym jako PSCdb01560 wyróżniającym się szczególnie korzystną przewidywaną energią wiązania.
Obserwowanie ruchu molekuł w wirtualnym mikroskopie
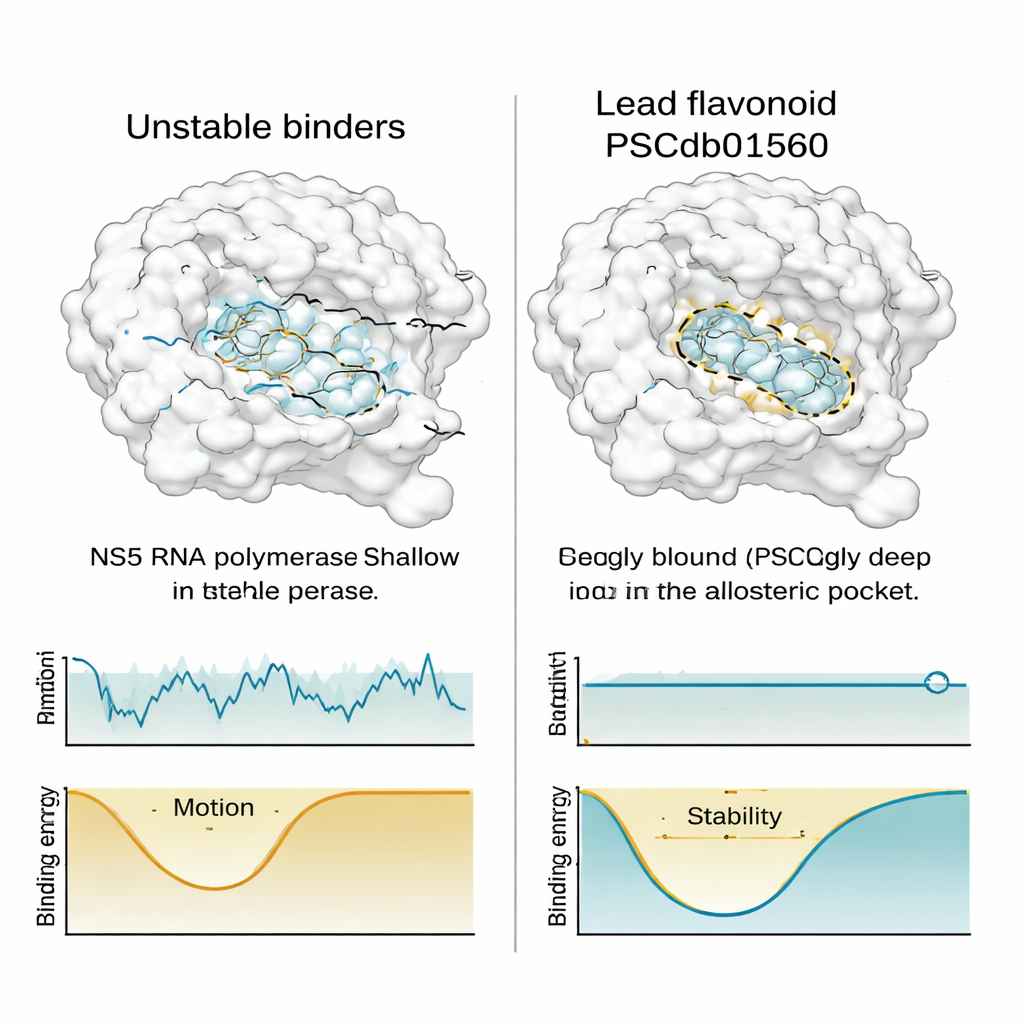
Dobre dopasowanie w statycznym zrzucie nie wystarcza; użyteczny lek musi także pozostać na miejscu, gdy wszystko się porusza. Aby to sprawdzić, zespół przeprowadził długie, szczegółowe symulacje dynamiki molekularnej — komputerowe filmy trwające równowartość pół mikrosekundy — dla NS5 w parze z najlepszymi flawonoidami oraz znanym inhibitorem odniesienia. Śledzili, jak bardzo białko i każdy związek się chwiejny, jak ciasno upakowany pozostaje kompleks, jak bardzo jest eksponowany na otaczającą wodę oraz jak często powstają i zrywają się kluczowe kontakty chemiczne. PSCdb01560 wykazał niezwykle stabilne zachowanie: pozostał głęboko osadzony w kieszeni N, poruszał się bardzo niewiele w porównaniu z rywalami i wydawał się stabilizować ogólny kształt NS5 zamiast go zaburzać.
W przeciwieństwie do tego, dwa inne flawonoidy, które początkowo wydawały się obiecujące, zaczęły dryfować w obrębie kieszeni lub stawać się bardziej odsłonięte na powierzchni rozpuszczalnika w miarę upływu czasu — oznaki słabszego, mniej niezawodnego wiązania. Gdy badacze odwzorowali „krajobraz swobodnej energii” każdego kompleksu — sposób wizualizacji kształtów faworyzowanych termodynamicznie — odkryli, że PSCdb01560 zajmował głęboką, dobrze zdefiniowaną dolinę energetyczną, podczas gdy mniej stabilne związki przeskakiwały między kilkoma płytszymi zagłębieniami. Porównanie najniższej energetycznie migawki do początkowo zadokowanych pozycji wykazało, że pozycja PSCdb01560 zmieniła się nieznacznie, co podkreśla jego konformacyjną lojalność.
Liczby sugerujące siłę na poziomie leku
Na koniec zespół zastosował ramy obliczeń energetycznych, aby oszacować, jak silnie każdy flawonoid będzie wiązał się po uwzględnieniu całego zasymulowanego ruchu. PSCdb01560 osiągnął energię swobodnego wiązania korzystniejszą niż ustalony związek odniesienia, napędzaną kombinacją dopasowania kształtowego, atrakcyjnych interakcji elektrostatycznych i hydrofobowych kontaktów wewnątrz kieszeni. Ten schemat — silne obliczeniowe powinowactwo, stabilne pozycjonowanie w czasie, ograniczone wewnętrzne wyginanie i angażowanie kluczowych reszt NS5 wspólnych dla szczepów dengu — czyni PSCdb01560 szczególnie przekonującym punktem wyjścia w projektowaniu leków.
Co to może oznaczać dla przyszłych terapii przeciw dengu
Te wyniki nie dostarczają jeszcze tabletki na dengę, ale znacznie zawężają poszukiwania. Praca identyfikuje jeden flawonoidowy szkielet pochodzenia roślinnego, który w kalkulacjach przewyższa kilku konkurentów, a nawet znany inhibitor odniesienia pod względem stabilności i przewidywanej siły wiązania. Kolejne kroki są eksperymentalne: sprawdzenie, czy PSCdb01560 rzeczywiście blokuje NS5 w probówkach, zatrzymuje replikację dengu w zakażonych komórkach oraz jest bezpieczny w modelach zwierzęcych. Jeśli te przeszkody zostaną pokonane, chemicy mogliby udoskonalić ten flawonoid do postaci klinicznie użytecznego środka przeciwwirusowego. Na razie badanie niesie obiecujące przesłanie: biblioteka naturalnych związków wciąż skrywa narzędzia, które mogą unieszkodliwić jedno z najszybciej rosnących zagrożeń przenoszonych przez komary na świecie.
Cytowanie: Alsaady, I.M., Gattan, H.S., Aljahdali, S.M. et al. Conformational dynamics and binding free energy analyses unveil a stable flavonoid inhibitor of dengue virus NS5 polymerase. Sci Rep 16, 7761 (2026). https://doi.org/10.1038/s41598-026-38864-2
Słowa kluczowe: wirus dengu, polimeraza NS5, inhibitor flawonoidowy, odkrywanie leków przeciwwirusowych, docking molekularny