Clear Sky Science · pl
Kadm wywołuje ferroptozę w spermatocytach myszy przez aktywację szlaku ROS–cyklu TCA
Dlaczego powszechny metal ma znaczenie dla zdrowia mężczyzn
Kadm to miękki metal stosowany w akumulatorach, pigmentach i innych produktach przemysłowych. Może gromadzić się w glebie, wodzie i żywności, stopniowo dostając się do organizmów. Wiele badań powiązało narażenie na kadm ze spadkiem liczby plemników i pogorszeniem ich jakości u mężczyzn, lecz dokładny mechanizm uszkadzania komórek produkujących plemniki pozostawał niejasny. Niniejsze badanie przybliża ten problem, ujawniając, w jaki sposób kadm popycha mysie komórki spermatogenezy na specyficzną ścieżkę śmierci komórkowej związaną z żelazem i zaburzeniem układu energetycznego w mitochondriach, elektrowniach komórkowych.
Od zanieczyszczenia do podatnych komórek plemnikotwórczych
Kadm jest dobrze znanym środowiskowym czynnikiem szkodliwym dla układu rozrodczego mężczyzn. Mężczyźni narażeni zawodowo lub mieszkający w zanieczyszczonych regionach często wykazują mniejszą liczbę plemników, obniżoną ruchliwość i odsetek prawidłowych morfologii, a nawet uszkodzenia DNA w plemnikach. Badania na zwierzętach potwierdzają te obserwacje, pokazując pomniejszone jądra, uszkodzone bariery ochronne, niski poziom testosteronu i masową utratę komórek rozrodczych. Autorzy wcześniej zauważyli, że kadm może wywołać nietypową, żelazozależną formę śmierci komórkowej zwaną ferroptozą w tkance jądra. W obecnej pracy skupili się na spermatocytach mysich — komórkach w trakcie przekształcania się w plemniki — aby ustalić, jak dokładnie kadm je uszkadza i czy droga śmierci związana z żelazem jest zaangażowana.
Przeciążenie żelazem i szczególny rodzaj śmierci komórkowej
Aby to zbadać, zespół hodował linię spermatocytów mysich w pożywkach i wystawiał komórki na działanie kadmu, z dodatkiem lub bez leków znanych z blokowania ferroptozy. Kadm zmniejszył przeżywalność komórek o około połowę i spowolnił ich podziały. Wnętrze komórek wykazało wyraźny wzrost poziomów wolnego żelaza i markera uszkodzenia lipidów — malondialdehydu, podczas gdy kluczowy enzym ochronny GPX4 uległ obniżeniu. Inne białka biorące udział w magazynowaniu i eksporcie żelaza wzrosły, sygnalizując poważne zaburzenia w gospodarce żelazem. Gdy badacze dodali inhibitory ferroptozy — związek chelatujący żelazo i cząsteczkę chroniącą lipidy — wiele z tych szkodliwych zmian złagodniało, a przeżywalność komórek poprawiła się. Zmiany te odpowiadają sygnaturze ferroptozy, wskazując, że kadm nie zabija komórek w sposób ogólny, lecz popycha je w konkretny, żelazo‑ i lipidowy program śmierci.
Mitochondria pod ostrzałem
Opowieść pogłębiła się, gdy naukowcy zwrócili uwagę na mitochondria, centra energetyczne, które także wytwarzają reaktywne formy tlenu (ROS) jako produkty uboczne. W mikroskopie zdrowe komórki spermatogenezy miały długie, nitkowate mitochondria, podczas gdy komórki wystawione na kadm wykazywały krótkie, pękające struktury — oznakę uszkodzeń strukturalnych. Pomiary potwierdziły gwałtowny wzrost mitochondrialnych ROS, a także spadek potencjału błonowego mitochondriów — kluczowego wskaźnika funkcji. Komórki odpowiedziały zwiększeniem wewnętrznych systemów obronnych, w tym białek regulowanych przez czujnik stresu Nrf2, lecz te mechanizmy okazały się niewystarczające. Co ważne, leki blokujące ferroptozę zmniejszyły mitochondrialne ROS i częściowo przywróciły zdrowie mitochondriów, łącząc uszkodzone „elektrownie” bezpośrednio ze ścieżką śmierci zależną od żelaza.
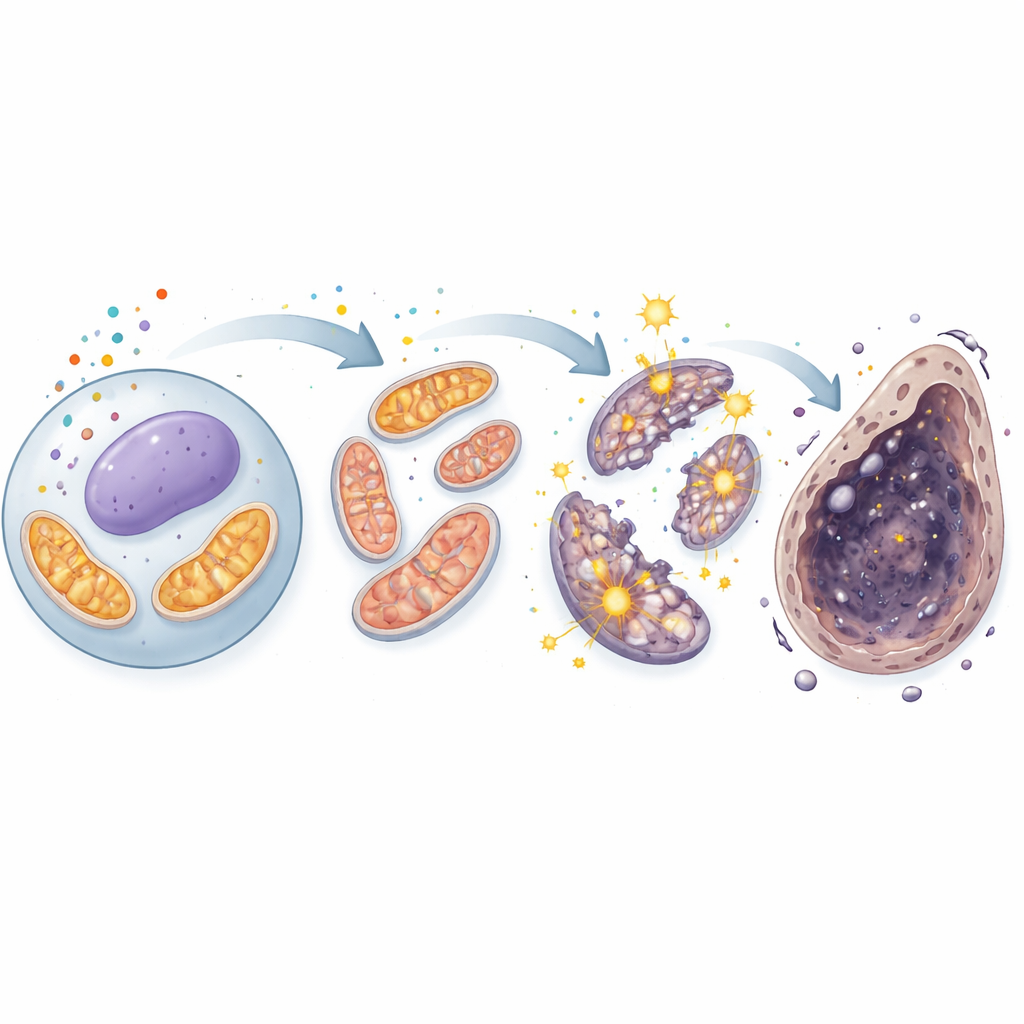
Błędne koło w elektrowni komórkowej
Wykorzystując kombinację profilowania aktywności genów i pomiarów metabolitów, badacze wykazali, że kadm robi coś więcej niż tylko uszkadza mitochondria — wydawał się przejmować ich podstawowy obieg energetyczny, czyli cykl kwasu szczawiooctowego (cykl TCA). Poziomy dwóch centralnych pośredników cyklu TCA — alfa‑ketoglutaranu i bursztynianu — wzrosły znacząco, a aktywność karboksylazy pirogronianowej, enzymu zasilającego cykl świeżym paliwem, została zwiększona. To sugeruje, że cykl TCA stał się paradoksalnie nadaktywny w uszkodzonych komórkach, wymuszając większy przepływ elektronów przez łańcuch oddechowy i wyciek większej ilości ROS. Dodatkowy ROS napędzał z kolei reakcje z żelazem i uszkodzenia błon, wzmacniając ferroptozę. Ponownie, inhibitory ferroptozy ograniczały te zniekształcenia metaboliczne, podkreślając ścisłe powiązanie między kadmem, mitochondrialnym przeładowaniem a żelazozależną śmiercią komórkową.
Co to oznacza dla płodności i przyszłych badań
Mówiąc wprost, badanie pokazuje, że kadm atakuje komórki tworzące plemniki, bezpośrednio uszkadzając ich mitochondria i wpędzając ich cykl energetyczny w szkodliwy nadbieg. Ta kombinacja zalewa komórki reaktywnymi cząsteczkami tlenu i zaburza równowagę żelaza, popychając je w kierunku ferroptozy. Ponieważ spermatocyty są niezbędne do wytworzenia zdrowych plemników, ich utrata pomaga wyjaśnić silne powiązanie między narażeniem na kadm a obniżoną płodnością męską. Choć eksperymenty przeprowadzono na komórkach mysich w hodowlach, dostarczają one klarownej mapy mechanistycznej, którą można zweryfikować w przyszłych badaniach na zwierzętach i ludziach. Praca wskazuje też potencjalne strategie ochronne: leki lub składniki odżywcze łagodzące stres mitochondrialny, modulujące cykl TCA lub zapobiegające żelazozależnemu uszkodzeniu błon mogłyby pomóc chronić układ rozrodczy mężczyzn przed metalami środowiskowymi, takimi jak kadm.
Cytowanie: Xiong, L., Yi, L., Zeng, X. et al. Cadmium induces ferroptosis in mouse spermatocytes by activating the ROS–TCA pathway. Sci Rep 16, 8449 (2026). https://doi.org/10.1038/s41598-026-38827-7
Słowa kluczowe: toksyczność kadmu, płodność męska, stres mitochondrialny, ferroptoza, reaktywne formy tlenu