Clear Sky Science · pl
Determinanty na poziomie reszt aminokwasowych stabilności termicznej ekstremofilnego endolizyny Ts2631
Dlaczego wirusy lubiące gorąco mają znaczenie dla przyszłych antybiotyków
Wraz ze wzrostem oporności na antybiotyki naukowcy ścigają się, by znaleźć nowe sposoby zabijania groźnych bakterii. Obiecujące podejście zapożycza narzędzia od wirusów infekujących bakterie, zwanych bakteriofagami. Te wirusy wytwarzają enzymy, zwane endolizynami, które przebijają ściany komórkowe bakterii. Opisywane badanie koncentruje się na niezwykle odpornej na wysoką temperaturę endolizynie Ts2631, pochodzącej od wirusa żyjącego w islandzkich gorących źródłach. Odkrywając, które pojedyncze elementy budulcowe tego białka odpowiadają za jego stabilność w temperaturach bliskich wrzenia, badacze liczą na zaprojektowanie bardziej wytrzymałych, trwalszych enzymów przeciwbakteryjnych do zastosowań medycznych i biotechnologicznych. 
Wirusowe narzędzie wykute w wrzących źródłach
Ts2631 pochodzi od bakteriofaga infekującego termofilną bakterię Thermus scotoductus, która dobrze rośnie w wodach osiągających znacznie powyżej 60 °C. Enzym Ts2631 przecina specyficzne wiązanie w peptydoglikanie, mocnej sieci otaczającej komórki bakteryjne. To, co wyróżnia Ts2631, to ekstremalna termostabilność: pozostaje złożony aż do około 100–105 °C, w zależności od roztworu. To znacznie powyżej temperatur, w których większość białek się rozpada. Autorzy porównali Ts2631 z jego najlepiej zbadanym krewniakiem z wirusa żyjącego w umiarkowanych temperaturach, lizozyminą T7, by ustalić, jakie strukturalne sztuczki wykorzystała natura, by utrzymać Ts2631 w całości w tak surowych warunkach.
Krótsze pętle i inny skład budulcowy
Białka to łańcuchy złożone z 20 rodzajów aminokwasów, pofałdowane w skomplikowane kształty. Gdy badacze nałożyli trójwymiarowe struktury Ts2631 i lizozyminy T7, stwierdzili, że ogólna architektura jest bardzo podobna: obie mają zwarty rdzeń z helis i arkuszy. Kluczowa różnica leży w elastycznych regionach pętli łączących te elementy. W Ts2631 pętle są krótsze i wykazują mniejszą elastyczność, podczas gdy lizozymina T7 ma dłuższe, bardziej wiotkie pętle. Ts2631 zawiera także więcej pewnych aminokwasów często powiązanych z odpornością na ciepło: sztywnej proliny; aromatycznych reszt, takich jak tyrozyna i tryptofan; oraz dodatnio naładowanej argininy. Jednocześnie ma mniej reszt seryny, kwasu asparaginowego i kwasu glutaminowego, które mogą czynić białka bardziej podatnymi w wysokich temperaturach. Ten wzorzec utrzymuje się nie tylko w porównaniu z lizozyminą T7, ale także gdy porównano Ts2631 z setkami tysięcy białek wirusowych i wieloma milionami bakteryjnych.
Wymiana pojedynczych aminokwasów, aby sprawdzić ich znaczenie
Aby przejść od korelacji do przyczynowości, zespół systematycznie zastąpił 55 pojedynczych aminokwasów w Ts2631 i zmierzył, jak każda mutacja wpłynęła na temperaturę topnienia (Tm) oraz zdolność enzymu do rozkładu ścian komórkowych bakterii. Niektóre zmiany wokół zawierającego cynk miejsca aktywnego były szczególnie szkodliwe. Kiedy zmieniono trzy reszty koordynujące cynk (H30, H131 i C139), Tm białka spadło o maksymalnie około 20 °C, a aktywność została utracona. Dwie konserwowane tyrozyny (Y60 i Y69) również przyczyniały się do stabilności. Co zaskakujące, usunięcie mostka dwusiarczkowego — rodzaju kowalencyjnego połączenia między cysteinami C80 i C90 — faktycznie podniosło temperaturę topnienia, choć zniszczyło aktywność. Pokazuje to, że bardzo duża stabilność w probówce nie zawsze oznacza lepsze funkcjonowanie białka w rzeczywistych warunkach. 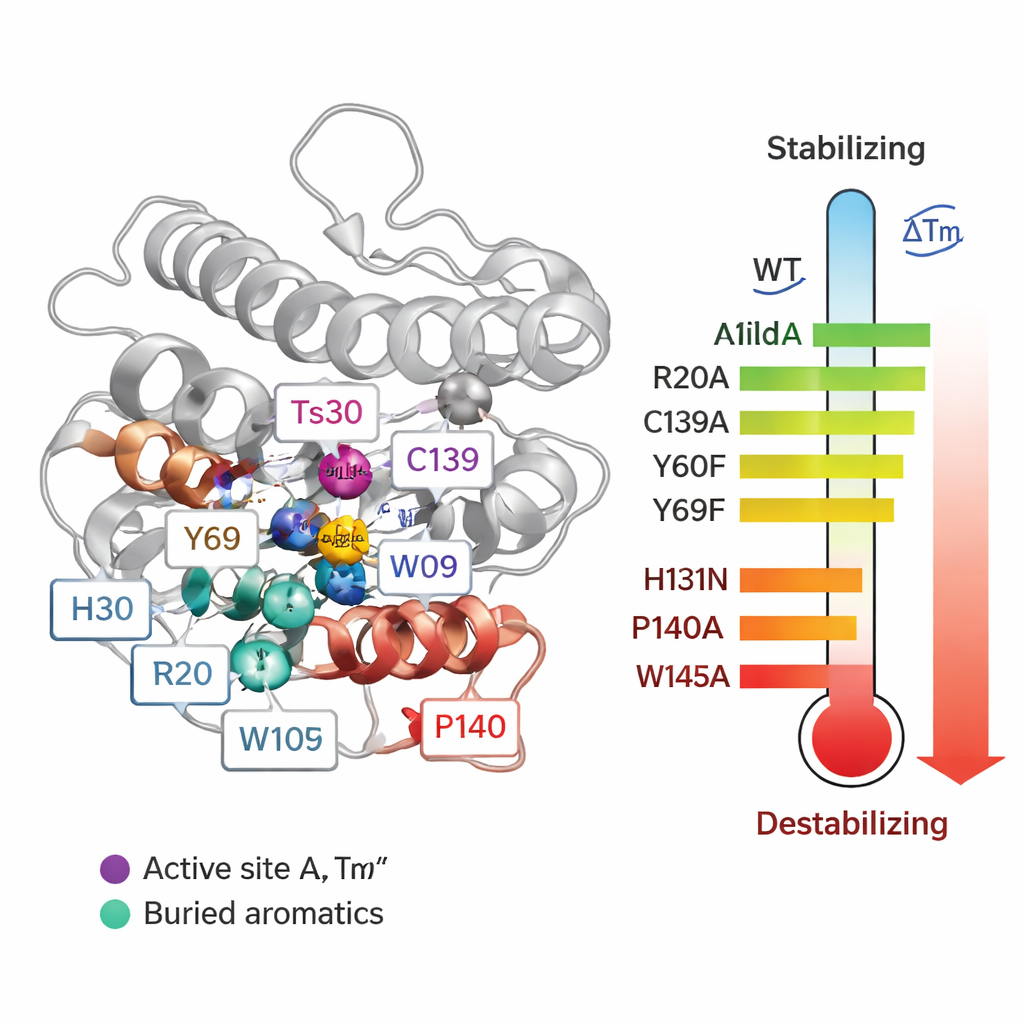
Ukryte aromatyczne „kotwice” i kluczowy chwyt ściany bakteryjnej
Najbardziej uderzające wyniki pochodziły z mutacji reszt proliny i tryptofanu. Zmiana pojedynczej proliny (P140), położonej tuż obok cysteiny C139 wiążącej cynk, obniżyła Tm o ponad 21 °C i osłabiła aktywność po ogrzewaniu, ponieważ mutacja zaburzyła specjalną geometrię wiązania niezbędną do prawidłowego wiązania metalu. Kilka głęboko zakopanych tryptofanów (W102, W109 i szczególnie W145) również okazało się krytycznych: zastąpienie ich alaniną spowodowało spadki Tm o 14–24 °C i sprawiło, że enzym stał się znacznie bardziej wrażliwy na ciepło podczas testów aktywności. Te aromatyczne reszty działają jak wewnętrzne kotwice, które blokują rdzeń białka na miejscu. Wśród arginin większość miała niewielki wpływ na stabilność, ale R20 okazał się niezbędny do chwytania peptydoglikanu. Po zastąpieniu R20 enzym słabo wiązał ścianę komórkową bakterii i tracił aktywność po ogrzewaniu, co ujawnia, że niektóre reszty bardziej przyczyniają się do funkcji niż do samej odporności termicznej.
Od enzymów z gorących źródeł do odporniejszych środków przeciwbakteryjnych
Podsumowując, badanie pokazuje, że niezwykła odporność termiczna Ts2631 opiera się na garstce dobrze umieszczonych aminokwasów, a nie na równomiernym wzmocnieniu całego białka. Reszty wiążące cynk, konserwowana prolina w pobliżu miejsca aktywnego i zakopane łańcuchy boczne aromatyczne tworzą stabilizujące jądro, podczas gdy niektóre klasyczne cechy stabilizujące, jak mostki dwusiarczkowe czy mostki solne, mają tu mniejsze znaczenie, niż można by się spodziewać. Dla szerszej dziedziny oznacza to, że mezofilowe (umiarkowane temperaturowo) endolizyny można uczynić bardziej trwałymi przez ostrożne podstawienie wybranych pozycji na tryptofan lub prolinę, nie poświęcając aktywności przeciwbakteryjnej. Innymi słowy, ucząc się, jak natura buduje enzymy odporne na temperatury bliskie wrzenia, naukowcy otrzymują praktyczny wzorzec do inżynierii bardziej niezawodnych, długowiecznych antybiotyków opartych na białkach.
Cytowanie: Cieminska, K., Kaczorowska, AK., Kozlowski, L.P. et al. Residue-level determinants of the thermal stability of the extremophilic Ts2631 endolysin. Sci Rep 16, 7630 (2026). https://doi.org/10.1038/s41598-026-38786-z
Słowa kluczowe: termotolerancyjna endolizyna, enzymy bakteriofagów, termostabilność białek, oporność na antybiotyki, inżynieria białek