Clear Sky Science · pl
Badanie biomarkerów przemiany komórek mięśni gładkich naczyń w komórki piankowate wywołanej homocysteiną
Dlaczego zatkane tętnice zaczynają się od drobnych zmian w komórkach
Miażdżyca — powolne zatkanie i stwardnienie tętnic — jest jedną z głównych przyczyn zawałów serca i udarów. Zwykle słyszymy o cholesterolu i diecie, rzadziej o tym, jak poszczególne komórki w ścianie naczynia zmieniają się w przebiegu choroby. To badanie skupia się na jednym z takich czynników — cząsteczce krwi zwanej homocysteiną — i pokazuje, jak może ona skłaniać zwykle dobrze funkcjonujące komórki mięśniowe w tętnicach do gromadzenia tłuszczu i przemiany w tzw. komórki piankowate, budulcowe elementy niebezpiecznych blaszek.
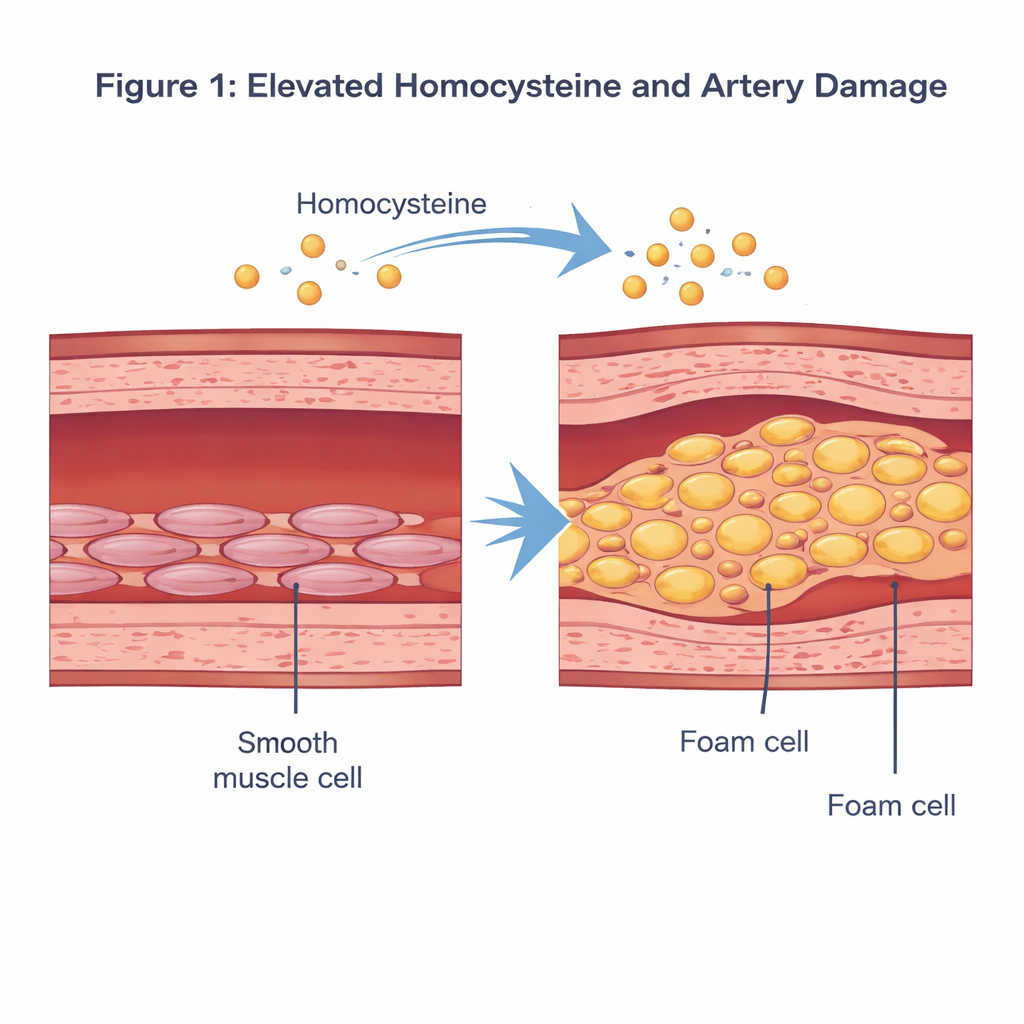
Aminokwas‑sprawca problemów we krwi
Homocysteina to siarkowy aminokwas powstający podczas przetwarzania przez organizm metioniny, składnika diety. W normalnych warunkach jej stężenie we krwi jest niskie. Gdy przekracza około 15 mikromoli na litr — stan zwany hiperhomocysteinemią — badania epidemiologiczne wiążą to ze zwiększonym ryzykiem chorób układu sercowo‑naczyniowego. Wcześniejsze prace sugerowały, że nadmiar homocysteiny może uszkadzać wewnętrzną wyściółkę tętnic, wywoływać stan zapalny i zmieniać zachowanie komórek mięśni gładkich naczyń, które znajdują się w środkowej warstwie ściany naczynia i pomagają regulować ciśnienie krwi przez kurczenie się i rozkurczanie.
Jak komórki mięśni tętnic zmieniają się w zapełnione tłuszczem komórki piankowate
Naukowcy skupili się na tym, jak homocysteina przebudowuje te komórki mięśniowe. W hodowlach laboratoryjnych poddali ludzkie komórki mięśni gładkich naczyń dawce homocysteiny odzwierciedlającej stan chorobowy i porównali je z komórkami nieleczonymi. Przy użyciu standardowych barwień i testów biochemicznych zaobserwowali, że komórki traktowane homocysteiną wypełniały się czerwonymi kroplami tłuszczu, a ich poziomy cholesterolu i triglicerydów gwałtownie wzrosły. Jednocześnie spadły białkowe markery ich zwykłej „kurczliwej” tożsamości, podczas gdy wzrosły markery stanu bardziej syntetycznego i sprzyjającego tworzeniu blaszek. Razem te zmiany pokazują, że homocysteina może odciągać komórki mięśniowe od ich normalnej roli i prowadzić je do fenotypu przypominającego komórki piankowate, obładowanego lipidami, który bezpośrednio przyczynia się do powstawania blaszek.
Poszukiwanie molekularnych odcisków palców wewnątrz komórek
Aby ustalić, które białka zmieniają się w trakcie tej przemiany, zespół sięgnął po nowoczesną proteomikę — technologię mierzącą tysiące białek jednocześnie. Porównali poziomy białek w komórkach traktowanych homocysteiną i w kontrolach i wiarygodnie zmierzyli prawie 4800 białek. Spośród nich 54 wyróżniały się istotnymi zmianami: 13 zwiększyło się, a 41 zmalało. Wiele z przemieszczających się białek uczestniczy w gospodarce lipidowej, przeżyciu komórki, stresie oksydacyjnym oraz przebudowie strukturalnej komórek. Autorzy wykorzystali następnie narzędzia bioinformatyczne do grupowania tych białek w funkcjonalne szlaki i mapowania interakcji między nimi, uwypuklając sieci powiązane z metabolizmem cholesterolu i reakcjami stresowymi w ścianie naczynia.
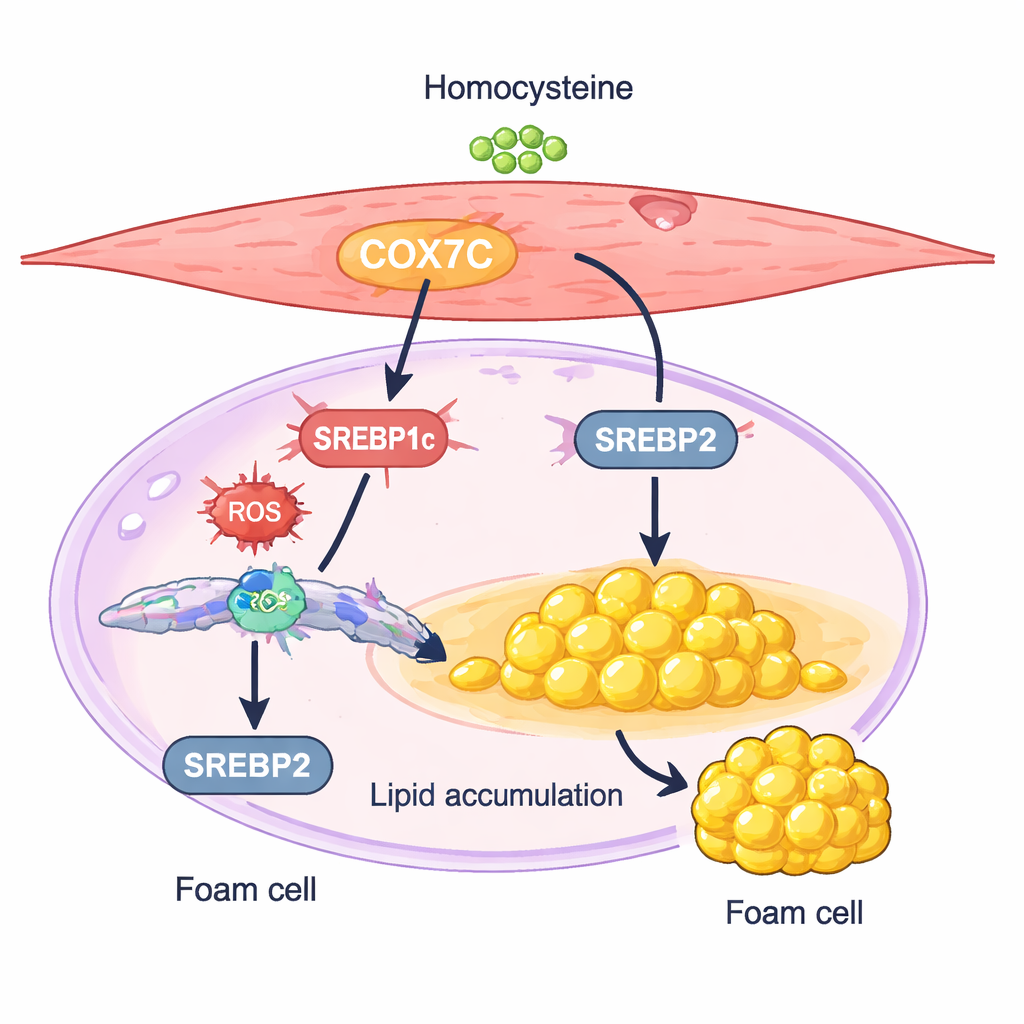
Mitochondrialny przełącznik, który popycha komórki do magazynowania tłuszczu
Jedno białko, zwane COX7C, wyłoniło się jako szczególnie interesujący podejrzany. COX7C jest składnikiem „elektrowni” komórkowych, mitochondriów, gdzie pomaga w zarządzaniu produkcją energii. W komórkach mięśni gładkich traktowanych homocysteiną poziomy COX7C były wyższe niż w kontrolach. Badacze wykazali, że dalsze zwiększenie COX7C sprawiało, iż komórki akumulowały jeszcze więcej tłuszczu i wykazywały wyższe poziomy dwóch głównych regulatorów produkcji lipidów, SREBP1c i SREBP2. Wyciszenie COX7C dawało efekt odwrotny: osłabiało aktywność SREBP, zmniejszało gromadzenie cholesterolu i triglicerydów oraz łagodziło zmiany przypominające komórki piankowate. Wyniki te wspierają model, w którym homocysteina podnosi poziom COX7C w mitochondriach, zwiększa wewnątrzkomórkowe sygnały stresowe, a w konsekwencji aktywuje syntezę lipidów napędzaną przez SREBP, przechylając komórki mięśniowe w kierunku stanu magazynowania lipidów.
Co to oznacza dla zdrowia serca i przyszłych terapii
Ta praca nie dowodzi jeszcze, że to samo dzieje się w ludzkich tętnicach, ponieważ wykonano ją na komórkach hodowlanych, a nie u pacjentów. Mimo to dostarcza szczegółowego wglądu w to, jak podwyższona homocysteina może pomagać przekształcać pomocne komórki mięśni tętnic w szkodliwe komórki piankowate i identyfikuje COX7C oraz powiązane białka jako potencjalne biomarkery lub cele terapeutyczne. Dla laika kluczowy przekaz jest taki, że poza „dobrym” i „złym” cholesterolem drobne przesunięcia w chemii krwi — jak nadmiar homocysteiny — mogą wewnętrznie przeprogramowywać ścianę naczynia. Wskazując molekularnych graczy, takich jak COX7C i szlak SREBP, badanie to tworzy podstawy pod przyszłe strategie mające powstrzymać tworzenie się blaszek, poprzez uniemożliwienie komórkom tętniczym zamiany w miniaturowe składy tłuszczu.
Cytowanie: Wang, X., Ma, X., Zhang, X. et al. Study on biomarkers of homocysteine-induced transformation of vascular smooth muscle cells into foam cells. Sci Rep 16, 7411 (2026). https://doi.org/10.1038/s41598-026-38763-6
Słowa kluczowe: miażdżyca, homocysteina, komórki piankowate, komórki mięśni gładkich naczyń, COX7C