Clear Sky Science · pl
Aktywacja transkrypcyjna LINGO1 ułatwia proliferację i ucieczkę przed układem odpornościowym w raku jelita grubego
Dlaczego białko mózgowe ma znaczenie w raku jelita
Rak jelita grubego jest jednym z najczęstszych i najbardziej śmiertelnych nowotworów na świecie, a wielu pacjentów nadal doświadcza nawrotów lub rozsiewu choroby mimo zabiegów chirurgicznych, chemioterapii i nowych leków immunologicznych. W badaniu skupiono się na mało znanej cząsteczce zwanej LINGO1, początkowo badanej w mózgu, i wykazano, że może ona wspierać wzrost guzów jelita oraz ich ukrywanie przed obroną organizmu. Zrozumienie tej nowej roli może poprawić prognozowanie i w przyszłości otworzyć drogę do bardziej precyzyjnych terapii.
Ukryty przełącznik podkręcony w komórkach nowotworowych
Naukowcy najpierw sprawdzili, czy poziomy LINGO1 różnią się między zdrową a nowotworową tkanką jelita. Korzystając z dużych publicznych baz danych genowych i kilku niezależnych grup pacjentów, stwierdzili, że LINGO1 jest konsekwentnie znacznie wyższy w guzach jelita grubego niż w przyległej tkance normalnej. Pacjenci, których guzy zawierały więcej LINGO1, mieli częściej zaawansowaną chorobę, zajęcie węzłów chłonnych, przerzuty odległe i krótsze przeżycie. Nawet po uwzględnieniu innych czynników klinicznych, LINGO1 pozostawał niezależnym wskaźnikiem ostrzegawczym, sugerując, że działa jak "pokrętło głośności", które po podkręceniu oznacza bardziej agresywny nowotwór.
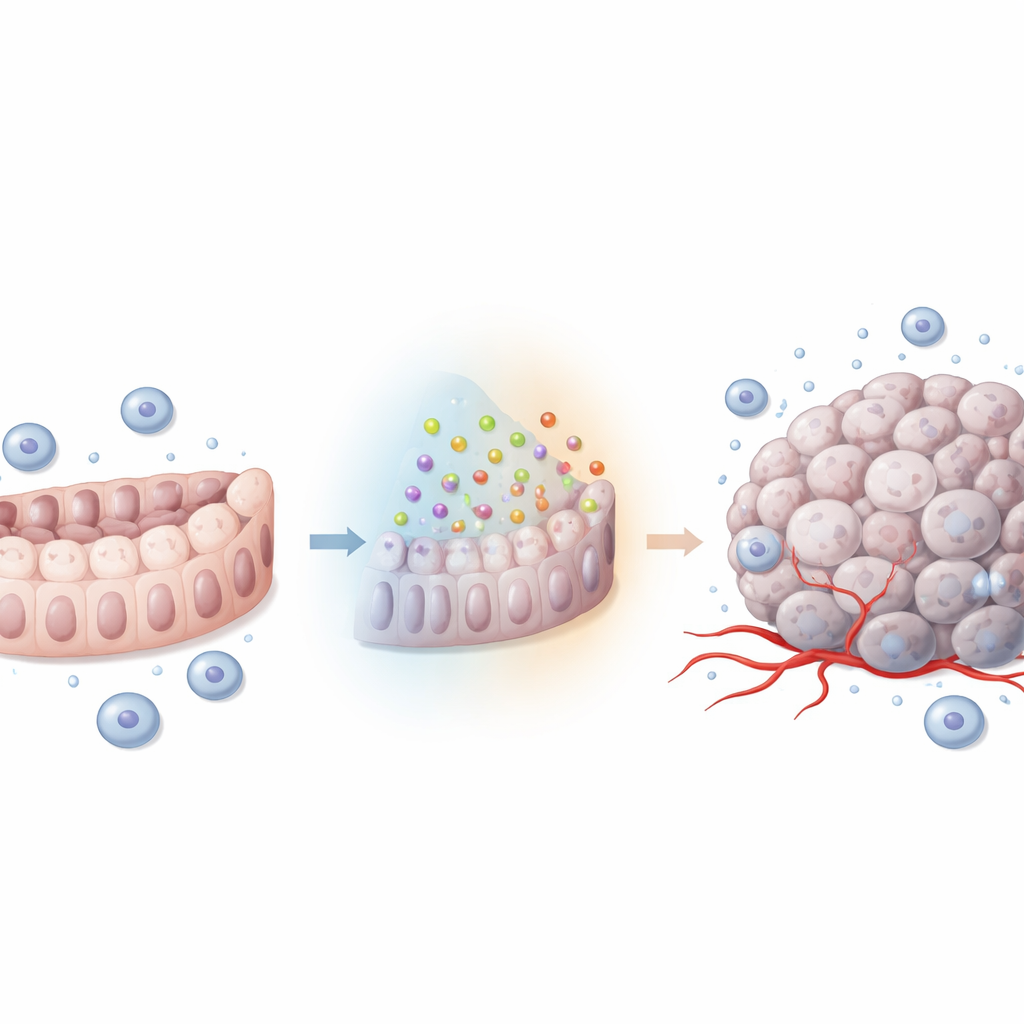
Od aktywności genu do szybszego wzrostu i rozsiewu
Aby wyjść poza statystyki, zespół przetestował, co się dzieje po zmniejszeniu lub zwiększeniu poziomu LINGO1 w komórkach raka jelita hodowanych w laboratorium. Gdy obniżono LINGO1, komórki nowotworowe dzieliły się wolniej, tworzyły mniej kolonii i miały mniejszą zdolność do przemieszczania się przez sztuczne membrany imitujące bariery tkankowe. Były też słabsze w pobudzaniu wzrostu i ruchu komórek naczyń krwionośnych, co sugeruje, że guzy z mniejszą ilością LINGO1 mogą mieć utrudnione zasilanie. Po zwiększeniu LINGO1 w innej linii komórkowej raka jelita zaobserwowano odwrotny efekt: wzrost, migracja, inwazja i zdolność stymulowania naczyń krwionośnych wzrosły. U myszy implantowane guzy z wyłączonym LINGO1 rosły wolniej i wykazywały mniej komórek w aktywnej fazie podziału, co bezpośrednio wiąże tę cząsteczkę z ekspansją guza in vivo.
Jak LINGO1 przekształca otoczenie guza
Badanie analizowało także, które geny i szlaki są bardziej aktywne przy wysokim poziomie LINGO1. Wzorce aktywności genów wskazywały na znane programy nowotworowe, w tym te, które rozluźniają więzi międzykomórkowe ułatwiając migrację komórek, oraz te pobudzające tworzenie nowych naczyń. Co równie istotne, wysoki LINGO1 wiązał się ze zmianami w „ekosystemie” guza. Guzy bogate w LINGO1 zawierały mniej cytotoksycznych limfocytów T — komórek odpornościowych zdolnych bezpośrednio atakować nowotwór — oraz więcej typów komórek hamujących odpowiedź immunologiczną, takich jak niektóre makrofagi i komórki regulatorowe T. Wiele molekularnych „hamulców” blokujących atak immunologiczny, powszechnie określanych jako punkty kontrolne odporności, było również bardziej aktywnych przy podwyższonym LINGO1. Próbki kliniczne potwierdziły, że obszary o wysokim LINGO1 miały skąpość cytotoksycznych limfocytów T i słabe oznaki aktywności niszczącej komórki, podczas gdy obszary o niskim poziomie LINGO1 były zapełnione aktywnymi komórkami odpornościowymi.
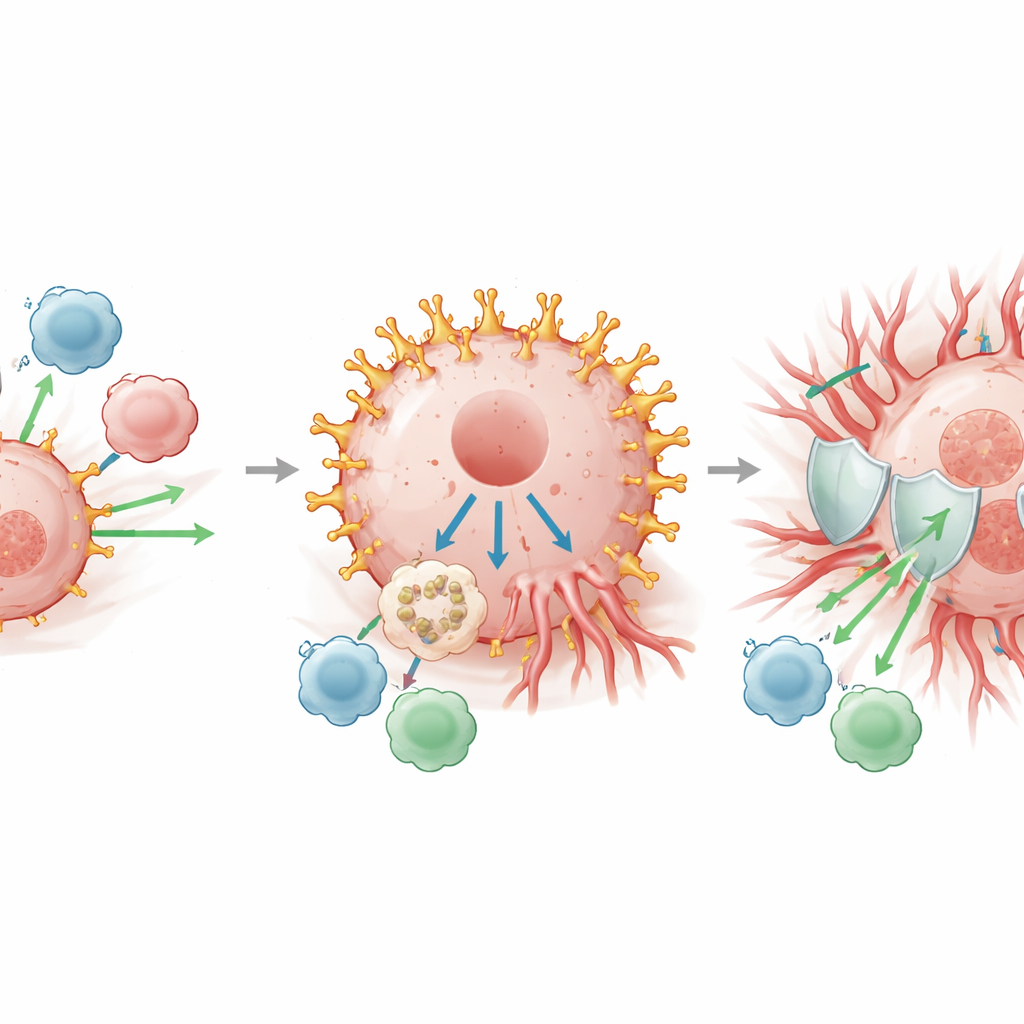
Możliwy punkt kontroli powyżej
Aby zrozumieć, dlaczego LINGO1 jest tak wysoki w tych guzach, autorzy poszukiwali białek kontrolnych działających jak przełączniki w regionie regulatorowym tego genu. Zidentyfikowali czynnik o nazwie USF1, który może wiązać się bezpośrednio z kontrolnym regionem LINGO1. W eksperymentach raportera dodanie większej ilości USF1 znacząco zwiększyło aktywność tego regionu, ale tylko gdy miejsce dokowania było nienaruszone. Sugeruje to, że przynajmniej w niektórych rakach jelita grubego USF1 pomaga podkręcić LINGO1, co z kolei napędza szybszy wzrost guza i tworzy bardziej nieprzyjazne środowisko dla komórek odpornościowych. Praca wykazała także, że LINGO1 jest nieprawidłowo podwyższony i często wiązany z gorszymi wynikami w kilku innych rodzajach nowotworów, co wskazuje, że jego wpływ może wykraczać poza jelito.
Co to oznacza dla pacjentów i przyszłej opieki
Podsumowując, badanie przedstawia LINGO1 jako dwuzadaniowego współuczestnika w raku jelita grubego: pobudza komórki nowotworowe do wzrostu, migracji i wspierania neowaskularyzacji, jednocześnie pomagając guzowi izolować się przed atakiem immunologicznym. Ponieważ jego poziomy przewidują bardziej zaawansowaną chorobę i gorsze przeżycie, LINGO1 mógłby służyć jako biomarker identyfikujący pacjentów o wyższym ryzyku. W dłuższej perspektywie leki obniżające aktywność LINGO1 — lub zakłócające jego kontrolę przez USF1 — mogłyby nie tylko spowalniać wzrost guza, ale także uczynić nowotwory bardziej rozpoznawalnymi dla układu odpornościowego i bardziej podatnymi na immunoterapię.
Cytowanie: Ma, P., Yao, F., Yue, P. et al. Transcriptional activation of LINGO1 facilitates proliferation and immune escape in colorectal cancer. Sci Rep 16, 9360 (2026). https://doi.org/10.1038/s41598-026-38760-9
Słowa kluczowe: rak jelita grubego, immunologia nowotworu, biomarkery, mikrosrodowisko guza, postęp nowotworu