Clear Sky Science · pl
Podgrzanie kolistymetanu sodu zwiększa jego skuteczność przeciwko wieloopornym i szeroko opornym pałeczkom Gram-ujemnym w płynie konserwującym
Dlaczego to ma znaczenie dla pacjentów po przeszczepie
Gdy ktoś otrzymuje ratujący życie przeszczep narządu, pobrany organ spędza godziny w schłodzonym płynie konserwującym przed operacją. Ten płyn czasami może zawierać niebezpieczne, silnie oporne na leki bakterie, które mogą powodować ciężkie zakażenia u już osłabionych pacjentów. W badaniu przeanalizowano zaskakująco prosty pomysł: niewielkie „podgotowanie” powszechnie stosowanego antybiotyku ostatniej instancji przed dodaniem go do płynu konserwującego, aby sprawdzić, czy zwiększa to jego skuteczność przeciwko tym trudnym do leczenia drobnoustrojom bez uszkadzania narządu.
Ukryte zarazki w kąpieli chłodzącej
Przeszczepiane narządy, takie jak nerki, są przepłukiwane i przechowywane w specjalnym płynie konserwującym podczas transportu od dawcy do biorcy. Badania pokazują, że ten płyn często jest skażony drobnoustrojami, zwłaszcza grupą pałeczek Gram-ujemnych, w tym znanymi szpitalnymi patogenami jak Pseudomonas, Klebsiella, Escherichia coli oraz Acinetobacter. Wiele z tych szczepów jest obecnie wieloopornych lub szeroko opornych, co oznacza, że opierają się większości standardowych antybiotyków. Choć nie każde skażenie prowadzi do zakażenia, transmisja tych odpornych drobnoustrojów do biorcy przeszczepu może skutkować dłuższym pobytem na intensywnej terapii, uszkodzeniem nerek, utratą przeszczepu, a nawet śmiercią.
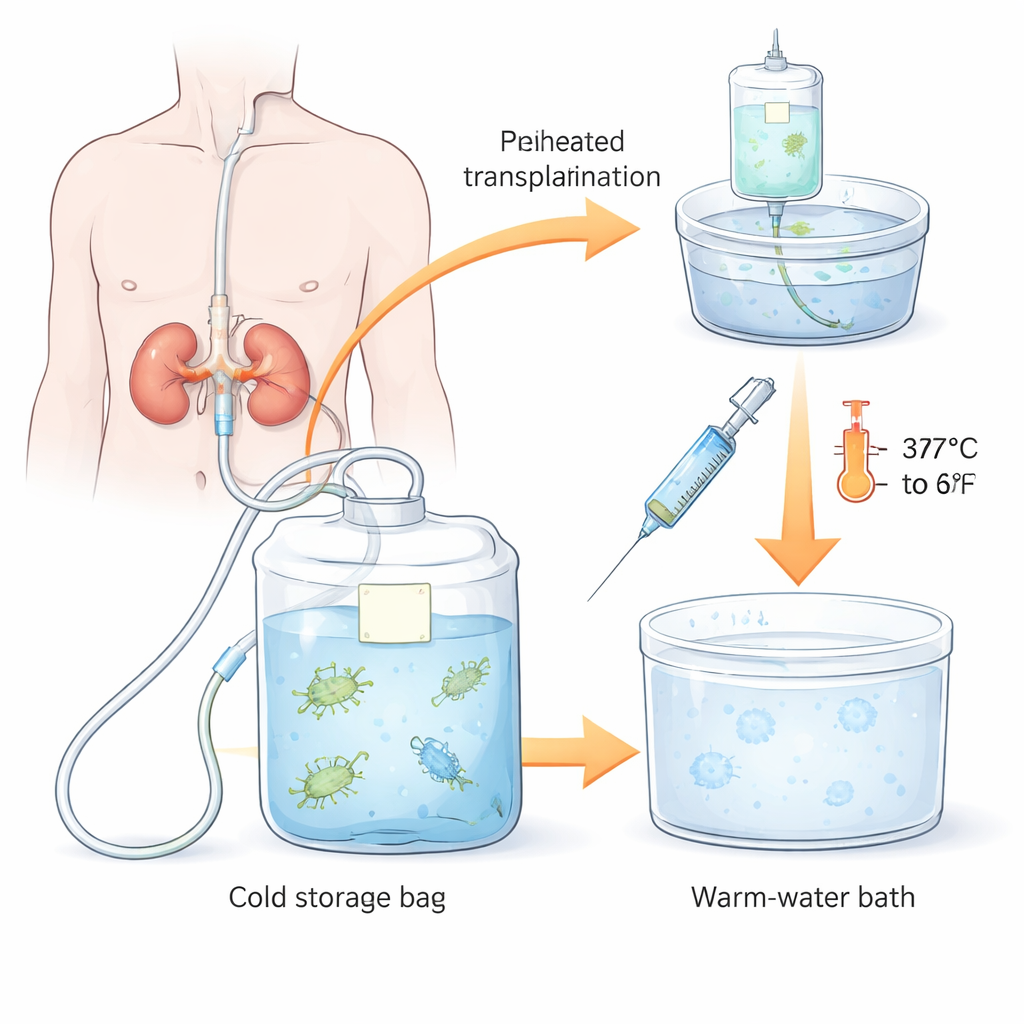
Antybiotyk ostatniej szansy z termicznym twistem
Naukowcy skupili się na kolistymetanie sodu (CMS), powszechnie dostępnym leku szpitalnym stosowanym jako leczenie z ostatniej linii przeciw wieloopornym pałeczkom Gram-ujemnym. Sam CMS jest prolekiem — musi się powoli rozłożyć do kolistyny, rzeczywistej substancji aktywnej atakującej zewnętrzne błony bakterii. Ta konwersja zwykle zachodzi przez wiele godzin w temperaturze ciała. Zespół zastanawiał się, czy można przyspieszyć ten etap aktywacji przez delikatne podgrzanie CMS w roztworze przed ponownym schłodzeniem i dodaniem go do płynu konserwującego. Testowali różne kombinacje temperatur (37 °C versus 60 °C) i czasu podgrzewania (5 do 30 minut) w warunkach naśladujących statyczne przechowywanie narządów w niskich temperaturach.
Podgrzewanie znacznie zwiększa zabijanie bakterii
W eksperymentach laboratoryjnych zespół wystawił podgrzany CMS na działanie pięciu rzeczywistych szczepów szpitalnych: czterech pałeczek Gram-ujemnych opornych na leki — karbapenemoodpornego Pseudomonas aeruginosa, Klebsiella pneumoniae, E. coli i Acinetobacter baumannii — oraz jednego szczepu Gram-dodatniego, metycylinoopornego Staphylococcus aureus (MRSA). Po trzech godzinach w warunkach zimnego przechowywania policzyli przeżywające bakterie. Podgrzewanie CMS w 60 °C przez 15–30 minut prowadziło do dramatycznych redukcji we wszystkich czterech pałeczkach Gram-ujemnych: niektóre szczepy zostały niemal całkowicie zniszczone, ze średnimi wskaźnikami zahamowania zbliżającymi się do 100% lub je osiągającymi. Niższa temperatura 37 °C przynosiła tylko skromną poprawę i dopiero przy dłuższym czasie, przy czym była znacznie mniej wiarygodna. MRSA, mający inną strukturę ściany komórkowej, pozostał nieczuły, co odpowiada znanej ograniczonej aktywności kolistyny przeciw bakteriom Gram-dodatnim.
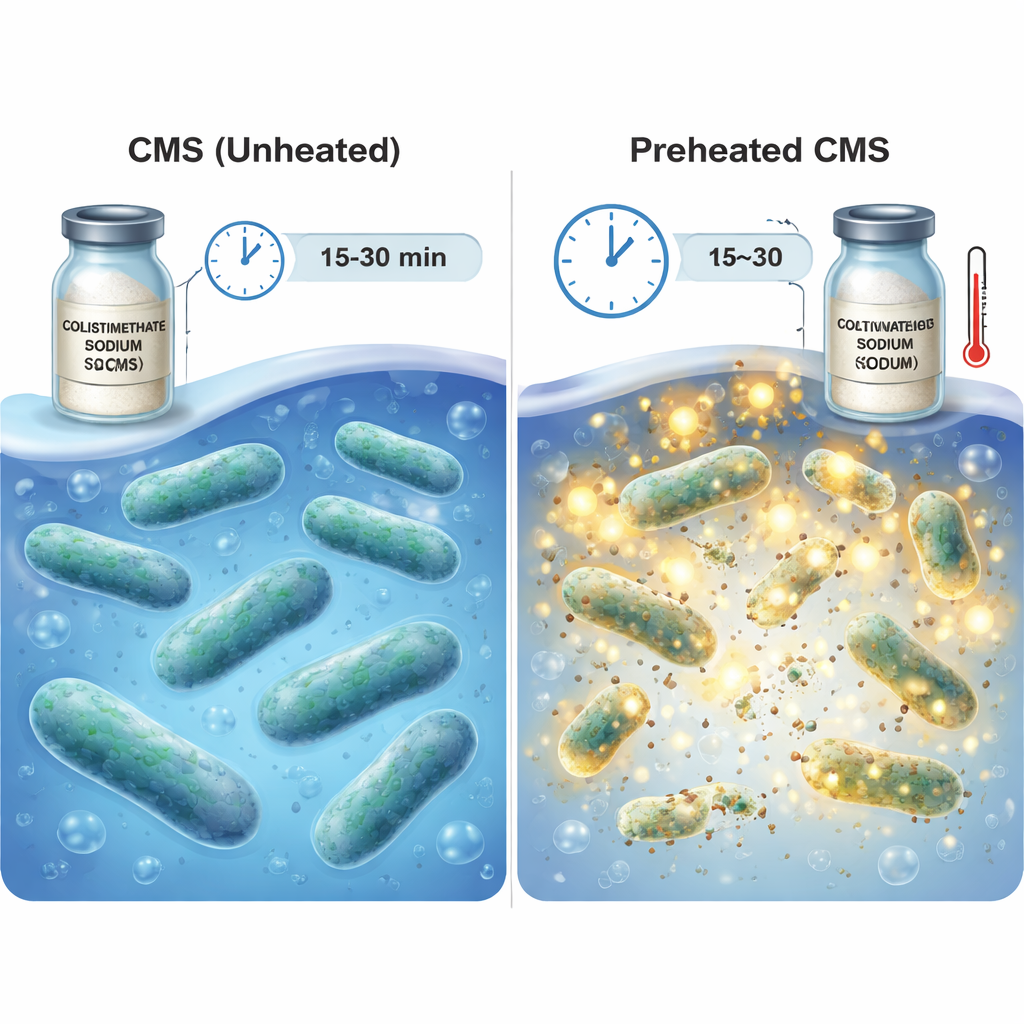
Sprawdzanie bezpieczeństwa dla nerki
Ponieważ leki z grupy polimyksyn, takie jak kolistyna, mogą uszkadzać nerki, gdy podaje się je pacjentom przez wiele dni, naukowcy sprawdzili także, czy ich mieszanka podgrzanego CMS uszkodzi komórki nerkowe w krótszym okresie, w którym organy dawcy są przechowywane na lodzie. Narażali ludzkie komórki kanalików nerkowych na podgrzany CMS w zimnych warunkach przez 3, 6 lub 18 godzin. Przez okres do 6 godzin — ramę czasową najbardziej istotną dla transportu narządów — komórki wyglądały normalnie pod mikroskopem i nie wykazywały istotnego spadku żywotności w porównaniu z komórkami nieleczonymi. Dopiero po 18 godzinach ciągłej ekspozycji pojawiły się wyraźne oznaki uszkodzenia komórek, co sugeruje, że krótkotrwałe, jednorazowe zastosowanie w płynie konserwującym może być znacznie bezpieczniejsze niż długotrwałe leczenie u żywych pacjentów.
Możliwe konsekwencje dla przeszczepów
Dla nie-specjalisty kluczowy przekaz jest taki, że prosty krok polegający na podgrzaniu i ponownym schłodzeniu istniejącego antybiotyku może znacząco poprawić jego zdolność do oczyszczenia płynu otaczającego organ dawcy podczas transportu. Podgrzanie CMS w 60 °C przez 15–30 minut, a następnie dodanie go do płynu konserwującego, szybko zabija w warunkach laboratoryjnych wiele z najbardziej obawianych wieloopornych pałeczek Gram-ujemnych, bez widocznych krótkoterminowych szkód dla komórek nerkowych w warunkach zimnego przechowywania. Jeśli dalsze badania potwierdzą te wyniki w rzeczywistych warunkach przeszczepowych i dopracują optymalny przepis temperatura-czas, ta niskotechnologiczna modyfikacja mogłaby zmniejszyć wczesne zakażenia po przeszczepie i uczynić rzadkie narządy dawcy bezpieczniejszymi i bardziej użytecznymi.
Cytowanie: Tang, D., Zhang, L., Duan, Y. et al. Preheating colistimethate sodium enhances its efficacy against multi/extensively drug-resistant Gram-negative bacilli in preservation fluid. Sci Rep 16, 7523 (2026). https://doi.org/10.1038/s41598-026-38748-5
Słowa kluczowe: przeszczepy narządów, bakterie oporne na leki, płyn konserwujący, kolistyna, podgrzewanie antybiotyku