Clear Sky Science · pl
Skuteczność fitochemikaliów pochodzących z Artocarpus heterophyllus (chlebowiec) jako inhibitorów proteazy NS2B/NS3 wirusa dengi: badanie in-silico
Dlaczego chlebowiec ma znaczenie przy chorobie przenoszonej przez komary
Gorączka denga, przenoszona przez komary, zakaża każdego roku miliony osób i czasem bywa śmiertelna. Mimo to lekarze wciąż nie dysponują powszechnie dostępnym lekiem doustnym, który bezpośrednio zatrzymywałby wirusa po zakażeniu. W tym badaniu zbadano nietypowe źródło potencjalnych terapii: naturalne związki występujące w chlebowcu (jackfruit), powszechnym drzewie tropikalnym. Korzystając z zaawansowanych symulacji komputerowych, badacze sprawdzili, czy którykolwiek z tych związków roślinnych mógłby przyłączyć się do kluczowej części wirusa i spowolnić jego działanie.
Wirusowe „nożyce” jako ważny słaby punkt
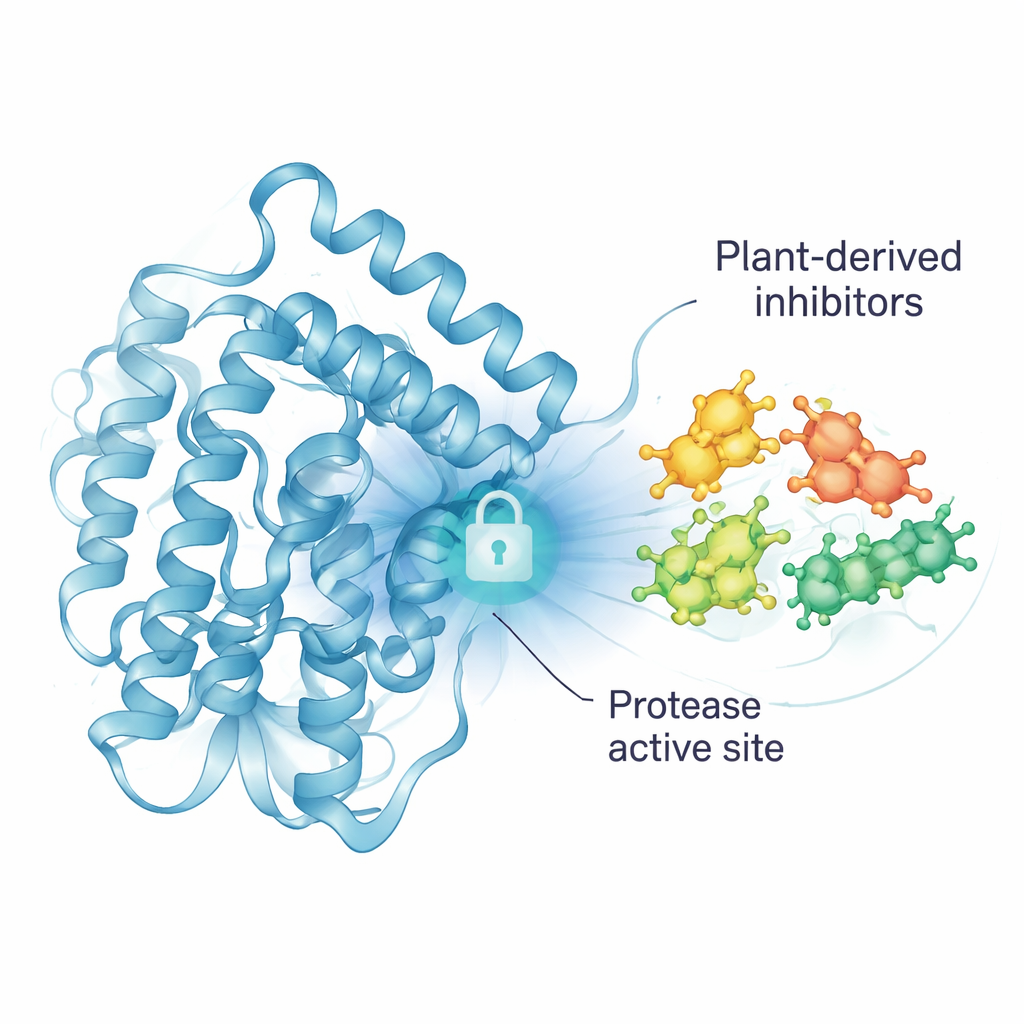
Aby mnożyć się w organizmie, wirus dengi polega na molekularnych „nożycach” zwanych proteazą NS2B/NS3. Ta mikroskopijna maszyna tnie długi łańcuch białka wirusa na mniejsze, funkcjonalne fragmenty. Jeśli nożyce zostaną zablokowane, wirus nie może się prawidłowo złożyć i infekcja powinna się zatrzymać. Z tego powodu naukowcy na całym świecie uważają tę proteazę za główny cel dla leków przeciwwirusowych. Jednak wcześniejsze próby projektowania takich leków często kończyły się niepowodzeniem ze względu na słabą skuteczność, działania niepożądane lub brak efektu w badaniach klinicznych, dlatego wciąż pilnie potrzebne są nowe klasy molekuł.
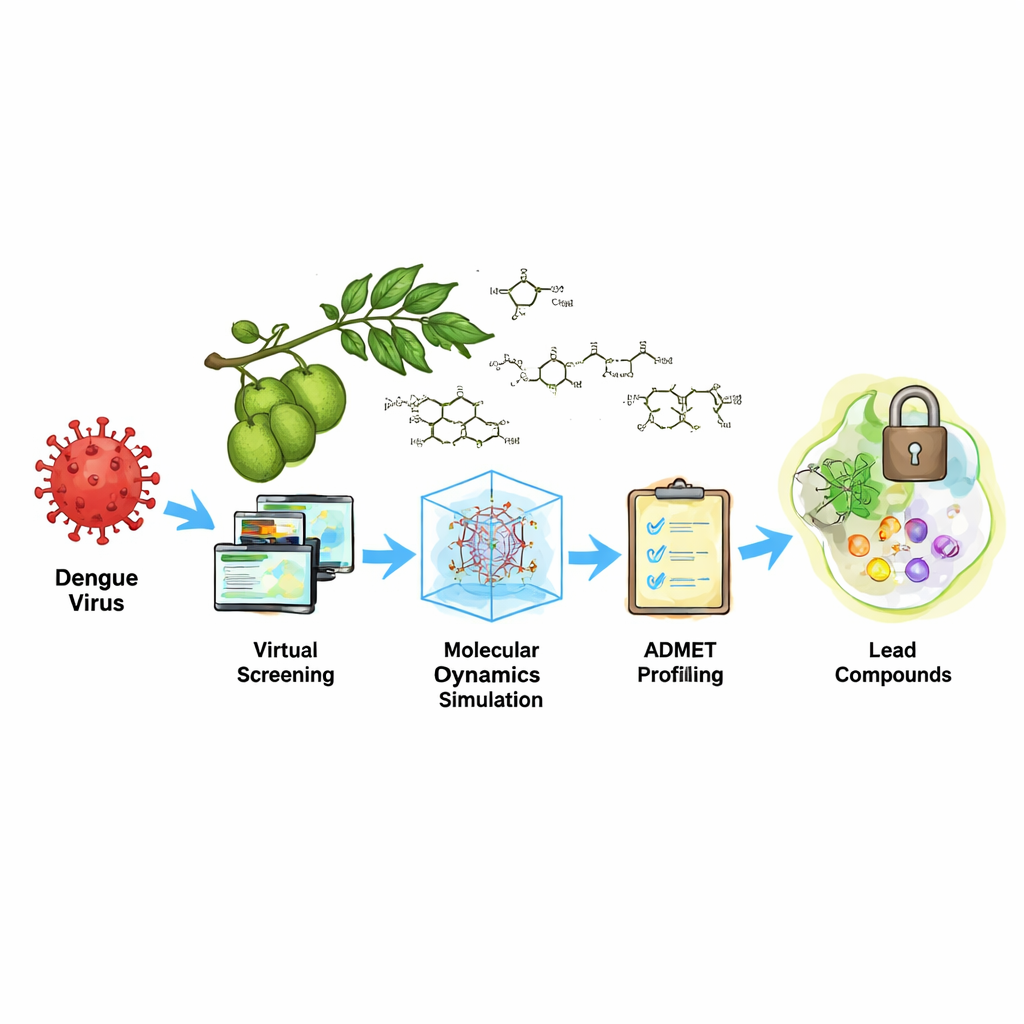
Chemia chlebowca poddana próbie
Chlebowiec ma długą historię zastosowań w medycynie tradycyjnej i jest bogaty w różnorodne związki roślinne. Zespół zgromadził 47 znanych związków z chlebowca z baz danych naukowych i przygotował je do „screeningu wirtualnego”. W tym procesie programy komputerowe szacują, jak dobrze każdy związek mógłby dopasować się do miejsca aktywnego proteazy — szczeliny tnącej wirusowych nożyc. Badacze zastosowali kilka etapów obliczeń dokujących, by przewidzieć, jak silnie każda molekuła może wiązać się z celem oraz jak dobrze odpowiada jego kształtowi i rozkładowi ładunku. Następnie użyli bardziej szczegółowej metody obliczania energii, znanej jako MM-GBSA, aby zawęzić listę kandydatów i skupić się na tych o najsilniejszym przewidywanym uchwycie.
Trzy wyróżniające się molekuły
Z początkowych 47 związków trzy molekuły z chlebowca wysunęły się na prowadzenie: Oxidihydroartocarpesin, Cyanomaclurin i Dihydromorin. Wszystkie trzy przewidywano, że zagnieżdżą się w aktywnej szczelinie proteazy i utworzą liczne kontakty niekowalencyjne z tzw. triadą katalityczną — trzema aminokwasami (His51, Asp75, Ser135) odpowiedzialnymi za cięcie. Kontakty te obejmowały wiązania wodorowe oraz oddziaływania hydrofobowe, które razem pomagają utrzymać związki na miejscu. W obliczeniach energetycznych trzy molekuły wykazały korzystniejsze wiązanie niż wiele innych badanych związków i wypadały podobnie do znanego inhibitora referencyjnego, co sugeruje, że mogłyby zakłócić funkcję proteazy.
Symulacja wirusowej maszyny w ruchu
Białka nie są posągami; poruszają się i wyginają w wodzie i w komórkach. Aby zobaczyć, jak stabilne byłyby związki z chlebowca w czasie, badacze przeprowadzili długie symulacje dynamiki molekularnej, praktycznie obserwując interakcje proteazy z każdą kandydatką przez dziesiątki nanosekund w środowisku wirtualnym. Gdy żadna molekuła nie była związana, proteaza przesuwała się i kołysała bardziej, zwłaszcza wokół miejsca aktywnego. Gdy związki z chlebowca były związane, ogólna struktura stała się bardziej zwarta i stabilna. Ruch w pobliżu kluczowych reszt katalitycznych zmniejszył się, a powierzchnia białka wystawiona na kontakt z wodą nieco się skurczyła. Zmiany te sugerują, że związki pomagają „zakleszczyć” proteazę w mniej elastycznej formie, która gorzej radzi sobie z cięciem wirusowych celów.
Wskazówki dotyczące bezpieczeństwa i dalsze kroki
Zespół użył także narzędzi online do oszacowania, jak trzy związki mogą zachowywać się w organizmie człowieka — czy mogą być wchłaniane, czy mogą uszkadzać wątrobę lub powodować uszkodzenia genetyczne. Wczesne sygnały były mieszane: molekuły generalnie spełniały wiele kryteriów „lekopodobnego” zachowania i nie wzbudzały niepokojów w zakresie uszkodzeń wątroby ani niektórych typów toksyczności. Jednak prognozy sugerowały możliwe ryzyko efektów przypominających działania kancerogenne, co wymagałoby dokładnego sprawdzenia w badaniach laboratoryjnych i na zwierzętach. Z tego powodu autorzy postrzegają te związki jako punkty wyjścia, czyli struktury „lead”, a nie gotowe leki.
Co to znaczy dla przyszłych terapii przeciw dengie
Dla czytelników niezajmujących się na co dzień tematem najważniejszym przekazem jest to, że pospolite rośliny, takie jak chlebowiec, mogą kryć obiecujące projekty przyszłych leków przeciwwirusowych. To badanie nie testowało związków w komórkach ani u zwierząt, więc nie oferuje dziś lekarstwa na dengę. Zamiast tego wykorzystuje zaawansowane metody komputerowe, by zawęzić dużą listę naturalnych molekuł do kilku, które najprawdopodobniej zablokują istotną maszynę wirusową. Wskazując projektantom leków na Cyanomaclurin, Oxidihydroartocarpesin i Dihydromorin oraz ujawniając, w jaki sposób te związki mogą usztywniać i unieruchamiać proteazę dengi, praca wskazuje bardziej ukierunkowaną ścieżkę ku lekom, które pewnego dnia mogą zmienić groźne zakażenie w znacznie łatwiejszą do opanowania chorobę.
Cytowanie: Uddin, M.A.R., Paul, A.C., Islam, M.S. et al. Efficacy of phytochemicals derived from Artocarpus heterophyllus (Jackfruit) as inhibitors against NS2B/NS3 protease of dengue virus: an in-silico investigation. Sci Rep 16, 7543 (2026). https://doi.org/10.1038/s41598-026-38726-x
Słowa kluczowe: wirus dengi, fitochemikalia chlebowca, inhibitory proteazy, screening wirtualny, odkrywanie leków przeciwwirusowych