Clear Sky Science · pl
Chemiczna synteza nowych pochodnych aminopirymidyn-4-yl-1H-pirazolu jako inhibitów kinazy tyrozynowej śledziony (SYK)
Dlaczego zablokowanie jednego enzymu może pomóc w walce z rakiem i stanami zapalnymi
Nasz układ odpornościowy polega na szybkiej wewnętrznej komunikacji, która mówi komórkom, kiedy atakować intruzów, a kiedy się wyciszyć. Gdy te sygnały zawodzą, mogą napędzać choroby autoimmunologiczne i nowotwory. W badaniu omówiono obiecujące podejście do uciszenia tych wadliwych sygnałów poprzez zaprojektowanie małych, podobnych do leków cząsteczek, które selektywnie blokują kluczowy enzym — kinazę tyrozynową śledziony (SYK), znajdującą się w centrum wielu reakcji odpornościowych.
Przełącznik sygnału w centrum wielu chorób
SYK działa jak główny przełącznik w niektórych komórkach odpornościowych. Po aktywacji napędza stany zapalne, produkcję przeciwciał i wzrost komórek. W zdrowych warunkach pomaga zwalczać infekcje. Jednak w chorobach takich jak reumatoidalne zapalenie stawów, astma oraz w niektórych nowotworach krwi i narządów stałych aktywność SYK może być nadmierna, utrzymując komórki odpornościowe w stanie uaktywnienia i wspierając przeżycie guza. Ze względu na tę centralną rolę naukowcy na całym świecie pracują nad lekami blokującymi SYK, które będą wystarczająco silne, by działać, a jednocześnie na tyle precyzyjne, by nie trafiać w wiele innych enzymów i nie wywoływać skutków ubocznych.
Budowanie rodziny dopasowanych małych cząsteczek
Autorzy stworzyli nową serię spokrewnionych związków opartych na wspólnym szkielecie chemicznym nazwanym aminopirymidyn-4-yl-1H-pirazolem. Zaczynając od prostych bloków budulcowych, składali te elementy krok po kroku, a następnie modyfikowali jedną część struktury, aby uzyskać dziewięć końcowych kandydatów. Każdą cząsteczkę dokładnie sprawdzono standardowymi metodami analitycznymi, by potwierdzić jej strukturę i czystość. Takie modułowe podejście pozwoliło zespołowi badać, jak subtelne zmiany kształtu i elastyczności wpływają na sposób, w jaki te związki oddziałują z SYK.
Obserwacja, jak związki chwytają swój cel
Zanim przystąpiono do prac laboratoryjnych, badacze użyli symulacji komputerowych, by ocenić, jak mocno każda cząsteczka może przyczepić się do SYK. Obliczenia dokowania oszacowały, jak dobrze związki pasują do kieszeni wiążącej enzymu, wskazując jednego kandydata, oznaczonego jako 44, jako szczególnie obiecującego. Bardziej szczegółowe symulacje dynamiki molekularnej, w których kompleks białko–lek śledzono przez setki nanosekund, wykazały, że 44 tworzy wyjątkowo stabilne partnerstwo z SYK. Białko pozostawało zwarte, kluczowe kontakty utrzymywały się, a układ osiadał w jednej, niskoenergetycznej konformacji z wieloma silnymi wiązaniami wodorowymi, zwłaszcza z udziałem aminokwasów takich jak tryptofan i seryna, które pomagają utrzymać cząsteczkę.
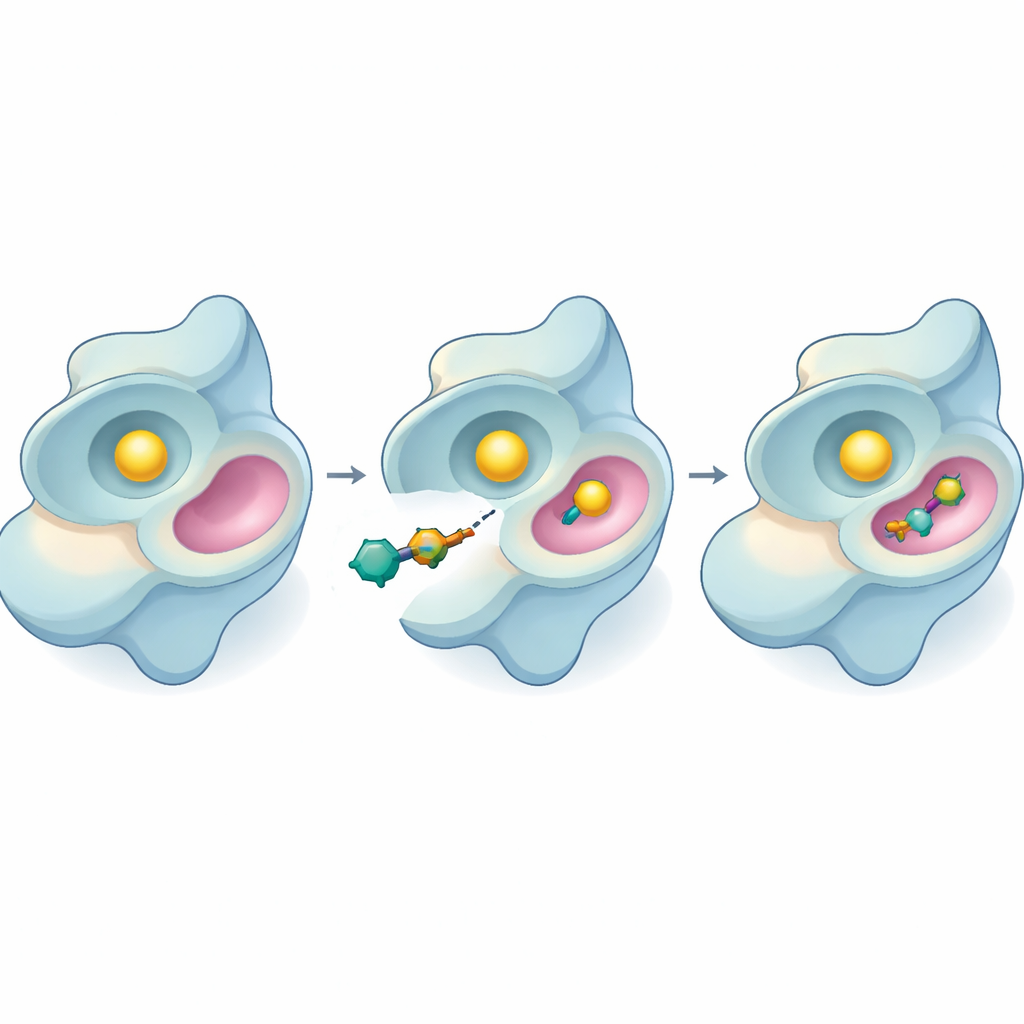
Testowanie nowych inhibitorów
Zespół przeszedł następnie do eksperymentów laboratoryjnych, stosując analizę opartą na świetle, która mierzy aktywność SYK w zużywaniu jego paliwa, ATP. Kilka nowych związków spowalniało enzym, ale ponownie wyróżnił się związek 44. Hamował SYK przy bardzo niskich stężeniach i stawał się bardziej skuteczny, im dłużej pozostawał z enzymem. Poprzez zmienianie ilości substratu obecnego w reakcji, badacze mogli wnioskować o mechanizmie działania 44: zamiast konkurować bezpośrednio z ATP w głównym miejscu aktywnym, wydaje się wiązać w innym, allosterycznym miejscu i zmieniać zachowanie enzymu z dystansu. To istotne, ponieważ inhibitory allosteryczne często zachowują efekt nawet przy wysokich poziomach ATP lub gdy mutacje zmieniają miejsce główne.
Co to może oznaczać dla przyszłych terapii
Razem, modele komputerowe i pomiary laboratoryjne tworzą spójny obraz: cząsteczka 44 silnie wiąże SYK, utrzymuje enzym w stabilnym, mniej elastycznym stanie i wyłącza jego aktywność poprzez pośredni, niekompetencyjny mechanizm. Dla osób niebędących specjalistami oznacza to, że badacze zidentyfikowali precyzyjny chemiczny klucz pasujący do zamka istotnego dla wielu chorób napędzanych przez układ odpornościowy, zamiast po prostu zablokować główne wejście. Choć przed nimi jeszcze wiele pracy — zwłaszcza testy w komórkach, u zwierząt i na szerszych panelach powiązanych enzymów — ten szkielet chemiczny stanowi obiecujący punkt wyjścia dla przyszłych leków mających na celu ujarzmienie szkodliwych stanów zapalnych i spowolnienie niektórych nowotworów przez celowanie w SYK.
Cytowanie: Rajasheker, K.V., Pallavi, M.S., Singh, P. et al. Chemical synthesis of novel aminopyrimidin-4-yl-1H-pyrazole derivatives as spleen tyrosine kinase (SYK) inhibitors. Sci Rep 16, 8323 (2026). https://doi.org/10.1038/s41598-026-38719-w
Słowa kluczowe: kinaza tyrozynowa śledziony, inhibitory kinaz, terapie przeciwnowotworowe, choroby autoimmunologiczne, leki allosteryczne