Clear Sky Science · pl
Adaptacyjna architektura fuzji wielowymiarowych cech z optymalizowanym uczeniem dla klasyfikacji nowotworów mózgu w MRI o wysokiej wierności
Dlaczego wczesne wykrycie nowotworów mózgu ma znaczenie
Nowotwory mózgu należą do najbardziej niebezpiecznych rodzajów nowotworów, a rozpoznanie nie tylko ich obecności, lecz także stopnia zaawansowania może decydować o skuteczności leczenia lub szybkim pogorszeniu stanu. Lekarze w dużym stopniu polegają na badaniach MRI, jednak nawet doświadczeni specjaliści mają trudności z odróżnieniem zmian wolnorosnących od agresywnych, gdy obrazy są zaszumione lub mają niski kontrast. W tym badaniu przedstawiono system sztucznej inteligencji zaprojektowany tak, by czytać skany mózgu wyraźniej i bardziej spójnie, dążąc do niemal perfekcyjnego rozróżnienia między zdrowym mózgiem a dwoma głównymi typami glejaków, najczęstszymi pierwotnymi guzami mózgu.
Oczyszczanie rozmytego obrazu
Obrazy medyczne często odbiegają od ideału. Guzy mogą zlewać się z otaczającą tkanką, a szum aparatu maskować drobne, lecz istotne szczegóły. Autorzy zaczynają od odbudowy samych obrazów MRI. Najpierw stosują starannie dobraną metodę regulacji kontrastu, wyraźniej oddzielając jasne i ciemne obszary skanu, dzięki czemu krawędzie nieprawidłowej tkanki stają się bardziej widoczne. Bezpośrednio po tym używają głębokiej sieci neuronowej wyspecjalizowanej w usuwaniu szumów, która nauczyła się eliminować plamkowy szum przy zachowaniu drobnych struktur. Testy pokazują, że ten dwustopniowy proces poprawy obrazu daje wyniki ostrzejsze i strukturalnie bliższe anatomii niż kilka standardowych technik stosowanych rutynowo w szpitalach.
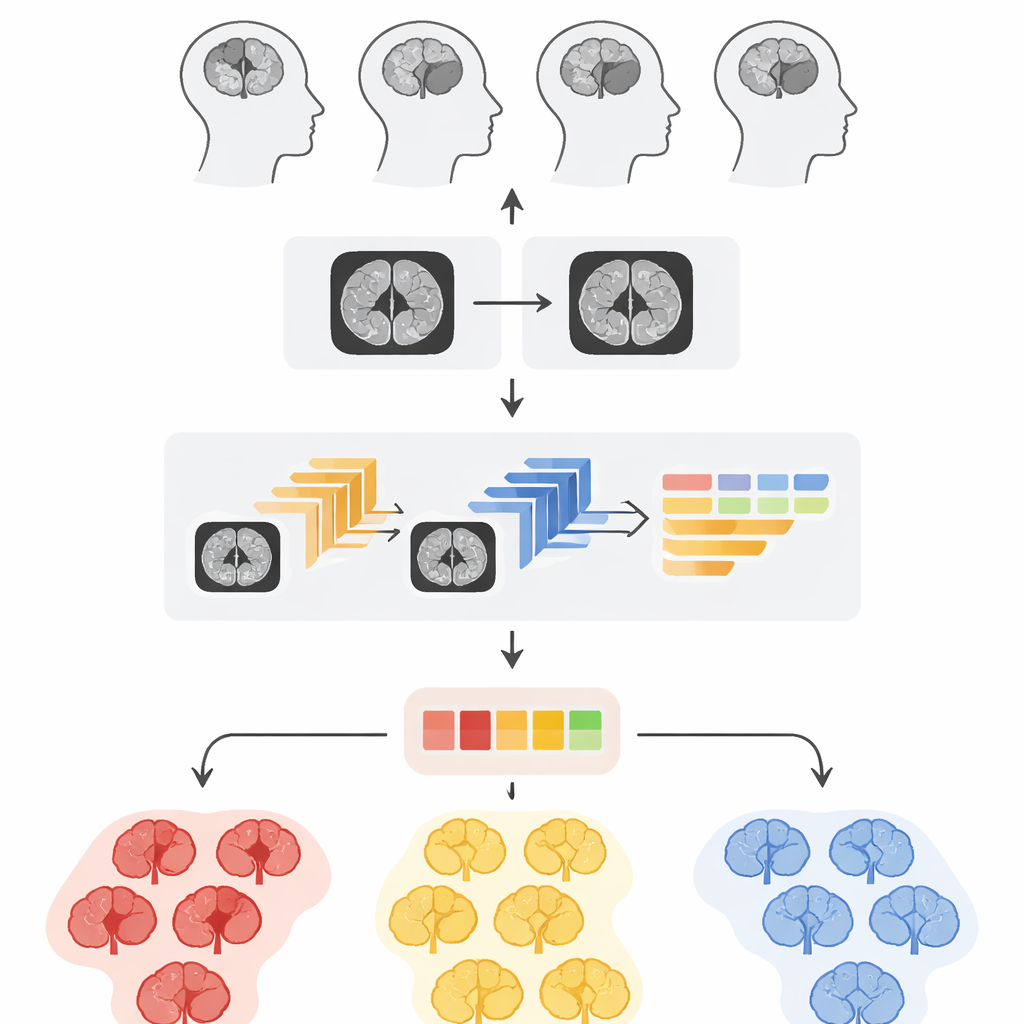
Nauka maszynowego widzenia podobnego do lekarzy
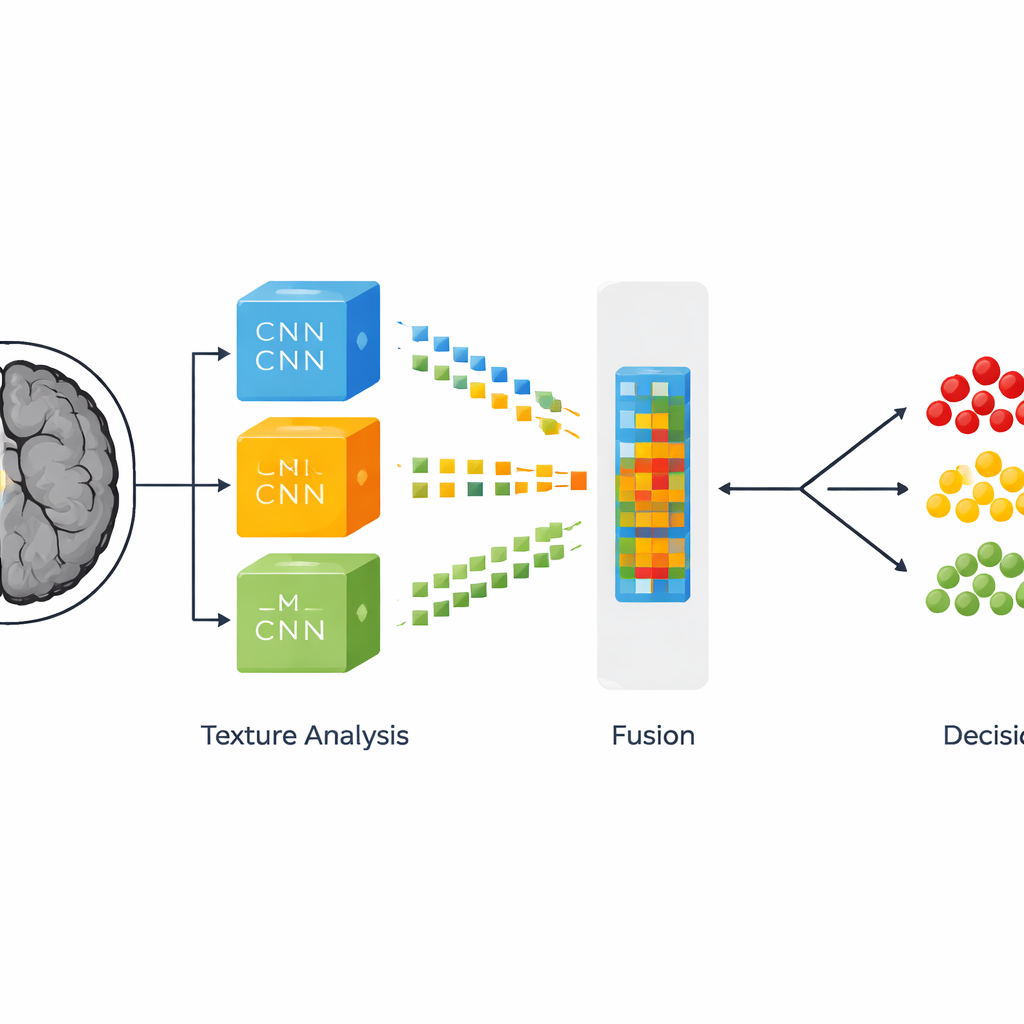
Gdy przekroczone i zmienione rozmiary przekrojów MRI są już oczywiste, system podejmuje subtelniejsze pytanie: czy mózg jest zdrowy, czy występuje w nim guz wolnorosnący, czy groźny guz agresywny? W tym celu badacze łączą dwa sposoby opisu obrazu. Pierwszy pochodzi z trzech potężnych, wstępnie wytrenowanych sieci neuronowych pierwotnie stworzonych do ogólnego rozpoznawania obrazów, a następnie dopasowanych do skanów mózgu. Sieci te uczą się dostrzegać wzorce wielkoskalowe, takie jak kształty i obszary przypominające guzy. Drugi opis koncentruje się na fakturze — drobnych zróżnicowaniach jasności i ziarnistości, które często rozróżniają stopnie zaawansowania guza. Analiza tekstury wykorzystuje klasyczne narzędzie statystyczne, które zlicza, jak często różne odcienie szarości pojawiają się obok siebie, przekształcając subtelne wzory powierzchni w liczbowe cechy zrozumiałe dla komputera.
Łączenie licznych wskazówek w jedną decyzję
Zamiast wybierać między uczeniem głębokim a analizą tekstury, autorzy je łączą. Z każdej z trzech sieci neuronowych wybierają trzy szczególnie informatywne warstwy wewnętrzne i spłaszczają ich złożone wzory aktywacji do długich list cech. Każdy z tych dziewięciu zbiorów łączy się następnie z odpowiadającymi mu pomiarami tekstury, tworząc to, co autorzy nazywają zintegrowanymi reprezentacjami cech. Te hybrydowe „odciski palców” przekrojów MRI są następnie przekazywane do kilku różnych algorytmów decyzyjnych, w tym lasów losowych, drzew z boostingiem oraz maszyn wektorów nośnych, jak również do ułożonego zespołu (stacked ensemble) mieszającego ich wyniki. Eksplorując liczne kombinacje, zespół identyfikuje, które zestawienie cech i klasyfikatorów daje najbardziej wiarygodne decyzje na tysiącach obrazów.
Pomiar wiarygodności, nie tylko surowej dokładności
Aby ocenić skuteczność systemu, badacze robią więcej niż podają jedną liczbę dokładności. Obliczają, jak często system poprawnie oznacza skany jako chore, jak często poprawnie uspokaja, że skan jest prawidłowy, i jak rzadko daje fałszywe alarmy. Najlepsza konfiguracja — wykorzystująca cechy z jednej konkretnej warstwy sieci neuronowej połączone z danymi tekstury i sklasyfikowane przez maszynę wektorów nośnych — poprawnie opisuje około 99 na 100 obrazów. Pokazuje też bardzo wysoką pewność, że wynik pozytywny rzeczywiście oznacza obecność guza, a wynik negatywny wskazuje brak groźnego rozrostu. Testy statystyczne potwierdzają, że ta najlepiej działająca konfiguracja nie jest wynikiem przypadku, lecz istotnie przewyższa alternatywne klasyfikatory, które próbowano.
Co to oznacza dla pacjentów i placówek
W praktyce badanie pokazuje, że starannie zaprojektowane połączenie lepszego oczyszczania obrazu, wielu modeli głębokiego uczenia i tradycyjnej analizy tekstury może zapewnić niemal bezbłędne sortowanie skanów MRI mózgu na kategorie: zdrowy, guz wolnorosnący i guz szybko rosnący. Cały proces potrafi przeanalizować pojedynczy przekrój skanu w znacznie poniżej sekundy, co sugeruje, że może być zastosowany w realnym środowisku szpitalnym bez opóźniania opieki. Choć system nie zastępuje ekspertów radiologów, może służyć jako niezawodne drugie oko, zwłaszcza na zatłoczonych oddziałach ratunkowych lub w regionach z niewielką liczbą specjalistów, pomagając szybko rozpoznać guzy agresywne i unikać nadmiernego leczenia łagodniejszych przypadków.
Cytowanie: Safy, M., Abd-Ellah, M.K., Bayoumi, E.S. et al. Adaptive multi-feature fusion architecture with optimized learning for high-fidelity brain tumor classification in MRI. Sci Rep 16, 8498 (2026). https://doi.org/10.1038/s41598-026-38672-8
Słowa kluczowe: MRI nowotworu mózgu, ocena złośliwości glejaka, Sztuczna inteligencja w obrazowaniu medycznym, fuzja cech, klasyfikacja guza