Clear Sky Science · pl
LncRNA FTX promuje włóknienie mięśnia sercowego przez pochłanianie miR-335-3p w celu regulacji szlaku TFEC/ILK
Dlaczego bliznowacenie serca ma znaczenie
Niewydolność serca dotyka dziesiątki milionów osób na całym świecie i często rozwija się skrycie przez lata. Głównym czynnikiem prowadzącym do tego pogorszenia jest włóknienie mięśnia sercowego — powolne, postępujące bliznowacenie mięśnia sercowego, które zwiększa jego sztywność i zmniejsza zdolność do pompowania krwi. W badaniu tym przeanalizowano molekularne „okablowanie”, które nakłania komórki serca do nadmiernego odkładania tkanki bliznowatej, i zidentyfikowano nowy łańcuch cząsteczek, które mogą być celem działań mających spowolnić albo nawet odwrócić ten szkodliwy proces.
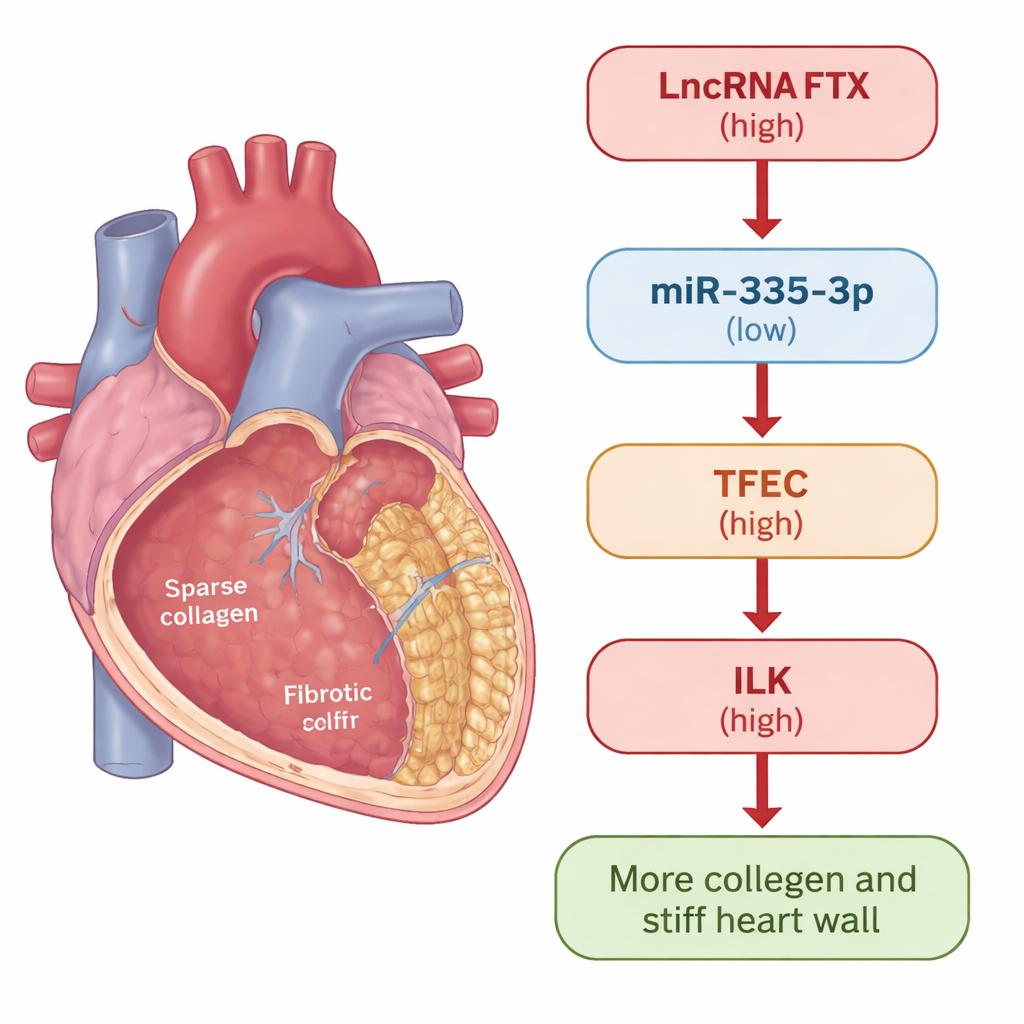
Bliższe spojrzenie na bliznowacenie serca
Gdy serce zostaje uszkodzone lub poddane stresowi, komórki wspierające zwane fibroblastami sercowymi wchodzą do akcji. W zdrowej reakcji naprawczej pomagają załatać uszkodzenia. W przewlekłej chorobie mogą jednak przejść w stan nadaktywności, wytwarzając nadmiar kolagenu i innych składników macierzy pozakomórkowej, co ostatecznie usztywnia ścianę serca. Naukowcy użyli dwóch modeli do badania tego procesu: myszy leczone izoproterenolem, który niezawodnie wywołuje włóknienie serca, oraz ludzkie fibroblasty sercowe wystawione na działanie cząsteczki sygnałowej TGF-β1, znanego wyzwalacza bliznowacenia. W obu modelach zmierzono, jak zmieniają się konkretne geny i białka w miarę rozwoju włóknienia.
Szkodliwa reakcja łańcuchowa wewnątrz komórek
Zespół skupił się na czynniku transkrypcyjnym o nazwie TFEC — białku, które znajduje się w jądrze komórkowym i aktywuje inne geny. Stwierdzono, że TFEC wraz z innym białkiem, integrin-linked kinase (ILK), był konsekwentnie zwiększony, gdy fibroblasty były sprowokowane do stanu sprzyjającego bliznowaceniu. Wyciszenie TFEC lub ILK znacznie zmniejszyło klasyczne markery włóknienia, takie jak α-aktyna mięśni gładkich i kolageny I i III, a także zahamowało ścieżki kontroli wzrostu (Akt/GSK3β i sygnalizacja Hippo) znane z promowania bliznowacenia tkanki. Eksperymenty mapujące wiązanie z DNA wykazały, że TFEC bezpośrednio przyłącza się do promotora genu ILK i zwiększa jego aktywność, lokując TFEC wyraźnie powyżej ILK w pro-włóknieniowym kaskadowym szlaku sygnalizacji.
Przełączniki RNA kontrolujące regulatora głównego
Aby zrozumieć, co reguluje sam TFEC, badacze zwrócili się ku RNA niekodującym — cząsteczkom RNA, które nie kodują białek, ale działają jako precyzyjne regulatory aktywności genów. Zidentyfikowali małe RNA, miR‑335‑3p, które było zmniejszone w tkankach i komórkach z włóknieniem. Podniesienie poziomu miR‑335‑3p obniżało TFEC, podczas gdy jego zahamowanie zwiększało TFEC; testy reporterowe potwierdziły, że miR‑335‑3p wiąże się bezpośrednio z komunikatami TFEC i utrzymuje ich poziom w ryzach. Następnie odkryto długie RNA niekodujące, nazwane FTX, które było podwyższone we włóknieniu i fizycznie oddziaływało z miR‑335‑3p. FTX działało jak molekularna gąbka: pochłaniało miR‑335‑3p, uniemożliwiając temu małemu RNA hamowanie TFEC. W rezultacie TFEC i ILK rosły, a fibroblasty produkowały więcej kolagenu tworzącego blizny.
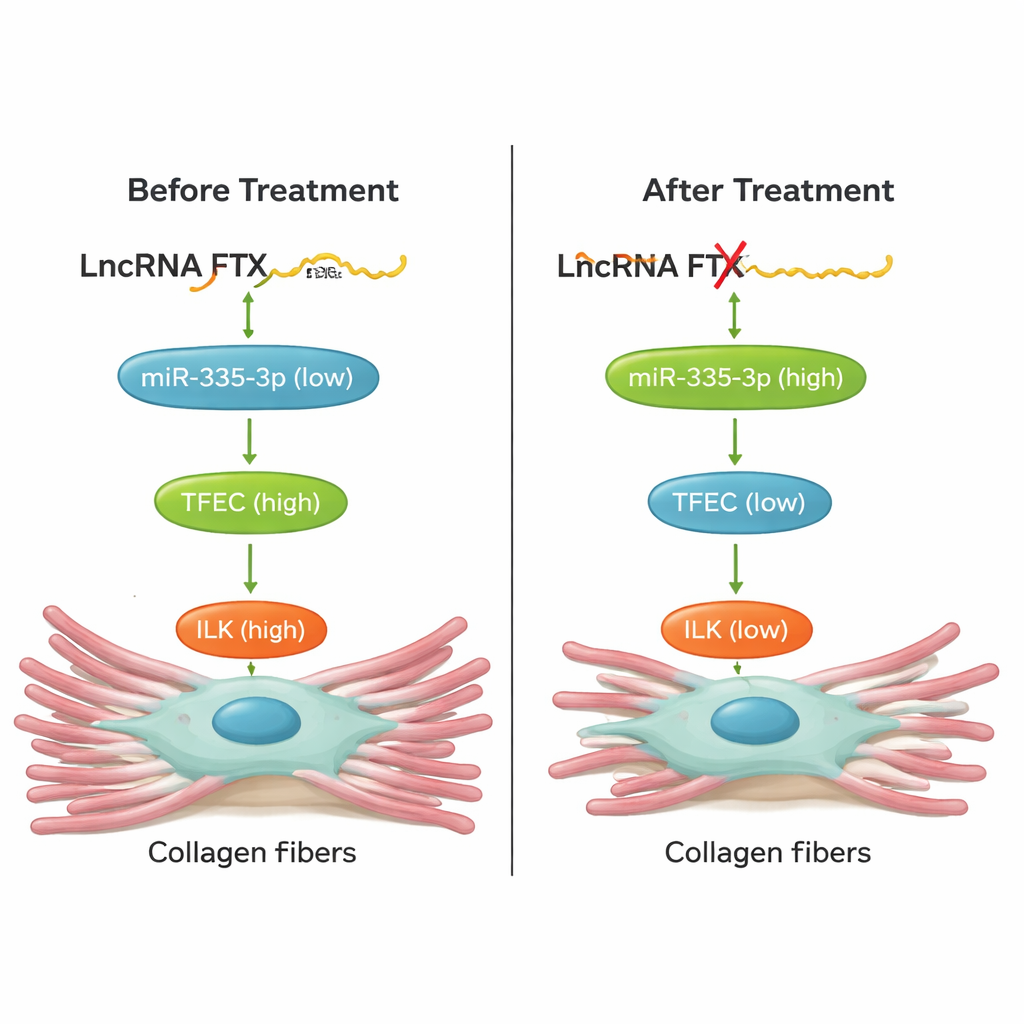
Od hodowli komórek do żywych serc
Co kluczowe, zespół sprawdził, czy przerwanie tego łańcucha faktycznie może chronić serca u zwierząt. U myszy poddanych działaniu izoproterenolu obniżenie TFEC, wyciszenie FTX w sercu przy użyciu wektora terapii genowej AAV9 albo zwiększenie miR‑335‑3p przy pomocy chemicznie stabilizowanego „agomiru” prowadziło do mniejszego nagromadzenia kolagenu i niższych poziomów markerów włóknienia w tkance sercowej. Interwencje te poprawiały też funkcję serca: objętość wyrzutowa i frakcja wyrzutowa wracały w kierunku normy, a szkodliwe wzrosty częstości akcji serca były ograniczone. Eksperymenty ratunkowe w komórkach wykazały, że zmiana jednego elementu osi FTX/miR‑335‑3p/TFEC/ILK przewidywalnie przesuwała pozostałe, co potwierdza, że jest to ściśle powiązany szlak, a nie luźna korelacja.
Co to oznacza dla przyszłych terapii
Dla osoby niezajmującej się specjalistycznie tematem, najważniejsze jest to, że autorzy zidentyfikowali nowy „dźwigniowy” punkt kontroli bliznowacenia serca. Długie RNA o nazwie FTX podnosi hamulec (miR‑335‑3p) z głównego przełącznika (TFEC), który następnie aktywuje ILK i dalsze sygnały sprzyjające bliznowaceniu, prowadząc do nadmiernego odkładania kolagenu i usztywnienia serca. Zmniejszając poziom FTX, przywracając miR‑335‑3p lub bezpośrednio blokując TFEC, udało się u myszy zmniejszyć bliznowacenie i poprawić funkcję pompowania. Chociaż potrzeba dalszych badań, by potwierdzić ten szlak u pacjentów i opracować bezpieczne terapie, łańcuch regulacyjny oparty na RNA oferuje kilka obiecujących punktów interwencji w niewydolność serca napędzaną włóknieniem.
Cytowanie: Yao, F., He, Z., Zheng, C. et al. LncRNA FTX promotes myocardial fibrosis by sponging miR-335-3p to regulate TFEC/ILK signaling. Sci Rep 16, 7340 (2026). https://doi.org/10.1038/s41598-026-38615-3
Słowa kluczowe: włóknienie mięśnia sercowego, niewydolność serca, RNA niekodujące, fibroblasty sercowe, sygnalizacja włóknienia