Clear Sky Science · pl
Proliferacja i efekty antyapoptotyczne wywołane przez DNMT3A p.R882C w komórkach raka trzustki
Dlaczego te badania mają znaczenie dla raka trzustki
Rak trzustki jest znany z późnego wykrywania, szybkiego rozprzestrzeniania się i słabej odpowiedzi na leczenie. Większość pacjentów ma gruczolakoraka przewodowego trzustki (PDAC), szczególnie agresywną postać choroby. To badanie bada niewielką zmianę w jednym genie, DNMT3A, i stawia ważne pytanie: czy ta subtelna modyfikacja może pomóc wyjaśnić, dlaczego niektóre raki trzustki rosną szybciej i opierają się śmierci komórkowej? Zrozumienie takich zmian może otworzyć drogę do wcześniejszego wykrywania i bardziej precyzyjnych, ukierunkowanych terapii.
Bliższe spojrzenie na śmiertelną chorobę
PDAC stanowi ponad 90% raków trzustki i ma pięcioletnie przeżycie poniżej 13%. Zwykle napędzany jest przez dobrze znane geny nowotworowe, takie jak KRAS i TP53, ale wielu pacjentów nadal nie odnosi korzyści z dostępnych terapii celowanych. Ostatnie prace sugerują, że kluczową rolę w tym raku odgrywają nie tylko mutacje genów, lecz także zmiany „epigenetyczne” — chemiczne oznaczenia na DNA kontrolujące, które geny są włączone lub wyłączone. DNMT3A jest jednym z głównych enzymów wprowadzających te chemiczne znaczniki, a jego defekty zostały już powiązane z nowotworami krwi, takimi jak ostra białaczka szpikowa.
W poszukiwaniu niebezpiecznych zmian w DNA
Naukowcy pobrali próbki guzów i przylegającej tkanki niekancerogennej od trzech pacjentów z umiarkowanie do słabo zróżnicowanym PDAC. Wykorzystali sekwencjonowanie eksomu, technikę odczytującą wszystkie regiony kodujące białka w genomie, a następnie zastosowali rygorystyczne filtry komputerowe, by oddzielić nieszkodliwe warianty DNA od takich, które prawdopodobnie zaburzają funkcjonowanie komórek. Z setek zmian zawęzili listę do 68 wysokiego ryzyka. Wśród nich wyróżnił się rzadki wariant w DNMT3A, znany jako p.R882C, ponieważ niemal nie występuje w dużych bazach populacyjnych i był konsekwentnie oceniany jako szkodliwy przez wiele narzędzi predykcyjnych.
Co ta mutacja robi wewnątrz komórek
DNMT3A to białko złożone z 912 aminokwasów, które pomaga ustanawiać wzorce metylacji DNA — chemiczne znaczniki działające jak przełączniki „włącz/wyłącz” dla genów. Zmiana p.R882C znajduje się w kluczowym regionie funkcjonalnym DNMT3A, gdzie może zaburzać aktywność enzymu. Przy użyciu modeli 3D zespół stwierdził, że ogólny kształt białka nie zmienił się dramatycznie, co sugeruje, że problem może leżeć w funkcji enzymu, a nie w jego fałdowaniu. Aby to przetestować, stworzyli linie komórkowe raka trzustki (PANC-1 i PaTu 8988t) produkujące albo normalne DNMT3A, albo wersję p.R882C, i porównali je z komórkami niosącymi pusty wektor kontrolny.
Szybszy wzrost, większa zdolność do przemieszczania się, mniejsza śmierć komórek
Co zaskakujące, mutacja p.R882C nie zmieniała ilości DNMT3A na poziomie RNA ani białka; ilość enzymu pozostała mniej więcej taka sama. Jednak jej obecność miała uderzające efekty na zachowanie komórek. W testach tworzenia kolonii i wzrostu komórek, komórki z mutantem DNMT3A tworzyły więcej kolonii i wykazywały silniejsze sygnały wzrostu niż te z wersją normalną. Testy gojenia ran i Trans‑well, mierzące tempo przemieszczania się komórek, wykazały, że komórki z mutacją poruszały się szybciej. Gdy zespół badał zaprogramowaną śmierć komórkową (apoptozę) za pomocą cytometrii przepływowej, komórki z mutacją p.R882C miały wyraźnie mniej komórek umierających, zarówno we wczesnych, jak i późnych stadiach apoptozy, co wskazuje na silną przewagę przeżyciową.
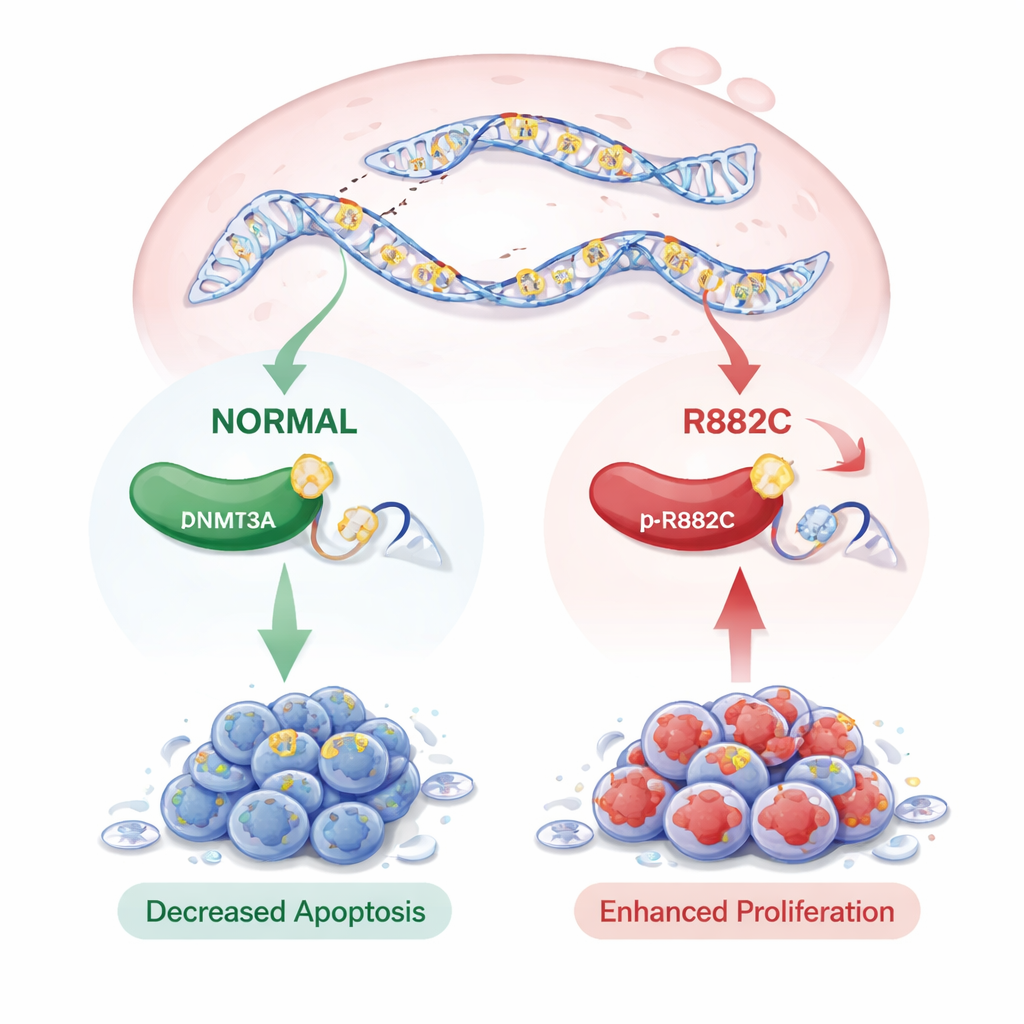
Co to może znaczyć dla przyszłej opieki
Składając te ustalenia razem, badanie sugeruje, że rzadka mutacja DNMT3A p.R882C pomaga komórkom raka trzustki rosnąć szybciej, łatwiej się przemieszczać i opierać autodestrukcji — cechy, które mogą przyczyniać się do progresji choroby. Chociaż mutacja nie zwiększa poziomów DNMT3A, prawdopodobnie zmienia aktywność enzymu i wzorzec oznakowań DNA w całym genomie, co przypomina obserwacje w niektórych nowotworach krwi. Autorzy zauważają, że zmiana jest rzadka i nie wykazała jeszcze wyraźnych związków z przeżyciem pacjentów w publicznych zbiorach danych, częściowo dlatego, że dostępne badania są niewielkie i często nie obejmują DNMT3A. Mimo to odkrycie tej mutacji w PDAC podkreśla potencjalnie istotnego nowego gracza w chorobie i stwarza możliwość, że w przyszłości DNMT3A p.R882C może służyć jako marker ryzyka lub cel dla bardziej dopasowanych terapii.
Cytowanie: Qu, Z., Mao, J., Qian, Y. et al. DNMT3A p.R882C driven proliferation and anti-apoptotic effects in pancreatic cancer cells. Sci Rep 16, 7659 (2026). https://doi.org/10.1038/s41598-026-38613-5
Słowa kluczowe: rak trzustki, mutacja DNMT3A, PDAC, metylacja DNA, terapia celowana