Clear Sky Science · pl
Edytowanie genomu w różnych gatunkach Dictyostelia umożliwia porównawcze genetyczne badania funkcjonalne ameb społecznych
Jak pojedyncze komórki współpracują
Na co dzień ameby są drobnymi samotnikami pełzającymi w glebie i żywiącymi się bakteriami. Niektóre z nich, zwane amebami społecznymi, potrafią jednak nagle zjednoczyć się w organizm wielokomórkowy z prymitywną „głową” i „łodygą”. Ten zmienny tryb życia daje naukowcom rzadką możliwość przyjrzenia się, jak proste komórki uczą się współpracować i specjalizować — kluczowym etapom w ewolucji złożonego życia. W nowym badaniu opisano zestaw narzędzi do edycji genomu, który wreszcie pozwala badaczom badać te zachowania nie tylko w jednym ulubionym modelu laboratoryjnym, lecz w kilku odległych gatunkach ameb.
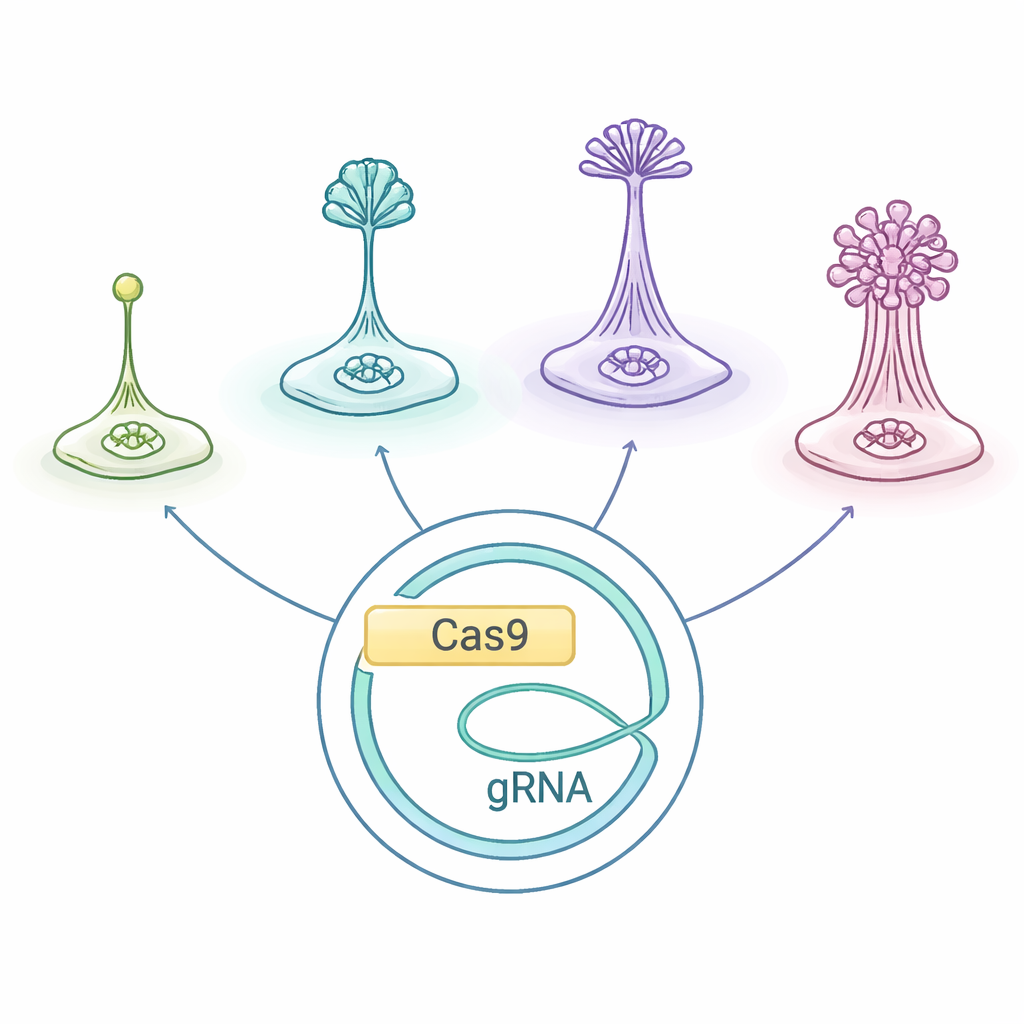
Maleńkie stworzenia o bogatym życiu społecznym
Ameby społeczne, zgrupowane jako Dictyostelia, żyją jako pojedyncze komórki, gdy pożywienia jest pod dostatkiem. Gdy zabraknie pokarmu, wysyłają chemiczne sygnały alarmowe i pełzają ku sobie, zbierając się w grudę, która przekształca się w miniaturowe „ciało owocujące”: kolumnę komórek-kolców poświęcających się, która wznosi wytrzymałe zarodniki w powietrze. Różne linie Dictyostelia budują te struktury na różne sposoby i z różnych typów komórek, co czyni je naturalnym laboratorium do badania, jak ewoluują ciała wielokomórkowe i podział pracy.
Jeden gatunek modelowy to za mało
Dotąd niemal wszystkie prace molekularne skupiały się na jednym gatunku, Dictyostelium discoideum, ponieważ jego geny stosunkowo łatwo modyfikować. Pozostało więc w dużej mierze nieprzebadanych ponad sto innych znanych gatunków — niektóre reprezentujące wcześniejsze gałęzie drzewa filogenetycznego Dictyostelia. Te pomijane gatunki mają różne historie życiowe, układy sygnalizacyjne i plany budowy ciała. Aby zrozumieć, jak wielokomórkowość zmieniała się w czasie, naukowcy muszą manipulować tymi samymi genami w wielu gatunkach i porównywać wyniki obok siebie.
Wprowadzenie CRISPR do zróżnicowanej rodziny ameb
Naukowcy zaadaptowali system edycji genów CRISPR/Cas9 pierwotnie zoptymalizowany dla D. discoideum i sprawdzili, czy działa on w całym drzewie Dictyostelia, włączając gatunki o wczesnym rozgałęzieniu oraz bardziej wyewoluowane. Użyli plazmidu — dodatkowego kolistego fragmentu DNA — który zawiera instrukcje dla „nożyczek molekularnych” Cas9, RNA prowadzącego wskazującego Cas9 na wybrany gen oraz marker oporności na lek. Wprowadzenie tego plazmidu do różnych ameb pozwoliło zespołowi przeciąć dwa dobrze poznane geny, nazwane stlA i pkaC, które są ważne dla sygnałów koordynujących agregację i prawidłowe formowanie ciała owocującego. W glebowej amebie Polysphondylium violaceum ta strategia niezawodnie dała mutanty z wyraźnymi defektami rozwojowymi, co pokazało, że zapożyczony system może działać poza zwykłym modelem.
Testowanie genów w różnych gatunkach
Następnie zespół przeszedł do bardziej odległych filogenetycznie gatunków, w tym Heterostelium pallidum z Grupy 2 oraz Cavenderia fasciculata z Grupy 1 — linii, które rozdzieliły się wcześniej w ewolucji. Używając tego samego projektu plazmidu, zaburzyli gen pkaC w obu gatunkach i stwierdzili, że mutanty nie agregowały i nie budowały normalnych ciał owocujących, odzwierciedlając poważne defekty obserwowane w D. discoideum. Ponieważ mutacje wywołane CRISPR tą metodą nie pozostawiają po sobie masywnych kaset selekcyjnych, powstałe linie były „wolne od markerów”. Ułatwiło to dodanie z powrotem wersji genu z D. discoideum i sprawdzenie, czy może ona zastąpić lokalną wersję. We wszystkich przypadkach obcy pkaC potrafił przywrócić wczesny etap agregacji, ale nie późniejsze formowanie dojrzałego ciała owocującego — dowód, że podstawowy zestaw sygnalizacyjny jest wspólny, podczas gdy precyzyjna kontrola czasu i pozycji ewoluowała w sposób specyficzny dla gatunku.
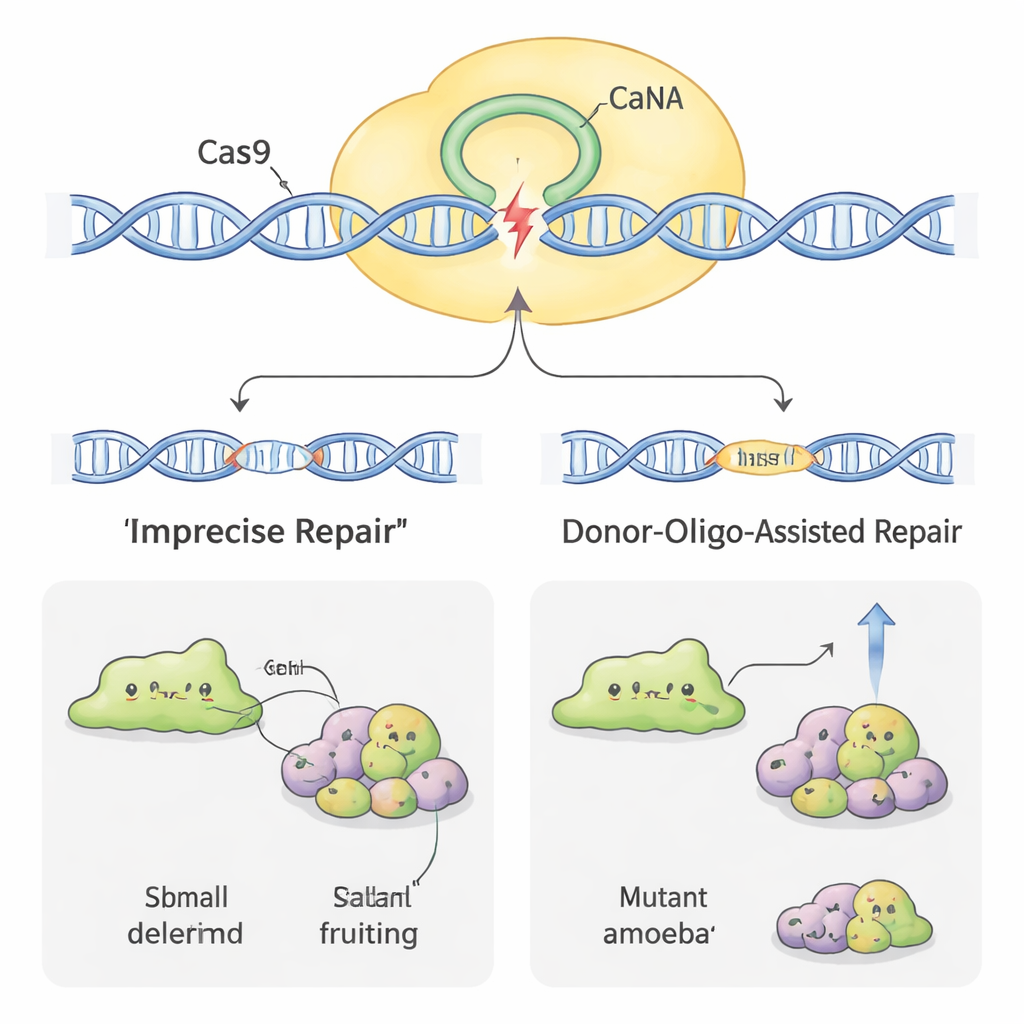
Usprawnianie efektywności edycji
Nie wszystkie ameby poddawały się edycji genomu równie łatwo. W niektórych gatunkach, takich jak H. pallidum, początkowy wskaźnik sukcesu był bardzo niski. Aby zwiększyć efektywność, naukowcy zastosowali inny trik: dodanie krótkich „donorowych” fragmentów DNA razem z plazmidem CRISPR. Donory te niosą mały znacznik i sygnał stopu otoczony krótkimi odcinkami zgodnymi z docelowym genem. Gdy komórka naprawia przecięcie Cas9, używając donora jako matrycy, niezawodnie uszkadza gen w łatwo rozpoznawalny sposób. W D. discoideum zwiększyło to udział wadliwych klonów i nawet pozwoliło uzyskać mutanty bez ciągłego stosowania selekcji lekiem. W bardziej opornym H. pallidum połączenie DNA-donorów z kilkudniowym leczeniem lekiem zwiększyło częstość mutacji prawie rzędem wielkości, zamieniając wcześniej rzadkie zdarzenia w coś zbliżonego do rutyny.
Otwieranie okna na początki złożoności
Dla laika szczegóły projektów plazmidów i matryc naprawczych mogą brzmieć technicznie, ale zysk jest szeroki: elastyczny zestaw narzędzi CRISPR działający w kilku gałęziach drzewa ameb społecznych. Dzięki niemu naukowcy mogą teraz porównywać, jak ten sam gen kształtuje rozwój w różnych gatunkach oraz jak subtelne zmiany w regulacji genów lub strukturze białek przyczyniają się do powstawania nowych typów komórek i planów budowy ciała. Innymi słowy, praca ta wyposaża badaczy w genetyczne narzędzia potrzebne do oglądania, na żywo i w szczegółach, jak ewolucja przerabiała jednokomórkowe organizmy, aby zbudować kooperatywne wielokomórkowe społeczeństwa.
Cytowanie: Oishi, S., Doi, S., Sekida, T. et al. Genome editing across Dictyostelia species enables comparative functional genetics of social amoebas. Sci Rep 16, 7457 (2026). https://doi.org/10.1038/s41598-026-38605-5
Słowa kluczowe: ameby społeczne, edycja genomu CRISPR, ewolucja wielokomórkowości, Dictyostelium, różnicowanie komórek