Clear Sky Science · pl
PLOD2 promuje proliferację, migrację i inwazję komórek raka jelita grubego poprzez szlak sygnałowy PI3K-AKT-GSK3β
Dlaczego otoczenie guza ma znaczenie
Rak jelita grubego jest jednym z najczęściej występujących nowotworów na świecie, a wiele osób zostaje zdiagnozowanych dopiero, gdy choroba jest już zaawansowana. W tym badaniu spojrzano poza same komórki nowotworowe, analizując ich otoczenie, czyli „sąsiedztwo” zbudowane z tkanek wspierających. Badacze skupili się na mało znanym enzymie o nazwie PLOD2 i wykazali, jak przyczynia się on do wzrostu i rozsiewu guzów jelita grubego, zmieniając zarówno otoczenie tkankowe, jak i kluczowe sygnały wzrostowe wewnątrz komórek.
Ukryty budowniczy rusztowania guza
Nasze narządy podtrzymywane są przez sieć białek zwaną macierzą zewnątrzkomórkową, której głównym składnikiem strukturalnym jest kolagen. PLOD2 to enzym, który chemicznie modyfikuje kolagen, wspomagając powstawanie silnych sieci wiązań krzyżowych i sztywnych włókien. Zespół przeanalizował duże bazy danych genetycznych i białkowych, a następnie zbadał próbki tkanek od 75 pacjentów. Stwierdzono, że poziomy PLOD2 były znacznie wyższe w tkance raka jelita grubego niż w przylegającej tkance prawidłowej. Wysokie PLOD2 wiązało się z bardziej zaawansowanymi guzami, przerzutami do węzłów chłonnych oraz naciekaniem wzdłuż nerwów, a pacjenci, których guzy zawierały więcej PLOD2, mieli krótszy czas przeżycia. Te wyniki wskazują na PLOD2 jako silny kandydat na marker agresywnej choroby.
Jak PLOD2 zwiększa agresję komórek nowotworowych
Aby wyjść poza korelacje widoczne w próbkach pacjentów, badacze skonstruowali w laboratorium linie komórkowe raka jelita grubego. W jednej linii zwiększyli produkcję PLOD2; w innej wyłączyli go. Komórki z nadmiarem PLOD2 szybciej się namnażały, tworzyły więcej kolonii i szybciej zamykały sztuczne „rany” na szalkach, co wskazywało na zwiększoną zdolność do przemieszczania się. Przechodziły też łatwiej przez porowate membrany i penetrowały żel naśladujący barierę tkankową w porównaniu z komórkami kontrolnymi. Gdy PLOD2 był wyciszony, wszystkie te właściwości osłabły. Razem te eksperymenty pokazują, że PLOD2 aktywnie napędza wzrost, migrację i inwazję komórek nowotworowych, a nie jest jedynie biernym towarzyszem zmian.
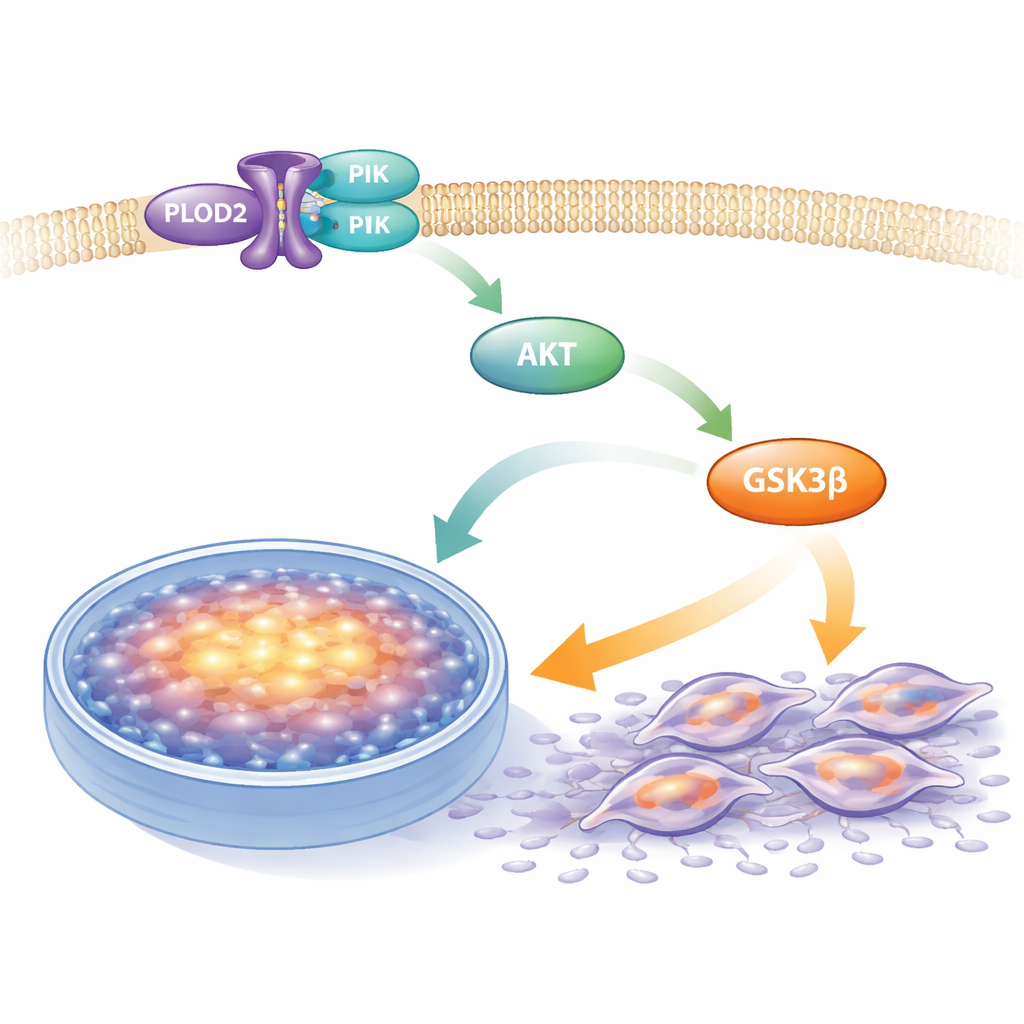
Włączanie sygnału sprzyjającego nowotworowi
Wewnątrz komórek nowotworowych wiele procesów kontrolowanych jest przez powiązane łańcuchy sygnałowe. Jeden z centralnych szlaków, znany ogólnie jako PI3K–AKT–GSK3β, pomaga komórkom przeżyć, dzielić się i dostosować metabolizm. Wykorzystując eksplorację danych i testy biochemiczne, badacze odkryli, że PLOD2 jest ściśle powiązany z tym szlakiem. Pokazali, że PLOD2 fizycznie wiąże się z PI3K, „enzymem startowym” w tym łańcuchu. Gdy poziomy PLOD2 były wysokie, zwiększała się aktywna (sfosforylowana) forma PI3K, AKT i GSK3β, mimo że całkowite ilości tych białek pozostawały niezmienione. Gdy PLOD2 został zmniejszony, aktywacja tego szlaku spadła, co sugeruje, że PLOD2 działa jak przełącznik włączający ten system sprzyjający wzrostowi i ruchliwości.
Testowanie szlaku za pomocą narzędzi chemicznych
Aby potwierdzić, że szkodliwe efekty PLOD2 zależą od tego łańcucha sygnałowego, zespół użył leków blokujących lub stymulujących PI3K. W komórkach nadprodukujących PLOD2 inhibitor PI3K osłabił aktywację AKT i GSK3β oraz spowolnił wzrost, migrację i inwazję komórek. W komórkach, w których PLOD2 został wyciszony, aktywator PI3K przywrócił aktywność szlaku i częściowo odzyskał zdolność komórek do proliferacji i migracji. Chociaż przywrócenie nie było pełne — co sugeruje, że PLOD2 może wpływać także na inne drogi — te eksperymenty mocno wspierają ideę, że PLOD2 promuje złośliwość głównie poprzez zasilanie osi sygnałowej PI3K–AKT–GSK3β.
Co to oznacza dla pacjentów
Dla osoby niebędącej specjalistą te molekularne szczegóły można sprowadzić do prostej opowieści: PLOD2 pomaga komórkom raka jelita grubego utwardzać i przebudowywać swoje otoczenie, jednocześnie włączając wewnętrzne obwody wzrostu. Dzięki tym dwóm działaniom guzy stają się bardziej skłonne do agresywnego wzrostu i rozsiewu. Badanie sugeruje, że pomiar PLOD2 mógłby pomóc zidentyfikować pacjentów wysokiego ryzyka, a leki skierowane przeciwko samemu PLOD2 — lub przeciw szlakowi, który on aktywuje — mogłyby w przyszłości stać się elementem bardziej spersonalizowanych terapii raka jelita grubego. Potrzebne będą dalsze badania na modelach zwierzęcych i w większych grupach pacjentów, ale PLOD2 wyróżnia się teraz jako obiecujący punkt uchwytu w walce z trudną chorobą.
Cytowanie: Fang, H., Zheng, J., Ren, S. et al. PLOD2 promotes proliferation, migration and invasion of colorectal cancer cells via PI3K-AKT-GSK3β signaling pathway. Sci Rep 16, 8118 (2026). https://doi.org/10.1038/s41598-026-38593-6
Słowa kluczowe: rak jelita grubego, PLOD2, mikrośrodowisko guza, sygnalizacja PI3K AKT, przerzuty nowotworowe