Clear Sky Science · pl
Izofluran nasila uprzednio istniejącą proteotoksyczność u dorosłych nicieni poprzez osłabienie sprawności mitochondriów
Dlaczego ma to znaczenie dla chirurgii i zdrowia mózgu
Wielu starszych pacjentów doświadcza po operacji zamieszania i problemów z pamięcią, stanu znanego jako delirium pooperacyjne. Badanie stawia proste, lecz pilne pytanie: czy gaz znieczulający używany do utrzymania pacjentów w nieprzytomności może uczynić podatne mózgi bardziej kruche? Wykorzystując drobne nicienie jako model zastępczy dla ludzi, badacze pokazują, że szeroko stosowany anestetyk izofluran może pogorszyć uprzednio istniejące uszkodzenia białek w komórkach nerwowych i mięśniowych przez podważenie zdrowia mitochondriów — generatorów energii komórkowej. Odkrycia sugerują nowe podejścia do ochrony pacjentów zagrożonych przed wejściem na salę operacyjną.
Anestetyk działający dopiero, gdy komórki są już zestresowane
Nie wszystkie mózgi reagują na znieczulenie w ten sam sposób. Zespół pracował z nicieniem C. elegans, mikroskopijnym robakiem, którego biologia dzieli wiele zasadniczych cech z ludźmi. Część robaków była normalna, inne zostały zmodyfikowane tak, by produkować lepkie białka powiązane z chorobami, które mają tendencję do tworzenia grudek, naśladując stany takie jak choroba Huntingtona. Gdy normalne robaki wdychały izofluran przez kilka godzin, ich ruch i równowaga białkowa pozostawały w dużej mierze nienaruszone dni później. Ale u robaków już obciążonych agregującymi białkami ta sama ekspozycja na anestetyk prowadziła do wyraźnego i trwałego pogorszenia ruchu, co jest znakiem, że ich komórki miały trudności z radzeniem sobie. Innymi słowy, izofluran działał jak dodatkowy impuls na system, który już był bliski załamania.
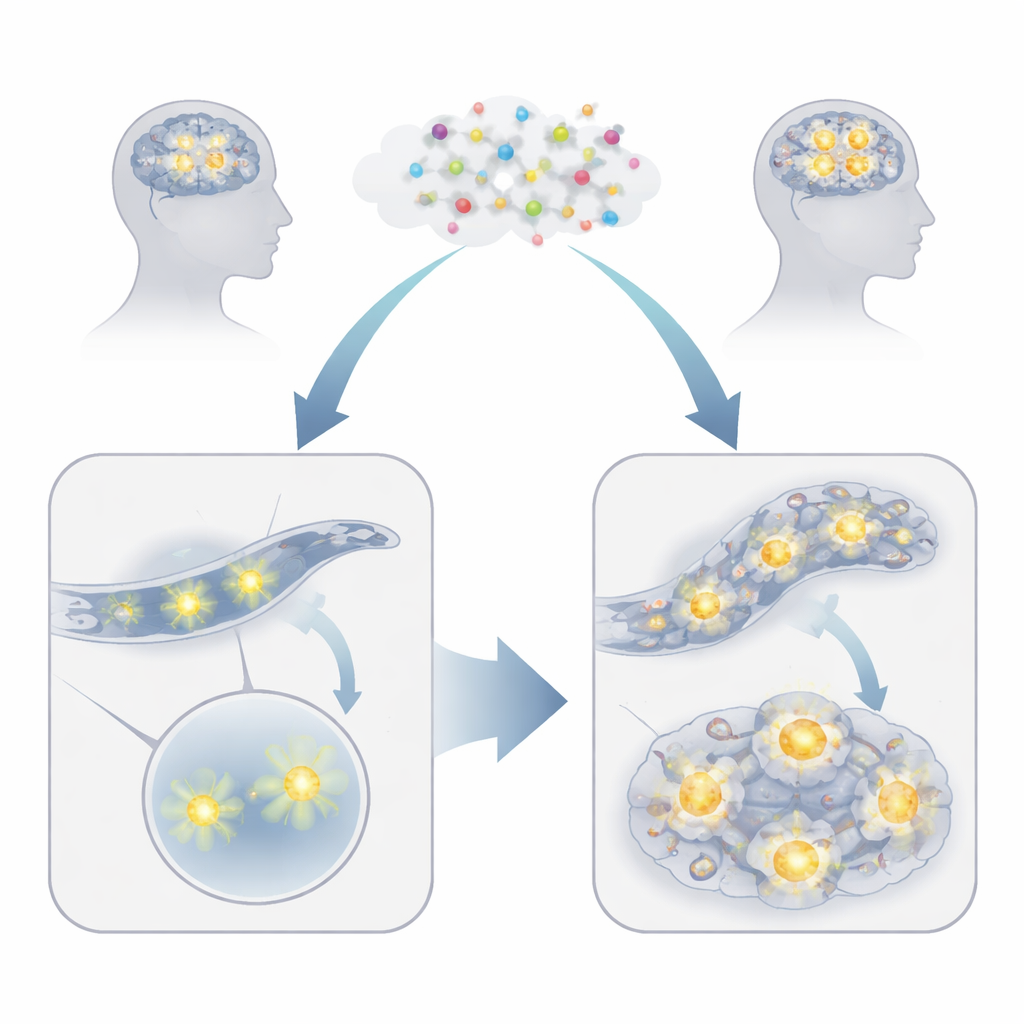
Ukryte zmiany w skupiskach białek i aktywności genów
Badając dokładniej, naukowcy odkryli, że u wrażliwych, znieczulonych robaków tworzyło się więcej widocznych ognisk białkowych — jasnych punktów, w których gromadzą się lepkie białka — a mimo to paradoksalnie było mniej dużych, odpornych na detergenty agregatów białkowych. Ten wzorzec sugeruje przesunięcie w stronę mniejszych, bardziej toksycznych zespołów białkowych zamiast łagodnych, ściśle upakowanych grudek. Jednocześnie komórki robaków przebudowały swoją aktywność genową. Setki genów związanych z reakcjami na stres, metabolizmem i usuwaniem białek zostało w górę lub w dół regulowanych po ekspozycji na izofluran, niezależnie od tego, czy robaki nosiły ryzykowne białka. Niektóre pomocnicze białka, jak określone chaperony wspomagające fałdowanie białek, zostały zwiększone, co wskazuje, że komórki wykryły problem i próbowały zareagować. Jednak przynajmniej jeden chaperon, HSP‑16.41, faktycznie pogarszał sytuację w obecności izofluranu, co podkreśla, jak system ochronny może stać się szkodliwy w niewłaściwych warunkach.
Mitochondria na celowniku
Najbardziej uderzające zmiany pojawiły się, gdy zespół zbadał, które białka faktycznie kończyły w nierozpuszczalnych grudkach. U robaków z uprzednim stresem białkowym wiele nowo zagregowanych białek pochodziło z mitochondriów, szczególnie z ich wewnętrznego sprzętu i kanałów importu białek. Gdy badacze obniżyli poziom tomm‑20 — kluczowego białka „drzwiowego”, które pomaga transportować inne białka do mitochondriów — izofluran nie był już w stanie pogorszyć problemów z ruchem, zarówno w komórkach mięśniowych, jak i nerwowych. Inne elementy mitochondrialne, takie jak podjednostka kompleksu I GAS‑1, również wpływały na wrażliwość robaków na anestetyk. Razem te ustalenia wskazują na mitochondria jako centralną scenę, na której rozgrywa się toksyczne partnerstwo między znieczuleniem a uszkodzeniem białek.
Kiedy komórkowe sprzątanie idzie za daleko
Komórki utrzymują mitochondria poprzez szlak recyklingu zwany mitofagią, który oznacza uszkodzone organelle do usunięcia. Zespół odkrył, że ten proces, zwykle ochronny, może stać się bronią obosieczną. Ekspozycja na izofluran zwiększała aktywność kilku genów związanych z ogólnym sprzątaniem komórkowym i recyklingiem mitochondriów. Jednak blokowanie konkretnych składników mitofagii, w szczególności kinazy PINK‑1 oraz receptorów ładunku SQST‑1, SQST‑2 i LGG‑1, w rzeczywistości chroniło robaki przed szkodliwymi efektami anestetyku. U robaków z wyzwaniem ze strony lepkich białek izofluran wydawał się przechylać równowagę w stronę nadmiernego usuwania mitochondriów bez wystarczającej ich wymiany, pozostawiając komórki z mniejszą liczbą zdrowych „elektrowni”. Wspierając ten pomysł, mała cząsteczka znana z poprawiania sprawności mitochondriów, VL‑004, pomogła przywrócić ich obfitość i częściowo uratowała ruchliwość u znieczulonych, stresowanych białkowo robaków.
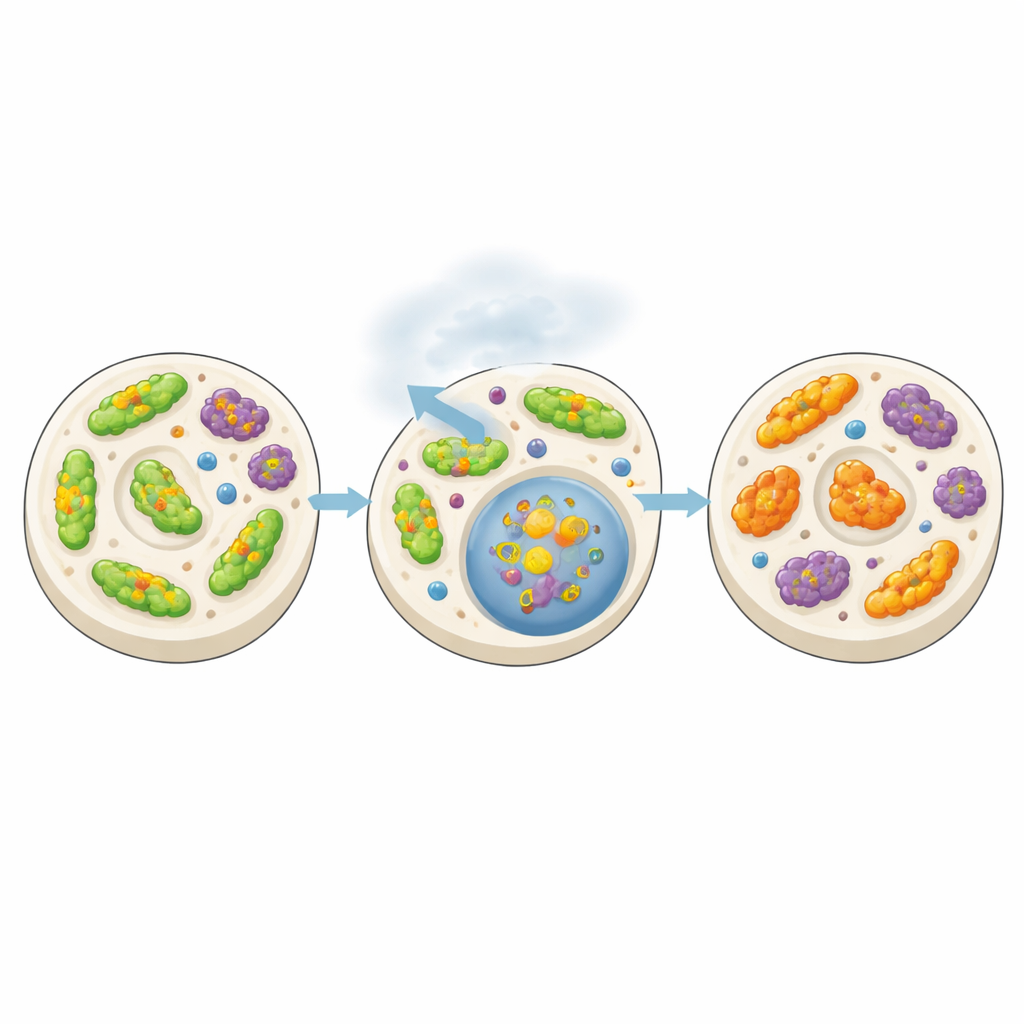
Co to może znaczyć dla pacjentów po operacji
Mówiąc krótko, praca ta sugeruje, że izofluran może pogłębiać uszkodzenia białek i spadek funkcji, ale głównie w komórkach już żyjących na krawędzi z powodu podatności związanej z wiekiem lub dziedzicznej wrażliwości. Przez nadmierne aktywowanie sprzątania mitochondrialnego i niezdolność do wspierania wzrostu nowych mitochondriów, anestetyk pozostawia te komórki ubogie w energię i mniej zdolne do radzenia sobie z toksycznymi gatunkami białkowymi. Chociaż robaki nie są ludźmi, podstawowe procesy badane tutaj są zachowane między gatunkami, a wyniki oferują mechanistyczne ogniwo łączące lotne anestetyki, stres mitochondrialny i długotrwałe problemy poznawcze po operacji. Badanie stawia możliwość, że ostrożne dostrojenie sprawności mitochondriów — być może za pomocą leków takich jak VL‑004 lub przez celowanie w szlaki mitofagii — mogłoby pomóc zmniejszyć ryzyko delirium pooperacyjnego u pacjentów z uprzednimi zaburzeniami poznawczymi lub problemami z gospodarką białkową.
Cytowanie: Elami, T., Zhu, H., Bruck-Haimson, R. et al. Isoflurane aggravates pre-existing proteotoxicity in adult nematodes by suppressing mitochondrial fitness. Sci Rep 16, 8098 (2026). https://doi.org/10.1038/s41598-026-38591-8
Słowa kluczowe: delirium pooperacyjne, izofluran, mitochondria, agregacja białek, C. elegans